Что такое электротерапия. Какие виды электротерапии существуют. Как работает электротерапия. Для чего применяется электротерапия. Какие заболевания лечат с помощью электротерапии. Какие противопоказания есть у электротерапии. Как проводится процедура электротерапии.
Что такое электротерапия и как она работает
Электротерапия — это метод физиотерапевтического лечения, основанный на воздействии на организм различными видами электрического тока. При электротерапии используются постоянные, импульсные и переменные токи различной частоты, формы, силы и напряжения.
Воздействие электрического тока на организм вызывает следующие эффекты:
- Усиление кровообращения в тканях
- Активизация обменных процессов
- Снятие болевых ощущений
- Расслабление или стимуляция мышц
- Противовоспалительное действие
- Улучшение трофики тканей
Механизм действия электротерапии основан на том, что электрический ток оказывает влияние на ионный состав тканей, проницаемость клеточных мембран, возбудимость нервных окончаний. Это запускает каскад физиологических реакций в организме, приводящих к лечебному эффекту.
.jpg)
Основные виды электротерапии
Существует несколько основных видов электротерапии, различающихся по типу используемого тока:
Гальванизация
При гальванизации применяется постоянный непрерывный ток низкого напряжения (до 80 В) и малой силы (до 50 мА). Гальванический ток оказывает противовоспалительное, обезболивающее, сосудорасширяющее действие.
Электрофорез
Электрофорез сочетает действие гальванического тока с введением лекарственных веществ через кожу или слизистые оболочки. Это позволяет создать высокую концентрацию препарата в зоне воздействия.
Диадинамотерапия
При диадинамотерапии используются импульсные токи низкой частоты (50-100 Гц). Оказывает выраженное обезболивающее и противоотечное действие, улучшает кровообращение.
Амплипульстерапия
Метод основан на воздействии синусоидальными модулированными токами частотой 5000 Гц. Обладает обезболивающим, противовоспалительным, сосудорасширяющим эффектом.
Показания к применению электротерапии
Электротерапия применяется при широком спектре заболеваний и патологических состояний:
- Заболевания опорно-двигательного аппарата (артриты, артрозы, остеохондроз, травмы)
- Заболевания периферической нервной системы (невралгии, невриты, радикулиты)
- Заболевания сердечно-сосудистой системы (гипертоническая болезнь, ИБС)
- Заболевания органов дыхания (бронхиты, пневмонии)
- Заболевания желудочно-кишечного тракта (гастриты, язвенная болезнь)
- Гинекологические заболевания
- Кожные заболевания
Электротерапия эффективна как в острый период заболевания, так и на стадии реабилитации. Она позволяет ускорить выздоровление и предотвратить осложнения.
Противопоказания к электротерапии
Несмотря на широкий спектр показаний, у электротерапии есть ряд противопоказаний:
- Онкологические заболевания
- Системные заболевания крови
- Активный туберкулез
- Острые инфекционные заболевания
- Беременность
- Наличие кардиостимулятора
- Индивидуальная непереносимость электрического тока
Перед назначением электротерапии врач обязательно оценивает наличие противопоказаний у пациента. При некоторых состояниях электротерапия может применяться с осторожностью под контролем специалиста.

Как проводится процедура электротерапии
Процедура электротерапии проводится следующим образом:
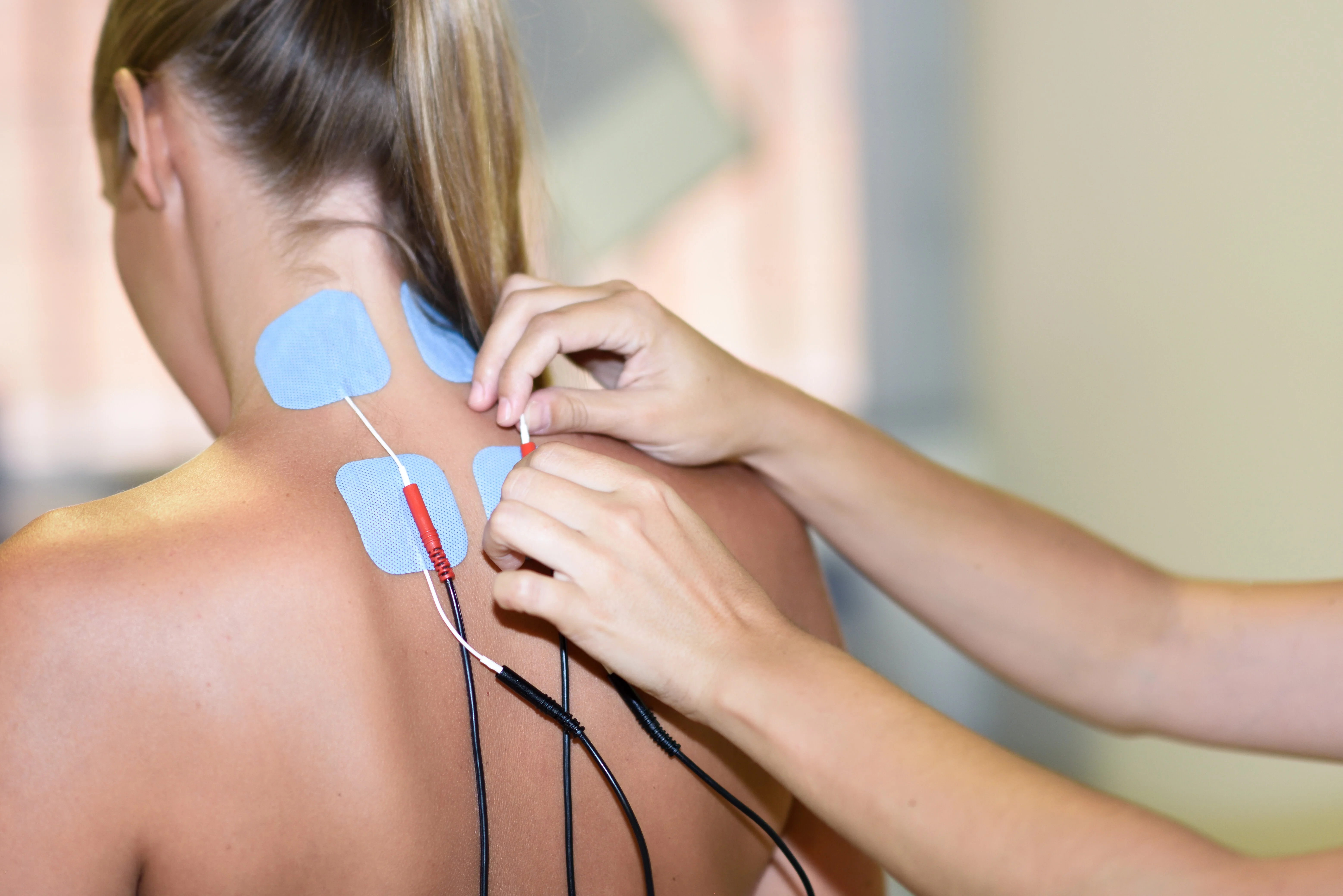
- Пациент располагается в удобном положении, обнажая область воздействия
- На кожу накладываются электроды, смоченные водой или специальным раствором
- Врач устанавливает на аппарате необходимые параметры тока
- Постепенно увеличивается сила тока до появления у пациента ощущения легкого покалывания или вибрации
- Процедура длится 10-20 минут
- По окончании сила тока плавно уменьшается, электроды снимаются
Курс электротерапии обычно составляет 10-15 процедур, проводимых ежедневно или через день. При необходимости курс повторяют через 1-2 месяца.
Современные аппараты для электротерапии
Современное оборудование для электротерапии позволяет точно дозировать параметры воздействия и делает процедуры максимально комфортными для пациента. Аппараты имеют следующие особенности:
- Микропроцессорное управление
- Большой выбор предустановленных программ лечения
- Возможность индивидуальной настройки параметров
- Автоматический контроль контакта электродов с кожей
- Система защиты от поражения током
- Эргономичный дизайн и удобный интерфейс
Ведущие производители постоянно совершенствуют аппараты для электротерапии, расширяя их функциональные возможности и повышая безопасность применения.

Эффективность электротерапии
Эффективность электротерапии подтверждена многочисленными клиническими исследованиями. При правильном применении она позволяет достичь следующих результатов:
- Уменьшение болевого синдрома на 50-70%
- Сокращение сроков лечения на 20-30%
- Снижение потребности в медикаментозной терапии
- Улучшение качества жизни пациентов
- Профилактика обострений хронических заболеваний
Электротерапия хорошо сочетается с другими методами лечения, усиливая их эффект. При этом она практически не имеет побочных эффектов при правильном применении.
Перспективы развития электротерапии
Электротерапия продолжает активно развиваться. Основные направления совершенствования метода включают:
- Разработку новых форм токов и режимов воздействия
- Создание портативных аппаратов для домашнего применения
- Комбинирование электротерапии с другими физиотерапевтическими факторами
- Внедрение систем биологической обратной связи
- Расширение показаний к применению метода
Электротерапия остается одним из ведущих методов физиотерапевтического лечения и реабилитации. Ее эффективность и безопасность в сочетании с постоянным совершенствованием технологий обеспечивают широкие перспективы применения в медицине.

Тема: «Электролечение» (импульсные токи).
1)Первый этап: Один электрод S=200 см. помещают в области поясничного отдела позвоночника, а второй S=50 см. – на животе в области проекции слепой кишки. Продолжительность воздействие 15 минут.
Второй этап: Первый электрод оставляют в области поясницы, второй перемещают на область проекции нисходящего отдела толстой кишки. Продолжительность воздействия 15 минут. Вид тока – синусоидальные модулированные токи при частоте модуляции 20-10Гц, глубина её 100%, ПП. Лучше проводить ручные включения и прерывания тока, делая посылки тока и пауз более продолжительными – соответственно 20-40 секунд (синусоидальные модулированные токи – ПМ – первый род работы, экспоненциальные токи – без автоматической модуляции). Сила тока – до получения отчётливых, но не болезненных сокращений мышц брюшной стенки под электродом. Процедуры проводят ежедневно. Курс до 15 процедур.
Настроить аппарат на параметры электростимуляции.
10. Включить
ритмическую или ручную стимуляцию.
Включить
ритмическую или ручную стимуляцию.
11.Установить вид тока.
12.Установить частоту импульсов.
13.Установить длительность.
14.Установить частоту ритмической модуляции.
15.После появления на экране осциллоскопа нулевой линии стрелку измерительного прибора следует установить в нулевое положение.
16.Предупредить пациента о начале процедуры.
17.Плавнр вращать ручку регулятора силы тока, до появления у него безболезненного четкого мышечного сокращения.18.По окончании процедуры ручку регулятора силы тока необходимо повернуть влево до отказа.
19.Тумплер включения аппарата поставить в положение « выкл.».
20.Отсоединить провода от аппарата.
21.Снять с пациента электроды.
22.Отключить аппарат от сети.
23.Вынуть вилку сетевого провода из розетки.
24.Гидрофильные прокладки прополоскать.
25.Предложить пациенту отдохнуть.
26.Сделать отметку в учетно-отчетной документации.
3) ДДТ
4)
1. Не
все лекарственные вещества могут быть
использованы для его проведения,
Не
все лекарственные вещества могут быть
использованы для его проведения,
2.Нельзя точно дозировать лекарственное вещество,
3.Не создается большой концентрации лекартсвен. вещества в депо,
4.Иногда отмечается противоположное действие лекарства и постоянного тока.
5) В организме ток распространяется по пути наименьшего омического сопротивления (по межклеточным пространствам, кровеносным и лимфатическим сосудам, оболочкам нервных стволов, мышцам). Через неповрежденную кожу ток проходит в основном по выводным протокам потовых желез. В живом организме электропроводимость ткани не является величиной постоянной. Ткани, находящиеся в состоянии отека, гиперемии, пропитанные тканевой жидкостью или воспалительным экссудатом, обладают более высокой электропроводимостью, чем здоровые.
Электропроводимость зависит от состояния нервной и гормональной систем.
Прохождение
тока через биологические ткани
сопровождается физико-химическими
сдвигами, которые лежат в основе
первичного действия гальванизации на
организм. Ток подводится к телу пациента
через контактно наложенные электроды
При гальванизации больше значение имеет
правильность расположения электродов
«Катод – Анод». Так, при гальванизации
головы при расположении в области лба
– Анода-снижает возбудимость головного
мозга, а при расположении в области лба
Катода – повышает.
Ток подводится к телу пациента
через контактно наложенные электроды
При гальванизации больше значение имеет
правильность расположения электродов
«Катод – Анод». Так, при гальванизации
головы при расположении в области лба
– Анода-снижает возбудимость головного
мозга, а при расположении в области лба
Катода – повышает.
6) Электротравмы (немедленно прекратить манипуляцию , вырубить рубильник , оттащить провода сухой веревкой от пациента, оттащить его не прикасаясь к телу пациента /только за одежду/, вызвать врача через 3 лицо , психологическая помощь , дать экстракт валерианы , дать чай, тепло укрыть; при тяжелой степени : ИВЛ + закрытый массаж сердца + нашатырный спирт. Если не помогло ,то доставляют в реанимацию, госпитализация пациента.
Остановка сердца : доврачебная помощь: вызвать врача через 3 лицо ,массаж сердца + ИВЛ , медикоментозно (Норадреналин в/в + 2 – 5 мл 5% кальция хлорида ,дополнительно вводят 8% гидрокарбонат натрия 1,5 – 2 мл на 1 кг массы тела.
Ожоги
: Успокоить пациента ,по необходимости
вызвать врача (зависит от степени
ожога),Обработать а/бак раствором
,наложить сухую или смазанную мазью
повязку.
Вариант №20
Дано: Больной, 35 лет.
Ds: Функциональное расстройство Н.С.
Назначено: Электросон
Вопросы: 1) Как располагают электроды при данной методике?
2) Какова последовательность мед. сестры при проведении электросна? (Алгоритм действий)
3) какие методики отпуска электросонтерапии существуют?
4) В чем недостатки данной процедуры,
5) Каким образом подаваемый ток подводится к телу пациента?
6) Возникновение какой неотложной ситуации возможно при проведении данной терапии?
Электрофорез по Вермелю
Среди современных методов электролечения электрофорез занимает особое место. Во время этой процедуры используется совместное воздействие медикаментов и постоянного электрического тока. Применение электрофореза выглядит следующим образом:
- специальная гидрофильная прокладка пропитывается лекарством;
- прокладка размещается на теле пациента в области требуемого воздействия;
- на неё накладываются электроды с соответствующим зарядом
Лекарственные вещества, растворяясь, диссоциируют на ионы (заряженные частицы). При попадании таких растворов в электрическое поле ионы приобретают способность к перемещению. Благодаря этому они проникают в ткани организма, оказывая терапевтическое действие.
При попадании таких растворов в электрическое поле ионы приобретают способность к перемещению. Благодаря этому они проникают в ткани организма, оказывая терапевтическое действие.
Основным эффектом от использования постоянного электрического тока является активизация обменных процессов в клетках и кровообращения в тканях. Кроме того, вещество, используемое для электрофореза, поставляется в патологический очаг в виде ионов, что значительно упрощает его попадание в ткани. В результате воздействие лекарственного средства локализируется, что значительно снижает риск появления аллергических реакций. Другое важное преимущество электрофореза – это создание «депо» препарата в тканях после процедуры и постепенное его поступление в кровь на протяжении целых 15-20 суток.
В современной физиотерапии существует несколько основных разновидностей электрофореза. Одна из них – метод электрофореза по Вермелю, также именуемый общей гальванизацией. Его главной особенностью является расположение электродов:
- прокладку большего размера, пропитанную лекарственным средством, размещают между лопатками, накладывая сверху электрод, соединяемый с аппаратом для гальванизации;
- две гидрофильные прокладки меньшего размера, поверх которых также размещаются электроды, накладываются на область икроножных мышц.

Сила тока при электрофорезе по Вермелю составляет 3—10 мА. Продолжительность самой процедуры – 20-40 минут, при этом в курсе физиотерапии может быть до 20 сеансов.
Во время общей гальванизации в организме происходят следующие процессы:
- изменяется проницаемость белковых субстанций;
- усиливается процесс осмоса и диффузии;
- наблюдается общая интенсификация обмена веществ.
В результате использования упомянутого метода организм пациента воспринимает поставляемый через кожу препарат гораздо эффективнее. К этому добавляется терапевтическое воздействие самих электрических токов, способствующих процессам регенерации.
Курс электрофореза по Вермелю может назначаться взрослым и детям при следующих патологиях:
- нарушения обмена веществ;
- заболевания, связанные с нарушениями периферического кровообращения;
- ослабление иммунитета;
- неврозоподобные состояния;
- вегетативно-трофические нарушения.

По результатам многочисленных исследований, после курса электрофореза по Вермелю у пациента наблюдались следующие реакции:
- общее улучшение состояния здоровья и самочувствия;
- активизация жизненных сил, повышение работоспособности;
- активизация защитных функций организма;
- улучшение кровообращения;
- противовоспалительный эффект и т.д.
Несмотря на эффективность электрофореза, для этого физиотерапевтического метода существует ряд противопоказаний. В частности, общую гальванизацию не рекомендуется проводить при:
- нарушении целостности кожных покровов в области воздействия;
- непереносимости постоянного электрического тока;
- нарушениях кожной чувствительности;
- острых воспалительных процессах любой локализации;
- склонности к кровотечению;
- некоторых заболеваниях сердечно-сосудистой системы и т.д.
Перед прохождением курса электрофореза по Вермелю в обязательном порядке требуется консультация нашего физиотерапевта.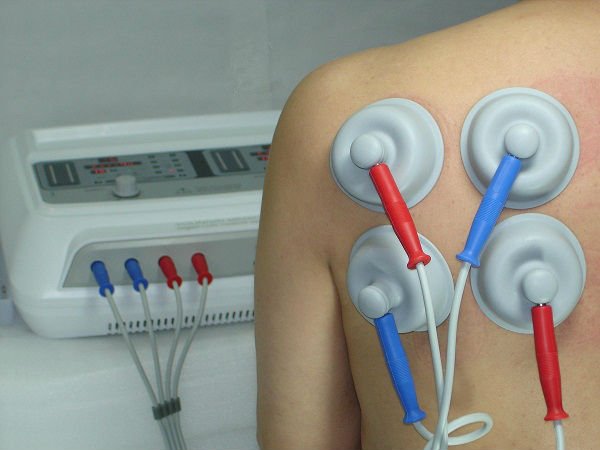
Проектирование и разработка прототипа электротерапевтического устройства
- Список журналов
- Open Biomed Eng J
- т.7; 2013
- PMC3856392
Open Biomed Eng J. 2013; 7: 100–108.
Опубликовано в сети 15 ноября 2013 г. doi: 10.2174/1874120701307010100
Информация об авторе Примечания к статье Информация об авторских правах и лицензии Отказ от ответственности . Система состоит из двух основных блоков: ведущего и ведомого. Блок Master, основным компонентом которого является ЦП, управляет пользовательским интерфейсом. Блок Slave, состоящий из микроконтроллера и генератора волн, вырабатывает соответствующие напряжения и токи, совместимые с желаемой обработкой. Вся система питается от источника питания 12 В, а напряжение выходного сигнала находится в диапазоне от -100 В до 100 В. Несмотря на то, что прототип может выполнять все электротерапевтические процедуры в диапазоне низких и средних частот, он был протестирован в эстетической мезотерапии. , а именно в антицеллюлитных, расположенных антицеллюлитных, антистрейчевых и антивялых. В этих обработках выходной сигнал состоит из перекрытия двух частот: первая выбрана в диапазоне 1,2 кГц — 1,8 кГц, а вторая — в диапазоне 0,07 Гц — 2 Гц. Система была протестирована в клинических условиях с реальными пациентами. Он показал хорошие результаты как по эффективности лечения, так и по уменьшению боли у пациентов.
Вся система питается от источника питания 12 В, а напряжение выходного сигнала находится в диапазоне от -100 В до 100 В. Несмотря на то, что прототип может выполнять все электротерапевтические процедуры в диапазоне низких и средних частот, он был протестирован в эстетической мезотерапии. , а именно в антицеллюлитных, расположенных антицеллюлитных, антистрейчевых и антивялых. В этих обработках выходной сигнал состоит из перекрытия двух частот: первая выбрана в диапазоне 1,2 кГц — 1,8 кГц, а вторая — в диапазоне 0,07 Гц — 2 Гц. Система была протестирована в клинических условиях с реальными пациентами. Он показал хорошие результаты как по эффективности лечения, так и по уменьшению боли у пациентов.
Ключевые слова: Электротерапия, Мезотерапия.
Электротерапия сейчас широко используется в медицине. Процесс безболезненный и очень эффективен при некоторых заболеваниях, поэтому имеет широкий спектр применения [1, 2]. Электростимуляция черепа (CES) — это неинвазивная процедура, которая десятилетиями использовалась для лечения тревоги, депрессии и бессонницы у населения в целом [3, 4]. Кроме того, было проведено исследований in vivo из для количественной оценки эффективности слабого постоянного электрического тока для лечения различных видов опухолей и некоторых видов рака [5, 6].
Кроме того, было проведено исследований in vivo из для количественной оценки эффективности слабого постоянного электрического тока для лечения различных видов опухолей и некоторых видов рака [5, 6].
Основным методом обезболивания является медикаментозное лечение. Еще один совершенно другой подход — применение электрических токов в диапазоне от мкА до мА к определенным областям головы. Хотя для большинства из нас это может показаться новой концепцией, годы исследований показывают, что транскраниальная стимуляция электротерапией (ТЭС) может неинвазивно увеличивать высвобождение эндогенных опиоидов из областей мозга, отвечающих за обезболивание [7-9].
В последнее время электротерапия используется для лечения мышечных болей, [8], мышечных спазмов [9], инфекции, артрит, выпадение волос, ревматические заболевания [10], контроль беспокойства, акне, потеря веса [11], лечение растяжек [12], лечение целлюлита и омоложение кожи [13, 14].
Протоколы или процедуры, которые может генерировать этот прототип стимулятора, охватывают как низкие, так и средние частоты спектра электротерапии [15].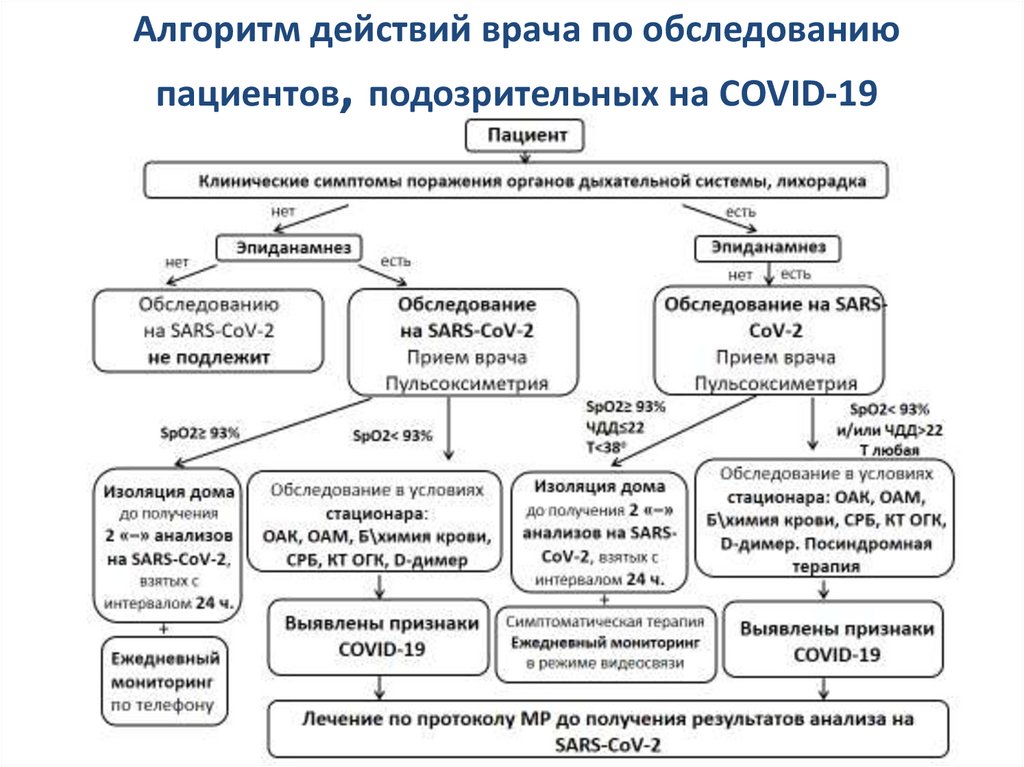 Основные группы доступных обработок показаны в Таблице . При правильной организации количество доступных процедур составляет 26; 12 из которых программируемые и 14 фиксированные. При программируемом лечении такие параметры, как ток, форма волны или частота, могут быть изменены оператором в широком диапазоне значений. Для фиксированных протоколов обычно необходим только текущий контроль. Методы лечения также различаются в зависимости от их электрических стимулов и физиологических эффектов, которые они вызывают. Такие эффекты могут быть чрезвычайно разнообразны для разных конфигураций того или иного протокола [10].
Основные группы доступных обработок показаны в Таблице . При правильной организации количество доступных процедур составляет 26; 12 из которых программируемые и 14 фиксированные. При программируемом лечении такие параметры, как ток, форма волны или частота, могут быть изменены оператором в широком диапазоне значений. Для фиксированных протоколов обычно необходим только текущий контроль. Методы лечения также различаются в зависимости от их электрических стимулов и физиологических эффектов, которые они вызывают. Такие эффекты могут быть чрезвычайно разнообразны для разных конфигураций того или иного протокола [10].
Table 1.
Electrotherapy protocols [12]
| Protocol | Fixed/Programmable |
|---|---|
| Traebert | Fixed |
| Diadynamic | Fixed |
| Iontophoresis | Fixed |
| Гальванический | Фиксированный |
| Экспоненциальный | Фиксированный |
| Интерференционный | Фиксированный |
| Russian | Programmable |
| Faradic | Programmable |
| Healing | Programmable |
| Muscle | Programmable |
| Tanifying | Programmable |
| TENS* | Programmable |
Открыть в отдельном окне
Примечание. Были объединены классические и недавно предложенные методы лечения. Это
всего можно получить 26 различных протоколов.
Были объединены классические и недавно предложенные методы лечения. Это
всего можно получить 26 различных протоколов.
* TENS: чрескожная электрическая стимуляция нервов
Этот проект финансировался компанией, основной целью которой была разработка прототипа аппаратного обеспечения, способного выполнять эстетическую мезотерапию, что позволило сократить технические знания, необходимые для проведения лечения. С другой стороны, поскольку прототип был разработан для проведения всех низко- и среднечастотных электротерапевтических процедур, можно расширить его функциональные возможности, просто обновив программное обеспечение. Таким образом, несмотря на то, что разработка этого прототипа нацелена на эстетическую медицину, он также может использоваться для других видов лечения, поскольку платформа принимает другие сигналы, изменяя лишь несколько параметров настройки.
Электронные устройства, применяемые в медицине, должны иметь точные показатели точности и надежности. Особенно те, которые находятся в непосредственном контакте с пациентом, что не оставляет права на ошибку. В прошлом все варианты, использованные при разработке этих устройств, в основном были связаны с выбором материалов и методов, которые использовались для максимального совершенства, качества, надежности и производительности. Для достижения наилучших результатов во время лечения оборудование должно гарантировать четкий и точный выходной сигнал с идеальным повторением и очень низким допуском ошибок (ниже 1%).
Особенно те, которые находятся в непосредственном контакте с пациентом, что не оставляет права на ошибку. В прошлом все варианты, использованные при разработке этих устройств, в основном были связаны с выбором материалов и методов, которые использовались для максимального совершенства, качества, надежности и производительности. Для достижения наилучших результатов во время лечения оборудование должно гарантировать четкий и точный выходной сигнал с идеальным повторением и очень низким допуском ошибок (ниже 1%).
Поскольку основной целью проекта была разработка прототипа для использования в эстетической мезотерапии, мы сосредоточим наше описание на этой области, несмотря на то, что прототип может выполнять другие процедуры электротерапии. В области эстетической медицины существуют различные виды лечения, которые можно рассматривать как ресурс мезотерапии, а именно:
Для каждого типа лечения требуется сигнал с одной полярностью, то есть выходной ток находится в диапазоне от нуля до максимального значения, выбирается оператором. Во всех вариантах применяемые сигналы подчинялись:
Во всех вариантах применяемые сигналы подчинялись:
V ( T ) = ( H F ( T ). L F ( T )) + L ( T )) + L 6 ( T )) + L 6 ( T )) + L 6 ( T )) + L 6 ( T )) + L 6 ( T )) + L 6 ( T )). (1)
, где V(t) — выходное напряжение, HF(t) — высокочастотная составляющая сигнала, значение которой находится в диапазоне от 1,2 кГц до 1,8 кГц, а LF(t) — нижняя частотный компонент сигнала, частота которого находится в диапазоне от 0,07 Гц до 2 Гц, то есть его период находится в диапазоне от 0,5 до 14 секунд. Обратите внимание, что V(t) всегда должен быть положительным. Если уравнение (1) дает отрицательное значение, для данного t выходной сигнал устанавливается равным нулю. На рис. () показано представление формы волны.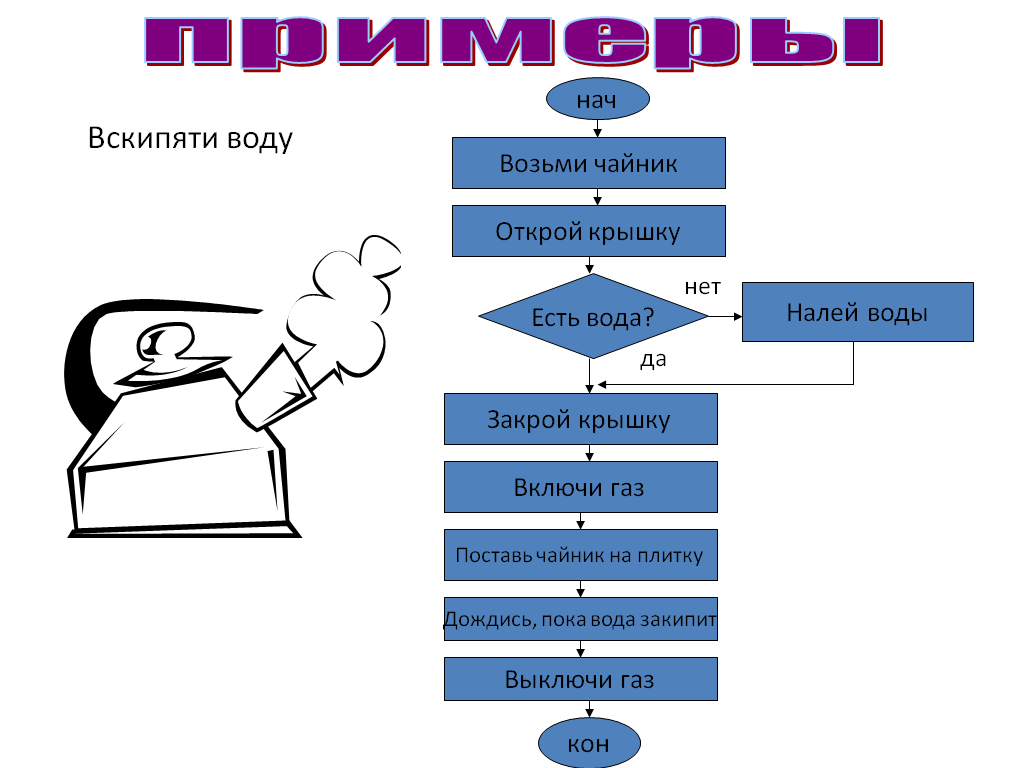
Открыть в отдельном окне
Желаемая форма выходного сигнала мезотерапии.
Наконец, следует учитывать тот факт, что некоторые лекарства работают только с отрицательными токами. В данном случае верно все, что было сказано в предыдущих абзацах, за исключением того, что для таких препаратов необходимо изменить нынешнее направление. Это делается путем изменения напряжения между минимальным отрицательным значением и нулем. Рис. ( ) показывает соответствующую форму сигнала.
Открыть в отдельном окне
Выходной сигнал мезотерапии с использованием препаратов отрицательной полярности.
Основной целью этого проекта является разработка прототипа устройства, способного проводить электротерапию на низкой и средней частоте, как указано выше. Для этого необходимо учитывать следующие характеристики:
-
Программируемый генератор сигналов должен иметь возможность генерировать сигналы с частотой до 10 кГц.
-
Из практических соображений напряжение питания системы не может превышать 12 В, а выходной сигнал может содержать пики, достигающие 100 В;
-
Установка должна иметь соответствующие меры безопасности, чтобы избежать травм пациента;
-
Пользовательский интерфейс должен быть удобным для использования техническим персоналом, не имеющим знаний в области электроники и вычислительной техники;
-
Установка должна быть достаточно гибкой, чтобы можно было вводить новые виды лечения без обновления оборудования;
-
Установка должна выполнять тесты самодиагностики и сообщать о любых аномалиях;
-
Установка должна работать 24 часа в сутки, 7 дней в неделю.
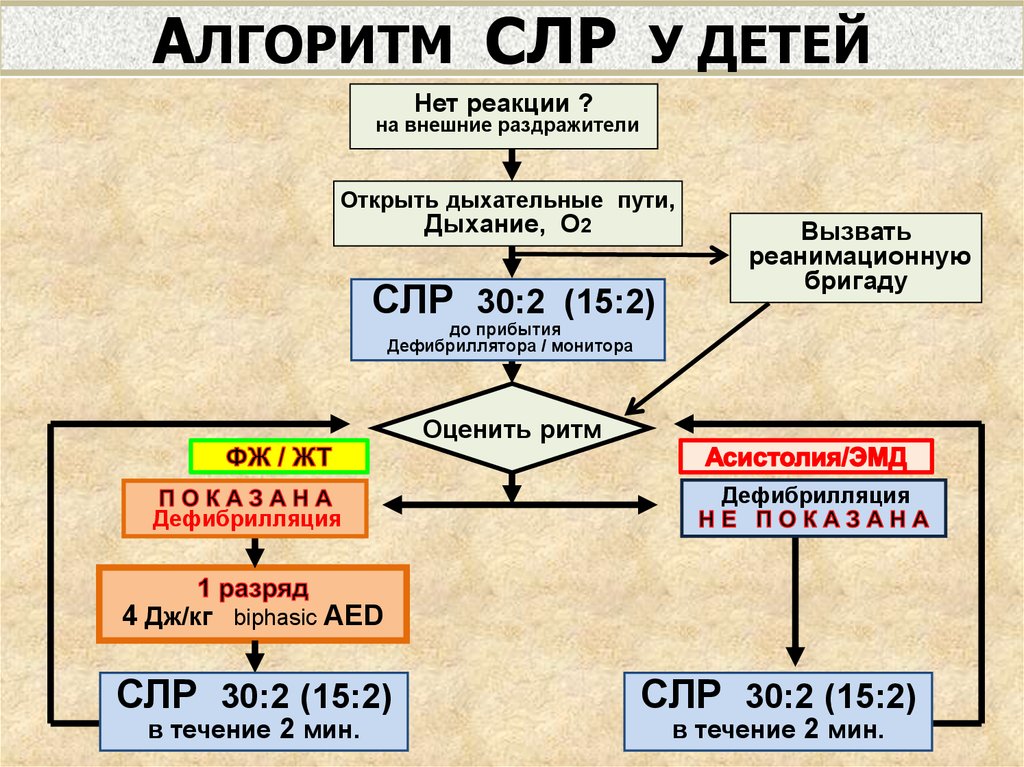
Общая архитектура системы, предлагаемая в этой статье, представляет собой структуру master-slave, так как есть два блока управления: высокоуровневый (master) и низкоуровневый (slave).
Блок управления верхнего уровня, центральный процессор (ЦП) или просто мастер отвечает за поддержку пользовательского интерфейса, обмен и обработку необходимой информации между пользователем и блоком управления нижнего уровня. Низкоуровневый блок управления или ведомый отвечает за преобразование цифровых данных, отправляемых высокоуровневым блоком управления, в аналоговые сигналы, которые непосредственно применяются к пациенту. Его основным компонентом является микроконтроллер. Блок управления нижнего уровня, запрограммированный на данные лечения, может работать самостоятельно. Тем не менее, может быть полезно поддерживать блок управления высокого уровня подключенным для отладки, контроля лечения и обнаружения ошибок или неисправностей. Рис. ( ) показывает архитектуру системы.
Открыть в отдельном окне
Архитектура системы. Центральный процессор работает как ведущий, а микроконтроллер — как ведомый. Функции микроконтроллера программируются ЦП, после чего микроконтроллер может работать самостоятельно.
Блок Master состоит из процессорного блока, сенсорного экрана и интерфейса Ethernet, а блок Slave состоит из микроконтроллера, драйвера, повышающего преобразователя постоянного тока, H-моста, фильтра и схема защиты пациента. И ведущий, и ведомый блоки взаимодействуют между собой посредством интерфейса USB. Рис. ( ) показывает блок-схему всей системы.
Открыть в отдельном окне
Блок-схема внутренней структуры устройства и связей между различными подсистемами.
ЦП является головной частью системы. Он отвечает за сбор всех данных, поступающих с консоли пользовательского интерфейса, их обработку и вычисление соответствующих векторов коэффициентов, которые будут использоваться микроконтроллером для создания соответствующего выходного сигнала.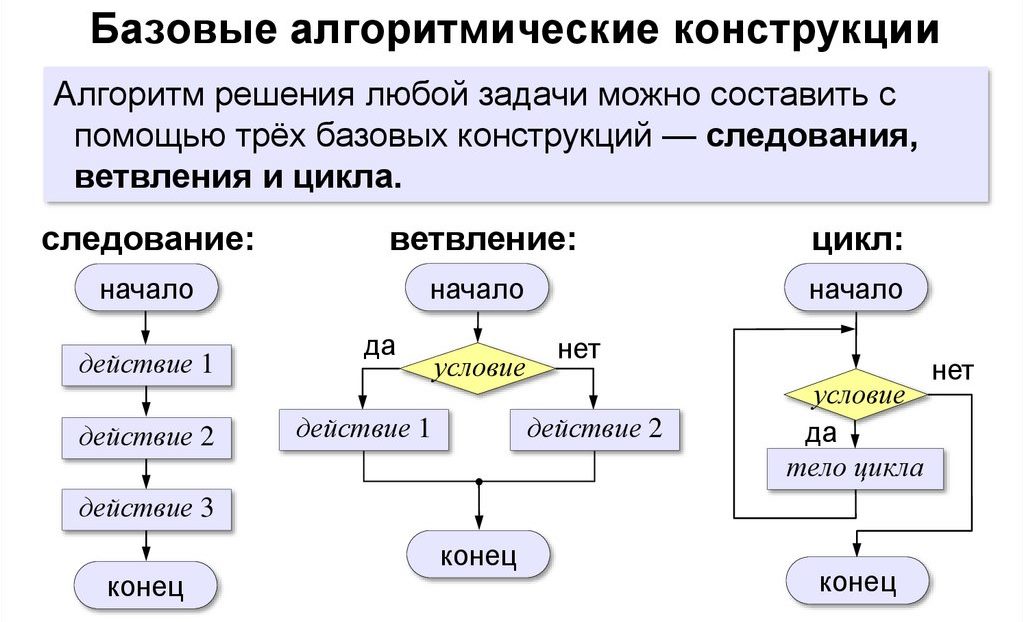
Если учесть, что технический персонал не имеет опыта работы с вычислительной техникой и электронными технологиями, важно обеспечить интуитивно понятный графический интерфейс. С этой целью для управления устройством использовался сенсорный монитор. В качестве языка программирования использовался C++, связанный с платформой Open GL, чтобы удовлетворить несколько требований, а именно работу в реальном времени, поддержку микроконтроллерных систем и достижение максимального графического потенциала системы. Программное обеспечение было разработано для набора конкретных процедур, при которых оператору не нужно изменять характеристики электрических сигналов, за исключением максимальной амплитуды, которая может меняться от пациента к пациенту. Тем не менее, он позволяет специалистам программировать новые сигналы. Важно отметить, что эта платформа основана на операционной системе Linux; из-за его большого потенциала для работы в реальном времени, связанного с тем преимуществом, что это бесплатное программное обеспечение, что упрощает и удешевляет коммерциализацию системы.
Еще одной особенностью системы является ее универсальность, которая позволяет обновлять прошивку и подключаться к другим устройствам через интерфейс Ethernet, что позволяет проводить широкий спектр процедур.
Интерфейс между ведущим и ведомым блоками достигается с помощью USB-подключения благодаря его широкой полосе пропускания и совместимости по принципу plug-and-play. Используется полнодуплексное низкоскоростное (1,5 Мбит/с) соединение, гарантирующее пропускную способность до 512 кбит/с в каждом направлении. Используемая топология шины представляет собой сокращенную топологию хоста, которая имеет уникальный USB-порт и не поддерживает полное дерево USB с концентратором. Это означает, что уменьшенный хост-контроллер предназначен для обработки уникального соединения «точка-точка» с уникальным USB-устройством.
Все соединения между ЦП и другими функциональными блоками являются двунаправленными, что обеспечивает непрерывную обратную связь, позволяющую мгновенно обнаруживать любую аномалию.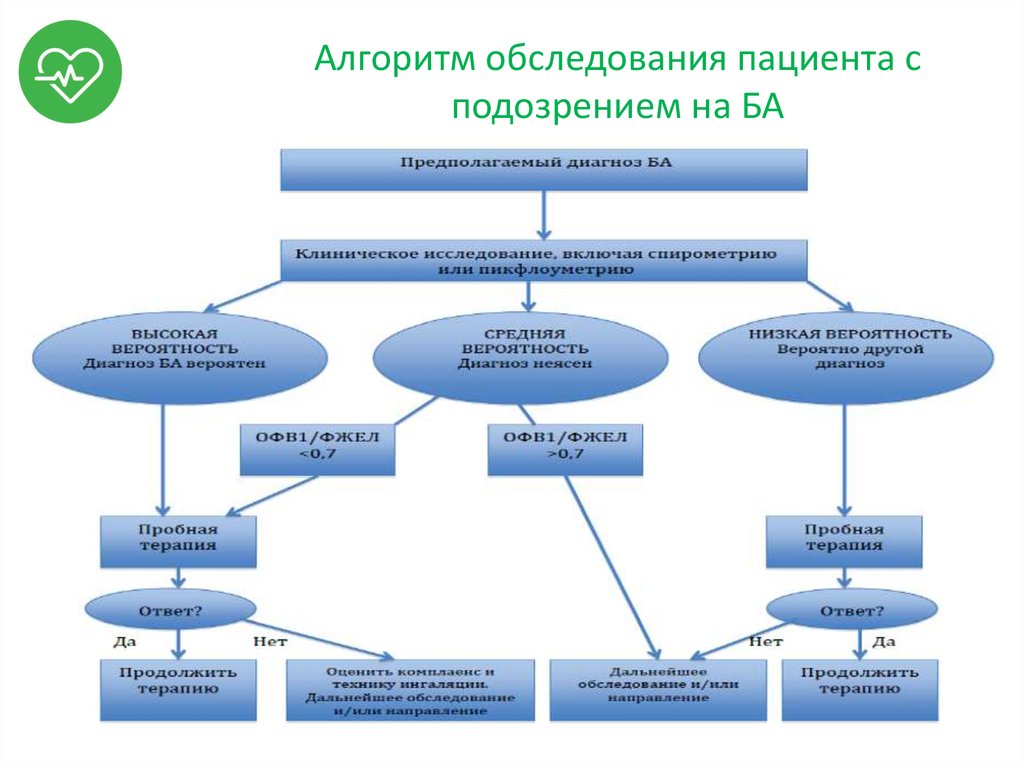
Главный блок блока управления нижнего уровня представляет собой микроконтроллер, который отвечает за сбор информации, отправляемой ЦП, для управления Н-мостом. Он вычисляет время включения/выключения ШИМ (широтно-импульсной модуляции), генерируя требуемый сигнал на выходе системы. Для формирования сигналов с частотой до 10 кГц частота дискретизации, используемая в микроконтроллере, примерно в 50 раз превышает частоту выходного сигнала, чтобы обеспечить низкую пульсацию на выходе фильтра. Для этого использовался кварц 8 МГц. Микроконтроллер был AT90USB1287, который представляет собой 8-битный CMOS-модуль с низким энергопотреблением, основанный на AVR с 64/128 КБ ISP Flash, контроллер USB-устройства с поддержкой полной и низкой скорости передачи данных и усовершенствованной архитектурой RISC. Выполняя мощные инструкции за один такт, AT90USB1287 достигает пропускной способности, приближающейся к 1 MIPS на МГц, что позволяет разработчику системы оптимизировать энергопотребление в зависимости от скорости обработки.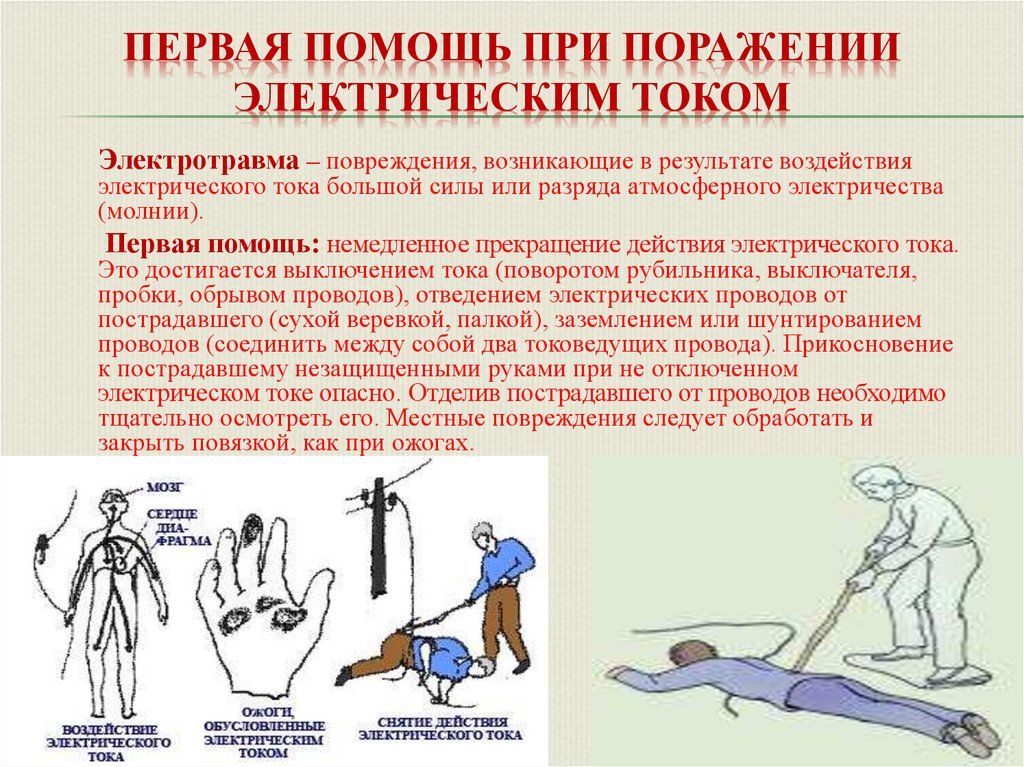
Выходной сигнал микроконтроллера создает пиковое напряжение 3,3 В. Для проведения эффективного лечения необходимо усилить этот сигнал до более высоких уровней, которые могут достигать 100 В, в зависимости от лечения. Для выполнения этой задачи был реализован H-мост с двумя квадрантами, позволяющий изменять полярность выходного сигнала в соответствии с соответствующей обработкой. H-мост был реализован с помощью чипа STMicroelectronics L6225, который представляет собой устройство двойного полного моста DMOS, которое сочетает в себе изолированные силовые DMOS-транзисторы с CMOS и биполярными схемами на одном чипе. Рис. ( ) показана принципиальная схема драйвера и Н-моста.
Открыть в отдельном окне
Схема драйвера и схема Н-моста. Они основаны на технологии BCD. Сочетает изолированные силовые DMOS-транзисторы с CMOS и биполярными схемами на одном кристалле.
Стандартные требования, предъявляемые к медицинскому оборудованию, не позволяют системам питания, отвечающим за формирование лечебных сигналов, иметь входное напряжение выше 12 В. Тем не менее, для получения ожидаемых результатов выходной сигнал должен иметь пики до 100 В. Это достигается с помощью схемы повышающего преобразователя постоянного тока в постоянный, который обеспечивает до 100 В с малыми пульсациями и 500 мА максимального выходного тока. В этом приложении ток не будет превышать 50 мА. Схема повышающего преобразователя постоянного тока реализована на устройстве Linear Technology LT1680. Принципиальная схема преобразователя представлена на рис. ( ).
Тем не менее, для получения ожидаемых результатов выходной сигнал должен иметь пики до 100 В. Это достигается с помощью схемы повышающего преобразователя постоянного тока в постоянный, который обеспечивает до 100 В с малыми пульсациями и 500 мА максимального выходного тока. В этом приложении ток не будет превышать 50 мА. Схема повышающего преобразователя постоянного тока реализована на устройстве Linear Technology LT1680. Принципиальная схема преобразователя представлена на рис. ( ).
Открыть в отдельном окне
Повышающая схема. Мощный импульсный контроллер источника питания с режимом тока, оптимизированный для форсированных топологий. ИС управляет N-канальным МОП-транзистором, который переключает ток в катушке индуктивности.
Блок фильтра на рис. ( ) отвечает за уменьшение пульсаций, генерируемых ШИМ, до допустимых уровней. Это LC-фильтр нижних частот второго порядка с частотой среза 10 кГц. На рис. ( ) показана принципиальная схема фильтра.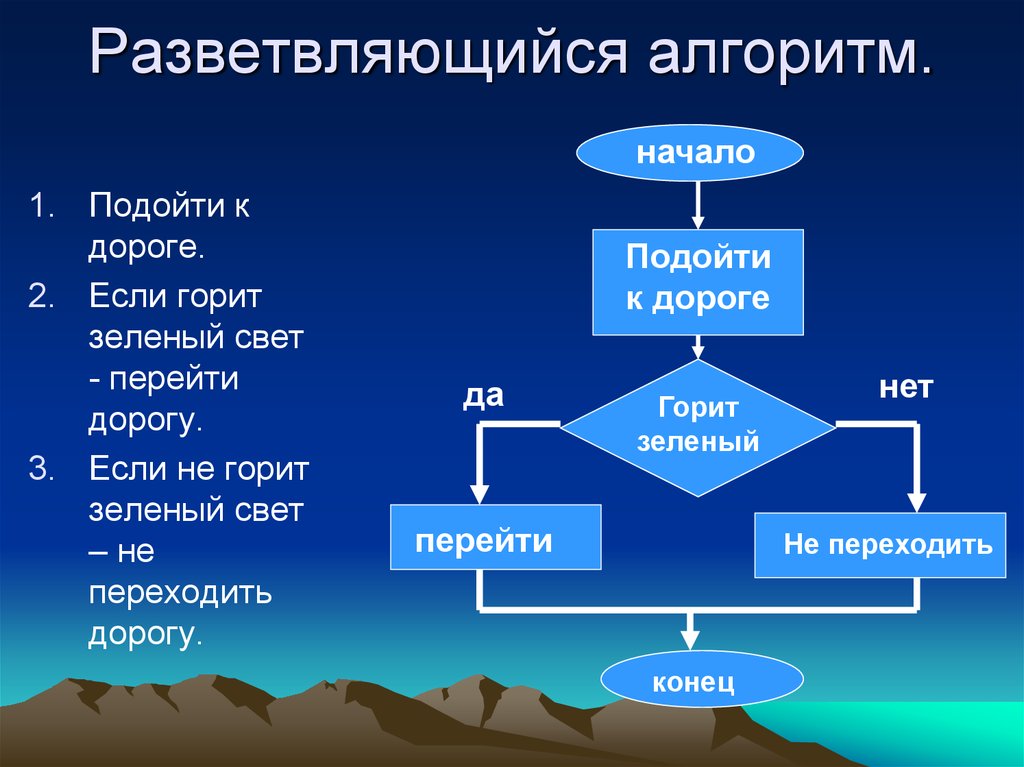 Его передаточная функция определяется выражением:
Его передаточная функция определяется выражением:
Открыть в отдельном окне
ФНЧ второго порядка с частотой среза 10 кГц.
H(jf)=11−(ffo)2+(jQ)(ffo)
(2)
где fo=1/(2πL C), Q=L C/(R C) R это сопротивление катушки. Частоту среза 10 кГц можно получить, сделав L = 2,5 мГн и C = 100 нФ.
Все оборудование должно соответствовать правилам безопасности, установленным ответственными лицами. Поэтому помимо основной задачи, то есть электротерапевтического оборудования, мы должны также обеспечить безопасность пациента. При этом на сигнальный выход был введен ограничитель тока. Когда ток достигает значений выше 30 мА, выходное напряжение схемы снижается. Рис. ( ) показывает форму волны выходного напряжения в зависимости от тока. Это ограничение тока реализовано микроконтроллером через цепь обратной связи, то есть выходное напряжение подается обратно в микроконтроллер с помощью АЦП (аналогово-цифрового преобразователя).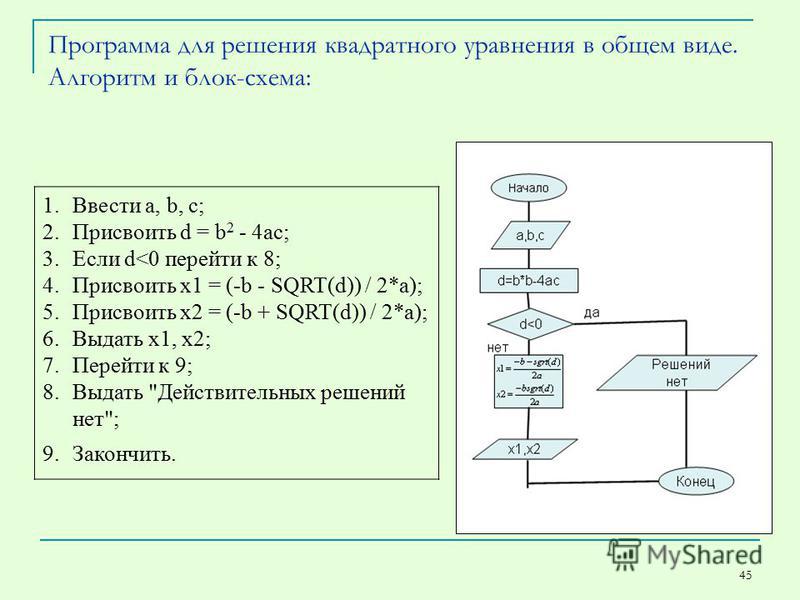 Этот контур обратной связи также позволяет контролировать выходное напряжение, проверять ошибки и обнаруживать неисправности.
Этот контур обратной связи также позволяет контролировать выходное напряжение, проверять ошибки и обнаруживать неисправности.
Открыть в отдельном окне
Зависимость выходного напряжения от тока. При токах выше 30 мА защита системы срабатывает снижением выходного напряжения. Vp – запрограммированное выходное напряжение.
На рис. ( ) показана блок-схема основного программного алгоритма. Основная операция начинается с ожидания инструкций пользователя. После этого он обрабатывает инструкции пользователя и отправляет соответствующие команды ведомому. Затем программа входит в цикл, управляемый таймером. Внутри этого цикла мастер не замечает только действия ведомого. Когда время обработки достигнуто или в состоянии ошибки, программа выходит из цикла, она отправляет команду на отключение ведомому устройству и ожидает новых инструкций пользователя.
Открыть в отдельном окне
Блок-схема мастер-алгоритма.
На рис. ( ) показана блок-схема алгоритма ведомого программного обеспечения. Он состоит из четырех независимых подпрограмм, каждая из которых активируется состоянием прерывания.
Он состоит из четырех независимых подпрограмм, каждая из которых активируется состоянием прерывания.
Открыть в отдельном окне
Блок-схема ведомого алгоритма.
Первая подпрограмма активируется, когда данные доступны на USB-порту. В этом случае микроконтроллер считывает данные, обрабатывает их и генерирует соответствующее условие прерывания, чтобы активировать одну из трех других подпрограмм. Подходящими условиями прерывания являются: обработка обработки, состояние обработки и окончание обработки.
Вторая подпрограмма активируется прерыванием обработки лечения. Он начинается с инициализации таймера. Затем он входит в цикл, управляемый тем же таймером. Внутри контура выходное напряжение обновляется путем перепрограммирования ШИМ-контроллера.
Третья подпрограмма активируется прерыванием состояния лечения. Это прерывание активируется двумя событиями: мастером, запрашивающим обратную связь; и в управляемом таймером событии, которое реализует описанную выше петлю обратной связи защиты. Когда эта подпрограмма активирована, она только считывает значение выходного напряжения и отправляет его мастеру.
Когда эта подпрограмма активирована, она только считывает значение выходного напряжения и отправляет его мастеру.
Четвертая подпрограмма активируется прерыванием окончания лечения. Когда это прерывание активировано, микроконтроллер отключает все устройства питания и сбрасывает все внутренние переменные.
На рис. ( ) показаны два изображения прототипа.
Открыть в отдельном окне
Внутренние схемы и внешний вид прототипа.
Выходной сигнал представляет собой сумму двух составляющих: низкой частоты 0,07 Гц (Период = 14 с) и высокой частоты 1,8 кГц. Фильтр устраняет высокочастотные составляющие, создаваемые ШИМ-модулятором, и все колебания сигнала сглаживаются. Рис. ( ) показана форма выходного сигнала системы, а на рис. () показана деталь формы сигнала на рис. () только для 5 периодов волны ШИМ, то есть для 10 мкс. На этом рисунке видно, что пульсация имеет амплитуду 11 мВ и не влияет на лечение.
Открыть в отдельном окне
Сигнал получен на выходе системы. Это соответствует сигналу на рис. (11), отфильтрованному с помощью фильтра нижних частот, с 2 с по оси времени и 5 В по оси напряжения.
Это соответствует сигналу на рис. (11), отфильтрованному с помощью фильтра нижних частот, с 2 с по оси времени и 5 В по оси напряжения.
Рис. ( ) показан выходной сигнал антицеллюлитной программы при 40% полной мощности.
Открыть в отдельном окне
Выходной сигнал антицеллюлитной программы на 40% полной мощности.
Другим аспектом, который был проверен на реальных пациентах, является риск ожога кожи. Испытания показали, что больший риск возникает в электроде, выполняющем роль анода. Тем не менее, риск значительно снижается, если применять некоторые из следующих правил:
-
Электроды должны быть очень аккуратно наложены на кожу, чтобы избежать горячих точек,
-
Электроды необходимо часто и глубоко увлажнять для повышения электро- и теплопроводности,
-
Постоянный ток необходимо включать с медленным увеличением интенсивности.
При соблюдении этих правил пациенты чувствуют очень слабое покалывание или совсем его не ощущают.
Прототип был испытан в клинических условиях с реальными пациентами. Результаты этих тестов являются субъективными и состоят из мнений техников и пациентов. На вопрос об эффективности лечения их ответы в основном были «хорошо» и «очень хорошо». На вопрос о наполняющей боли ответы были «нет боли» и «немного покалывает».
В этой статье описывается полный прототип системы для использования в низко- и среднечастотной электротерапии. Система состоит из архитектуры ведущий-ведомый, в которой главный блок основан на ЦП, а подчиненный блок основан на микроконтроллере. Первый прототип системы, предназначенный для эстетической мезотерапии, уже изготовлен и испытан в лабораторных условиях с характеристиками, соответствующими ожидаемым. Он также был испытан в клинических условиях с реальными пациентами. Результаты этих испытаний более или менее субъективны, поскольку они состоят из мнений техников и пациентов, но почти каждый считал работу прототипа хорошей или очень хорошей.
Подтверждение финансирования
Любые конфликты интересов.
1. Ya T, Runjing Z, Guanying Z. Проектирование электротерапевтического генератора сигналов на основе DSP Builder. В материалах 5-й Международной конференции по информационным технологиям и их применению в биомедицине совместно со 2-м Международным симпозиумом и летней школой по биомедицине и инженерии здравоохранения в Шэньчжэне. Китай. 2008: 603–606. [Google Scholar]
2. Быстрицкий А., Кервин Л., Фойснер Дж. Пилотное исследование черепной электростимуляции при генерализованной тревоге. Дж. Клин. психиатрия. 2008;69: 412–417. [PubMed] [Google Scholar]
3. Gilula MF, Kirsch DL. Обзор стимуляции краниальной электротерапии. Более безопасная альтернатива психофармацевтическим препаратам при лечении депрессии. Дж. Нейротер. 2005; 9: 7–26. [Google Scholar]
4. Ciria HC, Quevedo MS, Cabrales LB, Bruzón RP, Salas MF, Pena OG, Gonzalez TR, López DS, MFlores J. Противоопухолевая эффективность различного количества электрического заряда при Эрлихе и фибросаркоме Sa-37 опухоли. БМК Рак. 2004; 4:87. [Бесплатная статья PMC] [PubMed] [Google Scholar]
БМК Рак. 2004; 4:87. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Час Г. Д., Лайт М. Возможное использование низкоуровневой электротерапии постоянным током для лечения рака. Proc IEEE Eng. Мед. био. Соц. 1993:1515– 516. [Google Scholar]
6. Кацнельсон Ю., Лапшин В., Клод Дж., Барту Г. Транскраниальный электротерапевтический стимулятор для временного уменьшения боли. В Proc 25th Ann. Междунар. конф. IEEE EMBS. . 2003: 2285–2288. [Google Scholar]
7. Уайт П.Ф., Ли С., Чиу Дж.В. Электроанальгезия: ее роль в лечении острой и хронической боли. Анест. аналг. 2001;92: 505–513. [PubMed] [Google Scholar]
8. Джонсон М.И., Табасам Г. Исследование обезболивающего действия интерференционных токов и чрескожной электрической стимуляции нервов на экспериментально индуцированную ишемическую боль у добровольцев, не испытывающих боли. физ. тер. 2003;83 [PubMed] [Google Scholar]
9. Уорд А.Р., Шкуратова Н. Российская электростимуляция. физ. тер. . 2002;82 [PubMed] [Google Scholar]
10. Sequeira G, Macieira C, Ramos F, Saraiva F, Romeu JC, deQueiroz M V. Пилотное исследование эффективности, переносимости и безопасности мезотерапии при абартикулярных ревматических заболеваниях. rg o oficial da sociedade portuguesa de reumatologia. АКТА РЕУМ ПОРТ. . 2005;30:341–7. [Академия Google]
Sequeira G, Macieira C, Ramos F, Saraiva F, Romeu JC, deQueiroz M V. Пилотное исследование эффективности, переносимости и безопасности мезотерапии при абартикулярных ревматических заболеваниях. rg o oficial da sociedade portuguesa de reumatologia. АКТА РЕУМ ПОРТ. . 2005;30:341–7. [Академия Google]
11. Мадхере С., редактор. Великобритания, 15 июня: Taylor & Francis Ltd; 2006. Эстетическая мезотерапия и инъекционный липолиз в клинической практике. [Google Scholar]
12. Мондо ПКС, Росас РФ. Эффекты гальванического тока при лечении атрофических растяжек. Fisioterapia da Universidade do Sul de Santa Catarina-UNISUL. 2000 [Google Scholar]
13. Тости А., ДеПадова М.П. Атлас мезотерапии в омоложении кожи. Информа Здравоохранение Соединенное Королевство. Сентябрь. 2007 [Google Академия]
14. Амитрано С., Каппеллетти Р., Торре Р. Новые тенденции в мезопорации систем доставки лекарств — новый метод. Являюсь. J. Отчет доктора мезотерапии. 2007 [Google Scholar]
15. Мартин Дж. М. Р., редактор. 2-е изд. (на испанском языке) .: Editorial Medica Panamericana .; 2004. Электротерапия в физиотерапии. [Google Scholar]
Мартин Дж. М. Р., редактор. 2-е изд. (на испанском языке) .: Editorial Medica Panamericana .; 2004. Электротерапия в физиотерапии. [Google Scholar]
Статьи из The Open Biomedical Engineering Journal предоставлены здесь Bentham Science Publishers
Электротерапия: Значение удара | Nature
Глубокая стимуляция мозга — проверенный метод лечения болезни Паркинсона. Осталось выяснить, как это работает.
Прежде чем ваш врач начнет втыкать электроды в ваш мозг, было бы разумно надеяться, что он или она точно знает, что произойдет и почему. Но когда дело доходит до глубокой стимуляции мозга (DBS) при болезни Паркинсона, единственное, с чем могут согласиться эксперты, это то, что она работает.
Цветной рентгеновский снимок, показывающий электроды, имплантированные для глубокой стимуляции мозга. Кредит: Соверен, ISM/SPL
В DBS электроды толщиной в миллиметр имплантируются в мозг и нацелены на цель, меньшую, чем зерно кукурузы, местоположение которой было тщательно нанесено на карту на основе данных визуализации. Электроды доставляют к субталамическому ядру слабый поток электрических импульсов, которые могут контролировать изнурительные двигательные симптомы, которые испытывают пациенты.
Электроды доставляют к субталамическому ядру слабый поток электрических импульсов, которые могут контролировать изнурительные двигательные симптомы, которые испытывают пациенты.
За последние несколько десятилетий медицинское сообщество приняло этот метод лечения. «Эта процедура очень безопасна и эффективна, — говорит Андрес Лосано, нейрохирург из Университета Торонто в Канаде. По его оценкам, около 10 000 человек во всем мире ежегодно проходят операцию DBS по поводу болезни Паркинсона, и на сегодняшний день более 140 000 человек получают имплантаты. Тем не менее, мало что известно о том, как DBS восстанавливает нормальную функцию двигательной схемы мозга.
Однако прогресс налицо, и любой прогресс в понимании болезни может принести большие дивиденды в лечении конкретного пациента. «Сейчас мы просто взрываем мозг непрерывной стимуляцией, и удивительно, что такое грубое вмешательство так сильно помогает», — говорит Джилл Острем, невролог из Калифорнийского университета в Сан-Франциско (UCSF). «Представьте, что мы могли бы сделать, если бы подошли к этому более изощренно и индивидуально».
«Представьте, что мы могли бы сделать, если бы подошли к этому более изощренно и индивидуально».
Автоматический выключатель
Часть Nature Outlook: болезнь Паркинсона
Возможно, самым большим препятствием является сохраняющаяся неуверенность в том, как болезнь Паркинсона вызывает нарушение работы мозговых цепей. Большинство исследований в области нейрофизиологии болезни сосредоточено на «двигательной цепи» мозга, состоящей из базальных ганглиев, таламуса и части коры, которая управляет движением. По мере прогрессирования болезни Паркинсона нейроны базальных ганглиев, вырабатывающие нейротрансмиттер дофамин, умирают, нарушая работу двигательной цепи. «Дофамин играет главную роль в установлении правил нейронной активности», — говорит Лозано. «В отсутствие этого влияния нейроны начинают вести себя неправильно и запускать паттерн, который является патологическим».
Сначала исследователи, ищущие объяснение неправильного поведения нейронов, отдавали предпочтение тому, что было известно как «модель скорости», которая была разработана в 1980-х годах. Невролог Махлон Делонг из Университета Эмори в Атланте, штат Джорджия, предположил, что симптомы паркинсонизма возникают из-за более высокой скорости передачи сигналов в области базальных ганглиев, известной как субталамическое ядро. ДеЛонг полагал, что это усиленное возбуждение нейронов подавляет другие области двигательной цепи, и сообщил, что хирургическое разрушение субталамического ядра облегчает двигательные симптомы паркинсонизма у обезьян 1 . В 1990-х годах Алим-Луи Бенабид и его коллеги, работавшие тогда в Университетской больнице Гренобля во Франции, использовали результаты Делонга в качестве основы для разработки DBS для лечения болезни Паркинсона. Группа Бенабида продемонстрировала, что высокочастотная электрическая стимуляция, проводимая электродами, расположенными рядом с субталамическим ядром, облегчала двигательные симптомы, такие как ригидность 2 .
Электроды нацелены на крошечные ядра субталамуса (белые стрелки) для глубокой стимуляции мозга. Предоставлено: Людвик Зринцо
Хотя основы того, как DBS дается людям с болезнью Паркинсона, с тех пор мало изменились, модель оценки в значительной степени отошла на второй план. Вместо этого кажется, что симптомы возникают из-за изменения нормальных паттернов возбуждения в двигательной цепи, а не из-за чрезмерного возбуждения в одной точке. Сейчас концепция состоит в том, что цепь чрезмерно синхронизирована, говорит Филип Старр, нейрохирург из Калифорнийского университета в Сан-Франциско. «Отдельные клетки моторной коры и базальных ганглиев, которые обычно имеют тенденцию к независимой активации, теперь активируются вместе», — объясняет Старр. В частности, исследователи болезни Паркинсона выявили высокие уровни колебаний β-диапазона — активности мозговых волн, возникающей на частоте около 15–30 герц — в базальных ганглиях. Такие частоты также встречаются в здоровом мозгу, но становятся преувеличенными при болезни Паркинсона и, по-видимому, связаны с задержкой или нарушением сознательного движения.
В норме дофамин-продуцирующие нейроны в базальных ганглиях препятствуют установлению таких синхронизированных ритмов; в этой «модели паттерна» потеря этих нейронов снимает эту защиту. Но исследователям до сих пор неясно, как возникает разрушительная β-активность. Одна из возможностей состоит в том, что активность распространяется из других связанных областей мозга. Невролог Хелен Бронте-Стюарт из Стэнфордского университета в Калифорнии говорит, что β-активность, которая регулярно возникает в моторной коре, может передаваться по длинным аксонам, которые тянутся от нейронов в этой области к базальным ганглиям. Также неясно, как β-ритм мешает произвольному движению. Группа Старра исследует явление, известное как связь фазы и амплитуды, которое может сыграть важную роль в этом процессе. Согласно этой модели, паркинсоническая моторная кора вынуждена идти в ногу с β-ритмами, которые исходят из базальных ганглиев, а не независимо активироваться, чтобы обеспечить нормальные физические движения.
Пошуметь
На этом фоне нейробиологи не понимают, почему DBS работает так хорошо. Когда преобладала модель скорости, исследователи думали, что DBS напрямую подавляет чрезмерную активность, которую наблюдали Делонг, Бенабид и их коллеги. Но с тех пор исследователи показали, что электрическая стимуляция возбуждает, а не подавляет нейроны в базальных ганглиях, отсылая нейробиологов обратно к чертежной доске. «У нас была ситуация, когда субталамическая стимуляция была основной терапией, которая проводилась во всем мире в течение десяти лет с большим количеством подтверждающих доказательств, но мы больше не знали, как она работает», — говорит Старр.
Мы принимаем это патологическое поведение и подавляем его.
Большинство современных теорий моделей паттернов восходят к идее о том, что DBS разрушает нездоровые ритмы в двигательных цепях, вводя нерегулярные паттерны активности нейронов в базальные ганглии. «Мы берем это патологическое поведение и подавляем его», — говорит Лозано. «Кажется, вам лучше без результатов, чем с результатами, которые вызывают проблемы». Но исследователи все еще пытаются понять, как происходит эта потеря синхронизации, и эта модель еще не общепринята.
«Мы берем это патологическое поведение и подавляем его», — говорит Лозано. «Кажется, вам лучше без результатов, чем с результатами, которые вызывают проблемы». Но исследователи все еще пытаются понять, как происходит эта потеря синхронизации, и эта модель еще не общепринята.
Каким бы ни был механизм, общее мнение состоит в том, что активность DBS, разрушающая β-диапазоны, возникает из-за стимуляции клеток субталамического ядра базальных ганглиев. Но у нейробиолога Гордона Арбатнота из Окинавского института науки и технологий в Японии и его коллег есть альтернативная теория. Они утверждают, что стимуляция возбуждает длинные аксоны, соединяющие нейроны моторной коры с нейронами субталамического ядра, и что эффект передается «назад» по этим проводам в моторную кору, а не «вперед» в базальные ганглии. Гипотеза состоит в том, что DBS нарушает нездоровые паттерны активности в моторной коре, а эта область, в свою очередь, останавливает аномальную синхронизацию β-активности, наблюдаемую в базальных ганглиях 3,4 .
«Кажется, существует связь между двигательной активностью коры, потерей β-ритма и восстановлением», — говорит Арбатнотт. Это благоприятствовало бы модели, в которой болезнь Паркинсона управляется моторной корой, а не базальными ганглиями. Но исследования все еще находятся на ранней стадии — подтверждающие данные в основном получены на животных моделях. Попытки облегчить симптомы болезни Паркинсона у людей с помощью прямой электрической стимуляции моторной коры, а не базальных ганглиев, оказались безуспешными.
Лечение с потенциалом
Если оставить в стороне неразгаданные загадки механизма, DBS работает — и исследователи в настоящее время адаптируют его доставку к отдельным людям за счет сочетания клинического опыта и технического прогресса.
Один из горячих вопросов касается того, когда в течение болезни DBS может принести наибольшую пользу. Большинство людей получают имплантат после того, как они прожили с болезнью Паркинсона, управляемой с помощью медицинских препаратов, более десяти лет, когда прогрессирование заболевания сделало их симптомы более трудными для контроля. Клиническое исследование EARLYSTIM, проведенное в 2013 году, показало, что вмешательство на несколько лет раньше может быть полезным 9.0130 5 . В следующем году пилотное исследование под руководством исследователей из Университета Вандербильта в Нэшвилле, штат Теннесси, пошло еще дальше: они давали DBS людям, которые принимали лекарства всего шесть месяцев 6 . Оба исследования вызвали негативную реакцию отчасти из-за рисков, связанных с нейрохирургией, а также из-за опасений, что таким пациентам могли поставить неправильный диагноз и вместо этого иметь другое двигательное расстройство, не связанное с болезнью Паркинсона.
Клиническое исследование EARLYSTIM, проведенное в 2013 году, показало, что вмешательство на несколько лет раньше может быть полезным 9.0130 5 . В следующем году пилотное исследование под руководством исследователей из Университета Вандербильта в Нэшвилле, штат Теннесси, пошло еще дальше: они давали DBS людям, которые принимали лекарства всего шесть месяцев 6 . Оба исследования вызвали негативную реакцию отчасти из-за рисков, связанных с нейрохирургией, а также из-за опасений, что таким пациентам могли поставить неправильный диагноз и вместо этого иметь другое двигательное расстройство, не связанное с болезнью Паркинсона.
После DBS многие люди прекращают прием лекарств и получают очень хороший и стабильный ответ.
Однако некоторые клиницисты считают возможным выявить тех, кому раннее вмешательство принесет наибольшую пользу. «Обычно это пациенты с ранним началом болезни Паркинсона с преобладанием тремора», — говорит Бронте-Стюарт. По ее словам, после DBS «многие из них бросили принимать лекарства и имеют очень хороший и стабильный ответ, а некоторым из них посчастливилось никогда не развить когнитивные нарушения».
По ее словам, после DBS «многие из них бросили принимать лекарства и имеют очень хороший и стабильный ответ, а некоторым из них посчастливилось никогда не развить когнитивные нарушения».
На данный момент DBS является предложением по принципу «все или ничего». Он представляет собой непрерывную дозу электростимуляции с фиксированной частотой, которую может настроить только специалист. Более гибкие подходы, предназначенные для точной настройки времени, частоты и пространственного распределения тока, могут как повысить эффективность, так и уменьшить недостатки DBS.
Питер Браун, невролог из Оксфордского университета, Великобритания, исследует шаблонную стимуляцию. Он утверждает, что изменение времени электрических импульсов может радикально изменить эффект DBS на дисфункциональные ритмы двигательных цепей: «Вы можете помешать им, правильно рассчитывая время стимуляции, или вы можете ухудшить их, рассчитывая время неправильно».
Питер Тасс и его коллеги из Юлихского исследовательского центра в Германии разрабатывают версию этого подхода, называемую скоординированной перезагрузкой, которая последовательно обеспечивает стимуляцию отдельных субпопуляций субталамических нейронов. Этот подход показал себя многообещающим, и Браун впечатлен. «Вы можете лечиться в течение нескольких сеансов, и это может быть длительное, устойчивое улучшение в течение нескольких недель», — говорит он.
Этот подход показал себя многообещающим, и Браун впечатлен. «Вы можете лечиться в течение нескольких сеансов, и это может быть длительное, устойчивое улучшение в течение нескольких недель», — говорит он.
Существуют побочные эффекты DBS, такие как нарушение речи, непроизвольные движения и когнитивные нарушения, которые могут стать особенно проблематичными при непрерывной стимуляции. Браун сравнивает это с «постоянным обогревом комнаты в вашем доме, летом или зимой». Его команда входит в число тех, кто разрабатывает адаптивную DBS, в которой стимуляция изменяется в ответ на физиологические сигналы — по сути, установка термостата для мозга (см. «Термостат для глубокого мозга»). Самое сложное — выбрать правильный триггер. Команда Брауна сосредоточилась на чрезмерной активности β-диапазона в базальных ганглиях и показала, что адаптивный подход обеспечивает облегчение симптомов, эквивалентное обычному DBS, при одновременном снижении побочных эффектов 7 . Адаптивные системы также потребляют меньше энергии — важное преимущество, учитывая, что стандартные батареи для современных DBS служат всего 3–4 года и требуют хирургической процедуры для замены.
Предоставлено Питером Брауном
Тем временем команда Старра определила сигнатуры в активности нейронов моторной коры, которые предсказывают появление симптомов паркинсонизма, и разработала алгоритм, который инициирует стимуляцию при обнаружении этих паттернов 8 . А команда Бронте-Стюарт разработала адаптивную платформу DBS, которая использует умные часы с поддержкой Bluetooth для обнаружения начала тремора, а затем сигнализирует стимулятору о соответствующей реакции 9 .
Эти адаптивные подходы также могут помочь раскрыть некоторые тайны паркинсонического мозга. Ostrem, например, работал с новой системой DBS от Medtronic под названием Activa PC+S, которая позволяет гибко отслеживать активность мозга до, во время и после появления симптомов. Острем отмечает, что такие технологии в сочетании с накоплением данных визуализации мозга с высоким разрешением и усилиями по моделированию могут позволить разработать схемы лечения, нацеленные на определенные неврологические нарушения.

