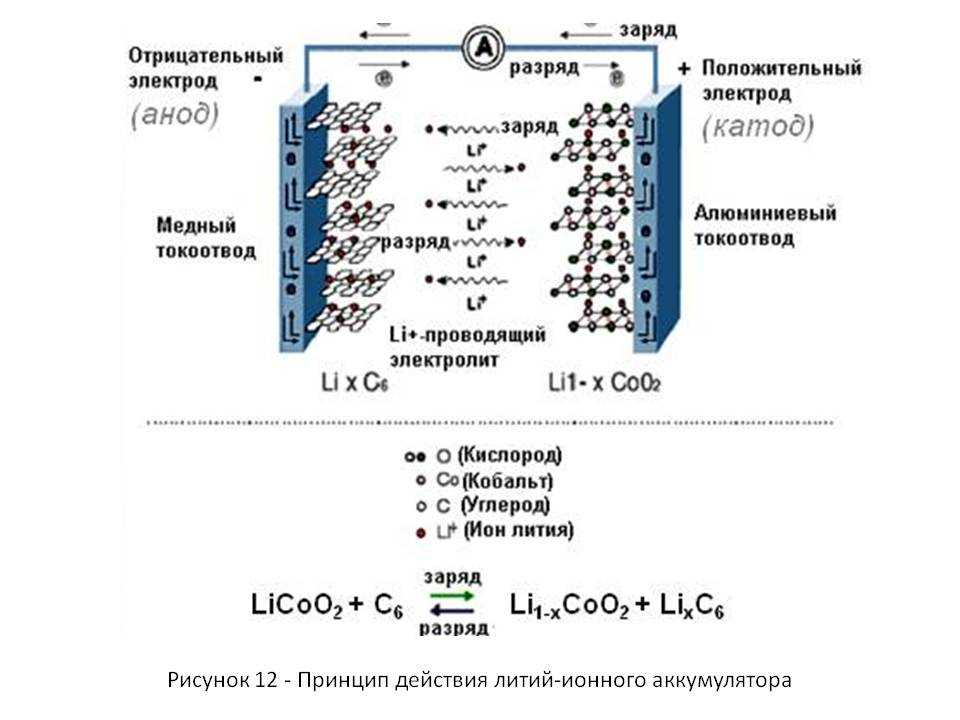
Как устроены литий-ионные аккумуляторы. Каковы основные компоненты Li-ion батарей. Какие химические процессы происходят при заряде и разряде. Почему литий-ионные аккумуляторы получили широкое распространение. Каковы преимущества и недостатки Li-ion технологии.
Устройство литий-ионного аккумулятора
Литий-ионный аккумулятор состоит из следующих основных компонентов:
- Катод (положительный электрод) — обычно это оксид лития, нанесенный на алюминиевую фольгу
- Анод (отрицательный электрод) — как правило, графит, нанесенный на медную фольгу
- Электролит — проводящая среда между электродами, обычно жидкий органический растворитель с солями лития
- Сепаратор — пористая мембрана, разделяющая катод и анод
- Токосъемники — медная и алюминиевая фольга для сбора тока с электродов
- Корпус — герметичная оболочка, защищающая внутренние компоненты
Такая конструкция позволяет литий-ионным аккумуляторам эффективно накапливать и отдавать электрическую энергию за счет движения ионов лития между электродами.

Принцип работы Li-ion аккумулятора
Работа литий-ионного аккумулятора основана на принципе интеркаляции — обратимом внедрении ионов лития в кристаллическую решетку электродных материалов. При этом происходят следующие процессы:
При заряде:
- Ионы лития высвобождаются из катода
- Проходят через электролит и сепаратор к аноду
- Внедряются между слоями графита на аноде
- Электроны движутся от катода к аноду по внешней цепи
При разряде:
- Ионы лития покидают графитовый анод
- Через электролит возвращаются к катоду
- Встраиваются обратно в структуру оксида лития
- Электроны движутся от анода к катоду, питая нагрузку
Таким образом, литий-ионный аккумулятор работает за счет циклического перемещения ионов лития между электродами, что сопровождается движением электронов во внешней цепи.
Преимущества литий-ионных аккумуляторов
Li-ion технология получила широкое распространение благодаря ряду важных преимуществ:
- Высокая удельная энергоемкость (до 250 Вт·ч/кг)
- Отсутствие эффекта памяти
- Низкий саморазряд (2-8% в месяц)
- Большое количество циклов заряда-разряда (500-1500)
- Широкий диапазон рабочих температур
- Быстрый заряд (80% за 30-60 минут)
- Высокий КПД (более 90%)
Эти характеристики делают литий-ионные аккумуляторы оптимальным выбором для портативной электроники, электротранспорта и систем накопления энергии.

Недостатки Li-ion аккумуляторов
Несмотря на множество достоинств, литий-ионная технология имеет и некоторые недостатки:
- Высокая стоимость производства
- Деградация при хранении и эксплуатации
- Чувствительность к глубоким разрядам
- Взрывоопасность при нарушении условий эксплуатации
- Необходимость систем контроля и управления
Однако большинство этих недостатков успешно преодолевается за счет совершенствования технологий производства и управления аккумуляторами.
Типы литий-ионных аккумуляторов
Существует несколько основных разновидностей литий-ионных аккумуляторов, различающихся материалами катода:
- LiCoO2 (литий-кобальтовые) — высокая емкость, но низкая безопасность
- LiFePO4 (литий-железо-фосфатные) — высокая безопасность и долговечность
- LiMn2O4 (литий-марганцевые) — высокая мощность, низкая стоимость
- LiNiMnCoO2 (NMC) — сбалансированные характеристики
- LiNiCoAlO2 (NCA) — высокая емкость и мощность
Выбор типа аккумулятора зависит от конкретного применения и требуемого баланса характеристик.

Системы управления батареями (BMS)
Для обеспечения безопасной и эффективной работы литий-ионных аккумуляторов применяются специальные системы управления батареями (Battery Management System, BMS). Основные функции BMS:
- Контроль напряжения, тока и температуры отдельных ячеек
- Балансировка заряда между ячейками
- Защита от перезаряда, переразряда и перегрева
- Оценка состояния заряда (SOC) и состояния работоспособности (SOH)
- Управление процессами заряда и разряда
- Коммуникация с внешними устройствами
Применение BMS позволяет значительно повысить безопасность, надежность и срок службы литий-ионных аккумуляторных батарей.
Перспективы развития литий-ионных технологий
Несмотря на уже достигнутые успехи, литий-ионные технологии продолжают активно развиваться. Основные направления исследований:
- Увеличение удельной энергоемкости (до 400-500 Вт·ч/кг)
- Повышение безопасности и надежности
- Снижение стоимости производства
- Улучшение низкотемпературных характеристик
- Увеличение скорости заряда
- Разработка твердотельных электролитов
Ожидается, что дальнейшее совершенствование литий-ионных аккумуляторов позволит еще больше расширить сферы их применения и ускорить переход к экологически чистой энергетике.

Применение литий-ионных аккумуляторов
Благодаря своим уникальным характеристикам, литий-ионные аккумуляторы нашли широкое применение в различных областях:
- Портативная электроника (смартфоны, ноутбуки, планшеты)
- Электротранспорт (электромобили, электробусы, электровелосипеды)
- Возобновляемая энергетика (накопители энергии для солнечных и ветровых станций)
- Аэрокосмическая отрасль (спутники, космические аппараты)
- Медицинское оборудование (портативные приборы, имплантаты)
- Электроинструмент и садовая техника
- Системы бесперебойного питания
Постоянное совершенствование технологии способствует расширению сфер применения литий-ионных аккумуляторов и их проникновению в новые отрасли.
Безопасность литий-ионных аккумуляторов
Несмотря на высокую надежность современных литий-ионных аккумуляторов, вопросы безопасности остаются актуальными. Основные риски связаны с возможностью:
- Теплового разгона (thermal runaway)
- Короткого замыкания
- Возгорания или взрыва при механических повреждениях
- Выделения токсичных газов при разрушении
Для минимизации этих рисков применяются различные меры безопасности:

- Использование защитных систем BMS
- Применение термостойких сепараторов
- Добавление огнезащитных добавок в электролит
- Установка предохранительных клапанов
- Разработка негорючих твердотельных электролитов
Соблюдение правил эксплуатации и применение современных систем защиты позволяет обеспечить высокий уровень безопасности литий-ионных аккумуляторов.
Как работает литиевая батарея — подробное устройство
Обновленная статья от: 10.11.2020
Литий-ионные аккумуляторы – универсальный тип элементов питания. Они используются в смартфонах, фонариках, портативной технике, специнструменте, источниках
бесперебойного питания. Литий-ионные батареи обеспечивают автономное питание складской и клининговой техники, электромобилей, гольфкаров, инвалидных колясок, гироскутеров, самокатов, велосипедов на электротяге и многих других устройств.
Источники питания на основе лития отличаются высокой энергоемкостью при относительно малых размерах и массе. Дополнительными их преимуществами выступают:
- большой ресурс – более 1000 полных циклов заряд-разряд;
- малый саморазряд – не более 5–10 % в год;
- высокая токоотдача;
- широкий диапазон допустимых температур – от -20 до +60 °С при работе, от 0 до +45 °С при подзарядке;
- простота и удобство использования.
Литиевый аккумулятор – устройство и принцип работы
В структуре Li-ion аккумулятора есть катод из производных лития на алюминиевой фольге и графитовый анод на фольге из меди. В качестве производных лития используются различные соединения: LiCoO2, LiMn2O4, LiFePO4, LiNiO2, LiMnRON, LiC6, LiMnO2, Li4Ti5O12 и др. Между катодом и анодом находится пористый сепаратор, пропитанный электролитом с функциями проводника. Заряд переносят ионы лития, легко встраиваемые в кристаллическую решетку пористого углерода и вызывающие соответствующую химическую реакцию.
В качестве производных лития используются различные соединения: LiCoO2, LiMn2O4, LiFePO4, LiNiO2, LiMnRON, LiC6, LiMnO2, Li4Ti5O12 и др. Между катодом и анодом находится пористый сепаратор, пропитанный электролитом с функциями проводника. Заряд переносят ионы лития, легко встраиваемые в кристаллическую решетку пористого углерода и вызывающие соответствующую химическую реакцию.
Конструкция из электродов и находящегося между ними сепаратора сворачивается в виде рулона и помещается в герметичную оболочку из стали, алюминия или полимерного материала. При этом электроды подсоединяются к токосъемникам. В итоге получаются Li-ion элементы цилиндрической или призматической формы – в зависимости от принципа сворачивания фольги. Самый распространенный типоразмер Li-ion аккумуляторов в форме цилиндра – 18650.
Как работает Li-ion аккумулятор
Принцип действия литий-ионного аккумулятора заключается в создании необходимых условий для перемещения ионов лития между катодом и анодом:
- При подаче на электроды напряжения ионы лития отрываются от катода, переходят через сепаратор к графитовому аноду и встраиваются в его молекулярную структуру.
 В результате протекает реакция окисления, и аккумулятор заряжается.
В результате протекает реакция окисления, и аккумулятор заряжается. - При подаче нагрузки ионы лития перемещаются обратно к катоду. Углеродистая пластинка на медной фольге становится «минусом», а производные лития на алюминии – «плюсом».
Задачи и функции BMS платы
Слабым местом Li-ion аккумуляторов считается их чувствительность к перезарядам и глубоким разрядам. Чтобы напряжение элементов автоматически поддерживалось в безопасном диапазоне, батарея оснащается BMS платой контроля и защиты. Она автоматически размыкает выходные ключи – отключает АКБ от нагрузки при критическом разряде и от сети при полном заряде. БМС плата оберегает элементы питания и от короткого замыкания. В таких ситуациях напряжение на элементах питания резко просаживается, и мгновенно срабатывает защита от глубокого разряда. Тем самым модуль защиты продлевает срок службы АКБ.
Основой BMS платы выступает микросхема. В ней есть полевые транзисторы, используемые для раздельного управления защитой на протяжении заряда и разряда ячеек. Плата защиты следит, чтобы напряжение на каждой ячейке не превышало 4,2 В и не опускалось ниже 2,3 В. Также в схеме обычно присутствует датчик, замеряющий уменьшение напряжения на полевых транзисторах. Функции измерительного шунта выполняет переходное сопротивление транзисторов. В ряде плат дополнительно используется детектор токовых перегрузок.
Плата защиты следит, чтобы напряжение на каждой ячейке не превышало 4,2 В и не опускалось ниже 2,3 В. Также в схеме обычно присутствует датчик, замеряющий уменьшение напряжения на полевых транзисторах. Функции измерительного шунта выполняет переходное сопротивление транзисторов. В ряде плат дополнительно используется детектор токовых перегрузок.
Как работает контроллер заряда в литиевой батарее
Контроллер заряда – важная составляющая зарядного устройства, которая обеспечивает правильный режим подзарядки. Для литиевых элементов это режим CC/CV – вначале осуществляется зарядка при неизменном токе, а затем – при стабильном напряжении.
Контроллер ограничивает зарядный ток и контролирует объем энергии, поступающей на ячейки в единицу времени. Избыточную энергию он рассеивает в виде тепла. При достижении порога срабатывания 4,2 В контроллер переключается в режим стабилизации напряжения и плавно уменьшает ток заряда.
Режимы работы литиевых АКБ
Есть 2 основных режима использования литиевых АКБ:
- Буферный – например, в современных источниках бесперебойного питания.
 Батарея в таком случае постоянно подпитывается от электросети, а при перебоях в электроснабжении – отдает накопленный заряд подключенному к ней оборудованию. Когда электроснабжение от сети восстанавливается, АКБ снова подзаряжается и находится в режиме постоянной готовности к дальнейшему использованию.
Батарея в таком случае постоянно подпитывается от электросети, а при перебоях в электроснабжении – отдает накопленный заряд подключенному к ней оборудованию. Когда электроснабжение от сети восстанавливается, АКБ снова подзаряжается и находится в режиме постоянной готовности к дальнейшему использованию. - Циклический – подразумевает чередование фаз заряд-разряд, когда после пассивной фазы восстановления заряда следует продолжительная фаза активной работы. В таком режиме работают аккумуляторные батареи электровелосипедов и других видов персонального электротранспорта, погрузчиков, поломоечных машин, электромобилей, мотолодок, мобильных кофемашин и другой техники. Срок службы таких АКБ измеряется не годами, а количеством циклов глубокого разряда (до 80%) и последующего заряда.
Литий-ионные батареи успешно используются и в буферном, и в циклическом режиме. Если эксплуатация АКБ подразумевает жесткие условия и частые глубокие разряды, лучше всего с такими задачами справляются литий-железо-фосфатные батареи (LiFePO4). В частности, они используются для питания лодочных электромоторов, складской и клининговой техники, е-байков и других видов электротранспорта.
В частности, они используются для питания лодочных электромоторов, складской и клининговой техники, е-байков и других видов электротранспорта.
Старение и деградация литиевых АКБ
В результате циклического заряда-разряда литиевые аккумуляторы постепенно «стареют» – ионы лития не всегда возвращаются в свое исходное положение, состояние катода меняется, в системе накапливаются продукты окисления. В итоге аккумуляторная батарея медленно и безвозвратно утрачивает часть своей емкости.
Считается, что при потере 30% исходной емкости жизненный цикл батареи завершается. При потере емкости на 50% батарея подлежит утилизации. Рабочий ресурс батареи определяется как количество полных циклов заряда-разряда до тех пор, когда емкость АКБ снизится на 20%. В среднем ресурс Li-ion аккумуляторов составляет 1000 циклов, у моделей вида LiFePO4 – более 2000, а у литий-титанатных – более 20 000.
Рекомендации по использованию
Чтобы продлить срок службы Li-ion батарей, нужно:
- Следовать рекомендациям производителя по их эксплуатации.
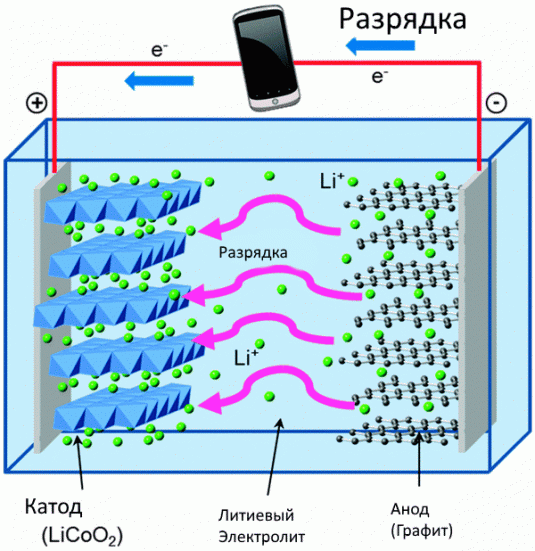
- Не превышать рекомендованный зарядный ток. Оптимальным током заряда считается значение, равное 50% номинальной емкости батареи. Так, для АКБ емкостью 10 Ач оптимальный зарядный ток составляет 5 А. Исключение – современные литий-титанатные модели. Они допускают токовые нагрузки до 10С.
- Избегать перезаряда, глубокого разряда батарей, их длительного хранения в разряженном состоянии, механических повреждений, перегрева и переохлаждения.
Используйте литиевые АКБ правильно, и они долго будут радовать вас отличными рабочими характеристиками.
Предлагаем для ознакомления обзор электрических фэтбайков – электровелосипедов с толстыми колесами.
Литий-ионный аккумулятор (Li-ion) — Принцип работы
В настоящее время литий-ионный аккумулятор используется абсолютно во всей домашней и портативной электронике.
Можно без преувеличения сказать: без портативных источников питания, мир современной техники был бы намного беднее.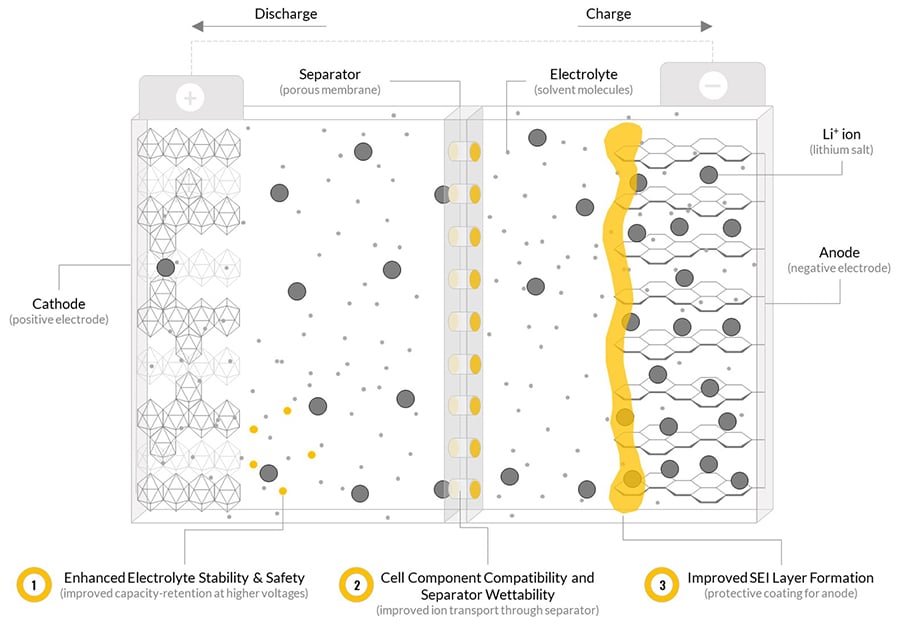 Все разнообразие карманных электронных гаджетов, приборов, смартфонов, гироскутеров, электромобилей наконец, стало возможным благодаря литий-ионным аккумуляторам.
Все разнообразие карманных электронных гаджетов, приборов, смартфонов, гироскутеров, электромобилей наконец, стало возможным благодаря литий-ионным аккумуляторам.
Принцип работы литий-ионного аккумулятора
Давайте рассмотрим литий-ионный аккумулятор. Как видите, он состоит из нескольких слоев с различным химическим составом.
состав литий-ионного аккумулятораВ основе работы литий-ионного аккумулятора лежит, так называемый, электрохимический потенциал. Суть его в том, что металлы стремятся «отдавать» свои электроны. Как видно на рисунке ниже, наибольшая способность к отдаче электронов – у лития, а наименьшая – у фтора. Если такой атом отдает свой электрон, то он становится положительным ионом.
Первая в истории электрическая батарейка, созданная более 200 лет назад Алессандро Вольтой, работала как раз на принципе электрохимического потенциала. Вольта взял два металла с разными электрохимическими потенциалами (цинк и серебро) и получил электрический ток. В честь его открытия такую «батарейку» назвали Вольтовым столбом.
В честь его открытия такую «батарейку» назвали Вольтовым столбом.
В 1991 г. Sony выпустила первый коммерчески успешный литий-ионный аккумулятор.
В литий-ионных элементах используется металл с наибольшей способностью отдавать электроны – литий. У лития всего один электрон на внешней орбите, и он постоянно стремится его «потерять».
атом литияИз-за этого литий считается чрезвычайно химически активным металлом. Он реагирует даже с водой и воздухом. Но активен только чистый литий, а вот его оксид, напротив, очень стабилен.
оксид литияЭто свойство лития как раз используется при создании литий-ионных аккумуляторов.
Допустим, мы каким-то образом отделили атом лития от оксида. Этот атом будет крайне нестабилен и сразу превратится в положительный ион, потеряв электрон.
положительный ионОднако в составе оксида литий гораздо более стабилен, чем одинокий атом лития. Если мы сможем каким-то образом обеспечить движение по двум отдельным путям для электрона и для положительного иона лития, то ион самостоятельно достигнет оксида и встанет там на свое место.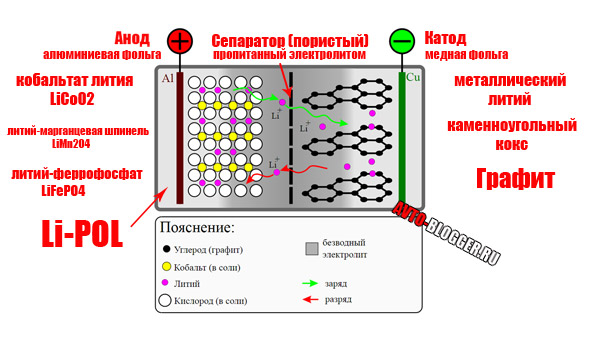 При этом мы получим электрический ток благодаря движению электрона.
При этом мы получим электрический ток благодаря движению электрона.
Итак, можно получить электрический ток из оксида лития, если сначала отделить атомы лития от оксида и затем направить потерянные ими электроны по внешней цепи. Рассмотрим, как эти две задачи решаются в литий-ионных элементах.
Строение литий-ионного аккумулятора
Помимо оксида лития, элементы содержат также электролит и графит. В графите связь между слоями гораздо слабее, чем между атомами внутри слоев, поэтому графит имеет слоистую структуру. (Переходи и смотри подробно про строение атома)
строение литий-ионного аккумулятораЭлектролит, помещенный между оксидом лития и графитом, служит барьером, пропускающим сквозь себя только ионы лития. Электроны же не могут проникать сквозь электролит и отскакивают от него, как теннисный мячик об стенку. В качестве электролита используется органическая соль лития, которая наносится на слой разделителя (о разделителе ниже в статье).
Процесс заряда и разряда литий-ионного аккумулятора
Итак, у нас есть разряженный аккумулятор
литий-ионный аккумулятор разряженныйДавайте же его зарядим. Для этого нам нужен какой-либо источник питания. Что произойдет в этот момент на самом литий-ионном аккумуляторе? Положительный полюс начнет притягивать электроны, «вытаскивая» их из оксида лития.
Для этого нам нужен какой-либо источник питания. Что произойдет в этот момент на самом литий-ионном аккумуляторе? Положительный полюс начнет притягивать электроны, «вытаскивая» их из оксида лития.
Поскольку электроны не могут проникать через электролит, то они движутся по внешней цепи через источник питания.
и в конце концов достигают графита
где очень удобно располагаются в слоях графита.
В этот же самый момент положительные ионы лития притягиваются отрицательным полюсом, проходя сквозь электролит и также попадают в графит, размещаясь между его слоями.
Когда все ионы лития достигнут графита и будут «захвачены» его слоями, батарея будет полностью заряжена.
Такое состояние батареи неустойчивое. Это можно представить как шар, который находится на самой верхушке холма и в любой момент может скатиться.
Вот мы и достигли первой цели: электроны и ионы лития отделены от оксида.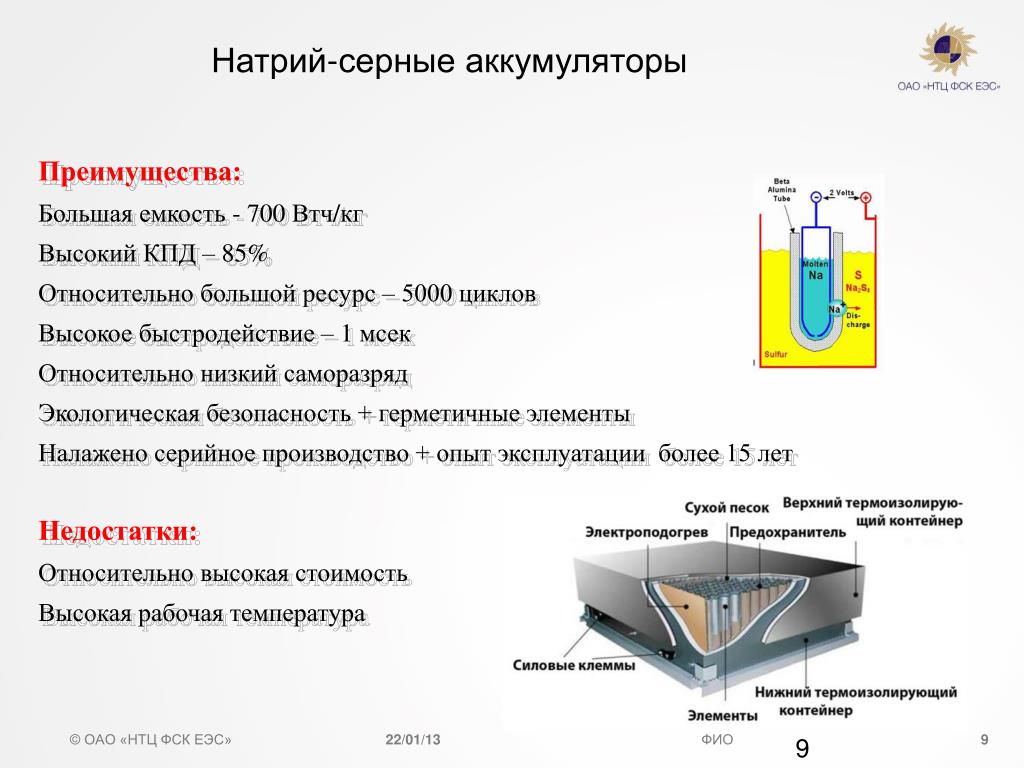 Теперь надо как-то сделать так, чтобы электроны и ионы двигались разными путями. Как только мы подключим какую-либо нагрузку к нашему заряженному литий-ионному аккумулятору, то начнется обратный процесс. В этом случае ионы лития через электролит пожелают вернуться в свое изначальное состояние.
Теперь надо как-то сделать так, чтобы электроны и ионы двигались разными путями. Как только мы подключим какую-либо нагрузку к нашему заряженному литий-ионному аккумулятору, то начнется обратный процесс. В этом случае ионы лития через электролит пожелают вернуться в свое изначальное состояние.
Поэтому они начнут двигаться обратно сквозь электролит, а электроны побегут через внешнюю цепь, то есть через нагрузку.
Так как электрический ток — это не что иное, как упорядоченное движение заряженных частиц, то в цепи лампочки накаливания возникнет электрический ток, который заставит эту самую лампочку светиться.
Как только все электроны «убегут» из графита, то батарея полностью разрядится. Чтобы ее снова зарядить, достаточно поставить аккумулятор «на зарядку».
При этом графит сам по себе не участвует в химических реакциях – он лишь служит «складом» для ионов и электронов лития.
Слой разделителя в литий-ионном аккумуляторе
Если внутренняя температура элемента по какой-то причине начнет расти, жидкий электролит высохнет, и произойдет короткое замыкание между анодом и катодом. В результате элемент может загореться или даже взорваться.
Чтобы этого не произошло, между электродами помещается дополнительный изолирующий слой, называемый разделителем. Разделитель проницаем для ионов лития благодаря наличию микропор. Электроны он не пропускает.
Из чего делают литий-ионный аккумулятор
В реальных литий-ионных аккумуляторах графит и оксид лития наносятся в виде покрытия на медную и алюминиевую фольгу. Ниже на рисунке мы видим, что на тонком листе меди у нас располагается графит, а на тонком листе алюминия — оксид лития.
Минус аккумулятора снимается с медной фольги, а плюс — с алюминиевой.
ну а между ними располагается еще разделитель, пропитанный электролитом
Для того, чтобы уменьшить объем, все эти три слоя сворачивают в «рулончик».
образуя при этом всем нам знакомую литий-ионную цилиндрическую батарейку
Литий-ионные аккумуляторы в автомобиле Tesla
Вообразите мир, в котором все машины оснащены электродвигателями, а не двигателями внутреннего сгорания. Электромоторы превосходят ДВС практически по всем техническим показателям, да к тому же намного дешевле и надежнее. У ДВС есть существенный недостаток: он выдает достаточный крутящий момент лишь в узком диапазоне скоростей. В общем, электродвигатель – однозначно лучший выбор для автомобиля. Об этом мы писали еще в статье про автомобиль Тесла.
Сравнение электромобилей и автомобилей с ДВСНо есть одно «узкое место», из-за которого электрическая революция в автопроме постоянно откладывается — это источники питания. Долгое время громоздкие, тяжелые, недолговечные и ненадежные аккумуляторы электромобилей никак не могли составить конкуренцию полному баку бензина. Но все изменилось, когда на рынок вышел производитель электромобилей Тесла.
Именно литий-ионные аккумуляторы использует компания Тесла для своих электрокаров.
Стандартный элемент выдает напряжение 3,7 – 4,2 В. Множество таких элементов, соединенных последовательно и параллельно, образуют модуль.
Литий-ионные элементы при работе выделяют много тепла. При этом высокая температура снижает срок службы и эффективность самих элементов. Для контроля температуры, а также их уровня заряда, защиты от перезаряда и общего состояния элементов питания, служит специальная система управления батареями (Battery management system, сокращенно BMS). В батареях Tesla используется спиртовая система охлаждения. BMS регулирует скорость движения спирта в системе, поддерживая оптимальную температуру батарей.
радиатор для аккумуляторов ТеслаЕще одна важнейшая функция BMS – защита от перезаряда. Допустим, есть три элемента с разной емкостью. Во время зарядки элемент с большей емкостью зарядится сильнее двух остальных. Чтобы этого не допустить, BMS использует так называемое выравнивание заряда элементов (cell balancing). При этом все элементы заряжаются и разряжаются равномерно и защищены от чрезмерного или недостаточного заряда.
При этом все элементы заряжаются и разряжаются равномерно и защищены от чрезмерного или недостаточного заряда.
И в этом преимущество Tesla над технологией аккумуляторов Nissan. У Nissan Leaf серьезная проблема с охлаждением аккумулятора из-за большого размера элементов и отсутствия системы активного охлаждения.
батарея Nissan Leaf и TeslaУ конструкции с множеством маленьких цилиндрических элементов есть и еще одно преимущество: при большом расходе энергии нагрузка распределяется равномерно между всеми элементами. Если бы вместо множества маленьких элементов был один огромный элемент, из-за постоянных нагрузок он очень быстро бы пришел в негодность. Tesla сделала ставку на маленькие цилиндрические элементы, технология производства которых уже хорошо отработана. Более подробно про батарейный модуль Тесла читайте в этой статье.
Защитный SEI-слой
Во время первой зарядки внутри литий-ионного элемента происходит одно замечательное явление, спасающее элемент от скорой «смерти». Неожиданной проблемой оказались электроны, находящиеся в слое графита. При контакте с электролитом они начинают разрушать его. Но одно случайное открытие позволило не допустить контакт электронов с электролитом. При первой зарядке элемента, как мы уже говорили, ионы лития движутся сквозь электролит. В процессе этого движения молекулы растворенного в электролите вещества покрывают ионы. Достигнув графитового слоя, ионы лития вместе с молекулами раствора электролита реагируют с графитом, образуя так называемая промежуточную фаза твердого электролита (solid electrolyte interphase, или SEI-слой). Этот слой предотвращает контакт электронов с электролитом, предохраняя электролит от разрушения.
Неожиданной проблемой оказались электроны, находящиеся в слое графита. При контакте с электролитом они начинают разрушать его. Но одно случайное открытие позволило не допустить контакт электронов с электролитом. При первой зарядке элемента, как мы уже говорили, ионы лития движутся сквозь электролит. В процессе этого движения молекулы растворенного в электролите вещества покрывают ионы. Достигнув графитового слоя, ионы лития вместе с молекулами раствора электролита реагируют с графитом, образуя так называемая промежуточную фаза твердого электролита (solid electrolyte interphase, или SEI-слой). Этот слой предотвращает контакт электронов с электролитом, предохраняя электролит от разрушения.
Вот так проблема случайным образом решилась сама собой. Хотя эффект SEI был открыт случайно, в последующие два десятилетия ученые целенаправленно улучшали процесс, подбирая наиболее эффективную толщину и химический состав.
Заключение
Сегодня уже удивительно, что еще два десятка лет назад в электронных гаджетах не применялись литий-ионные аккумуляторы. Индустрия литий-ионных аккумуляторов развивается с фантастической скоростью: ожидается, что в ближайшие несколько лет их рынок достигнет 90 млрд. долларов. Современные литий-ионные батареи способны выдержать примерно 3000 циклов зарядки-разрядки – это уже приличный показатель, но еще есть, куда расти. Лучшие умы во всем мире трудятся над тем, чтобы повысить их долговечность до 10 000 циклов. В этом случае аккумулятор электромобиля не придется заменять целых 25 лет. Миллионы долларов вкладываются в исследования, которые позволят заменить графит на кремний в качестве «хранилища» в литий-ионных элементах. Если это удастся сделать, их емкость возрастет более чем в пять раз! В настоящее время мир переходит уже на литий-полимерные аккумуляторы, которые показали себя чуточку лучше, чем литий-ионные.
Индустрия литий-ионных аккумуляторов развивается с фантастической скоростью: ожидается, что в ближайшие несколько лет их рынок достигнет 90 млрд. долларов. Современные литий-ионные батареи способны выдержать примерно 3000 циклов зарядки-разрядки – это уже приличный показатель, но еще есть, куда расти. Лучшие умы во всем мире трудятся над тем, чтобы повысить их долговечность до 10 000 циклов. В этом случае аккумулятор электромобиля не придется заменять целых 25 лет. Миллионы долларов вкладываются в исследования, которые позволят заменить графит на кремний в качестве «хранилища» в литий-ионных элементах. Если это удастся сделать, их емкость возрастет более чем в пять раз! В настоящее время мир переходит уже на литий-полимерные аккумуляторы, которые показали себя чуточку лучше, чем литий-ионные.
Материал подготовлен по статье
Как устроен литий-ионный аккумулятор? | Вольтмаркет
Автор:
Сергей Куртов
Время прочтения: 5 мин
Дата публикации: 18-02-2022
Рейтинг статьи: (2)
Содержание
Представление о современном мире было бы абсолютно другим, если бы не существовало литиевых аккумуляторных батарей. Литий-ионные аккумуляторы стали частью технологической революции, результаты которой мы постоянно наблюдаем вокруг себя (смартфоны, планшеты, ноутбуки и с недавних пор электротранспорт).
Литий-ионные аккумуляторы стали частью технологической революции, результаты которой мы постоянно наблюдаем вокруг себя (смартфоны, планшеты, ноутбуки и с недавних пор электротранспорт).
Несмотря на существование более продвинутых источников питания, например литий-титанатных ячеек (LTO), именно Li-Ion стали по-настоящему массовыми. Это связано с компактными размерами источника питания, невысокой ценой производства и оптимальным ресурсом работы. Под оптимальным ресурсом понимается далеко не самый длительный срок службы, а наоборот: литиевый аккумулятор зачастую соответствует жизненному циклу техники.
В связи с распространенностью элементов Li-Ion, полезно знать, как устроен литий-ионный аккумулятор, как правильно его эксплуатировать и в каких случаях он представляет опасность.
Как работает литий-ионный аккумулятор
В общих чертах строение литиевой батареи похоже на старые добрые свинцово-кислотные АКБ: здесь тоже есть анод, катод и электролит. Активными веществами здесь выступают графит (минус) и оксид лития (плюс). Конечно, анод и катод не состоят исключительно из перечисленных выше веществ. Данные вещества наносятся тонким слоем на медную и алюминиевую фольгу соответственно. Между листами фольги располагается разделитель, пропитанный электролитом.
Конечно, анод и катод не состоят исключительно из перечисленных выше веществ. Данные вещества наносятся тонким слоем на медную и алюминиевую фольгу соответственно. Между листами фольги располагается разделитель, пропитанный электролитом.
В итоге получается эдакий пласт из тонких листов фольги, который и представляет собой литий-ионный аккумулятор. Далее этот пласт скручивается в трубочку — и получается стандартный цилиндрический элемент 18650 и других типоразмеров.
А каким образом описанная выше структура вообще способна накапливать и отдавать электроэнергию? Тут все тоже довольно-таки интересно. Электрический ток — это движение заряженных частиц. Именно это движение нам требуется обеспечить. Цикл работы литий-ионного аккумулятора можно представить следующим образом:
- Процесс заряда. При подключении внешнего источника питания от стабильного оксида лития на алюминиевой пластине отделяются крайне нестабильные атомы лития. На внешней орбите атома имеется электрон, который стремится отделиться.
 Это мгновенно и происходит с атомом лития. Отделившийся электрон не может пройти через слой разделителя — тот пропускает только положительные ионы. Поэтому электрон минует разделитель через внешнюю цепь (зарядное устройство), попадая на медную пластину. После этого оставшиеся на “минусе” положительные ионы лития тоже начинают “притягиваться” положительным полюсом. Они беспрепятственно преодолевают разделитель. В итоге мы имеем положительный полюс, состоящий из слоев графита, которые захватили электроны лития и его ионы. В таком состоянии Li-Ion аккумулятор считается заряженным.
Это мгновенно и происходит с атомом лития. Отделившийся электрон не может пройти через слой разделителя — тот пропускает только положительные ионы. Поэтому электрон минует разделитель через внешнюю цепь (зарядное устройство), попадая на медную пластину. После этого оставшиеся на “минусе” положительные ионы лития тоже начинают “притягиваться” положительным полюсом. Они беспрепятственно преодолевают разделитель. В итоге мы имеем положительный полюс, состоящий из слоев графита, которые захватили электроны лития и его ионы. В таком состоянии Li-Ion аккумулятор считается заряженным. - Процесс разряда. Пока к аккумулятору не подключается внешняя цепь в виде нагрузки, ионы и электроны лития остаются в слоях графита. Но стоит подключить к АКБ потребителя, как начнется активное движение. Ионы “поспешат” вернуться на свое место, протекая через разделитель. Электроны, как и ранее, пройти его не могут и вынуждены двигаться через внешнюю цепь, которая представляет собой потребителя электроэнергии.
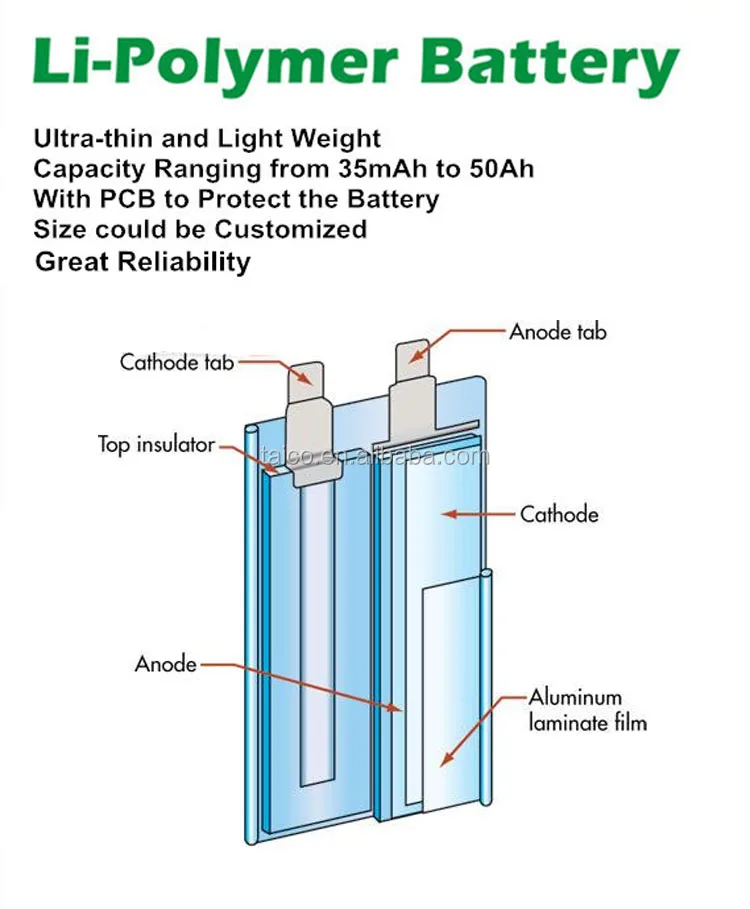 Пусть это будет традиционная лампочка. Протекая из положительной пластины через потребителя, электроны образуют электрический ток. Достигнув пункта назначения, ионы лития и электроны снова становятся частью стабильного оксида лития.
Пусть это будет традиционная лампочка. Протекая из положительной пластины через потребителя, электроны образуют электрический ток. Достигнув пункта назначения, ионы лития и электроны снова становятся частью стабильного оксида лития.
Таким образом, основной идеей литий-ионных аккумуляторов является то, что электронам требуется внешняя цепь, чтобы перетечь вслед за положительными ионами. Именно на счет этого аккумулятор может как заряжаться, так и разряжаться — меняется лишь направление движения частиц.
Опасны ли Li-Ion аккумуляторы
Как мы теперь знаем, в работе литиевого аккумулятора замешаны нестабильные вещества, которые то и дело норовят высвободить энергию. В процессе электрохимической реакции выделяются газы, так как когда ионы лития оседают на одной пластине, на другой образуются соли кислорода. Как и в случае с необслуживаемыми свинцово-кислотными АКБ, в случае нормальной работы газовыделение полностью контролируется. Но в случае перегрева или перезаряда аккумулятор может вздуться от внутреннего давления.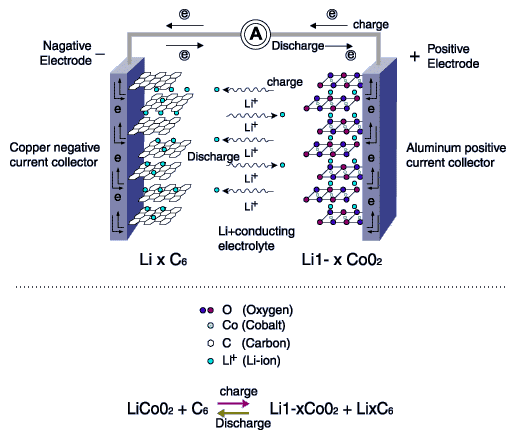
Как правило, АКб мобильных гаджетов оснащены контроллером и нарушение параметров заряда практически невозможно. Но всегда есть место заводскому браку или халатности “no-name” производителей, в результате чего аккумулятор может представлять опасность. Если АКБ вздулась — незамедлительно ее утилизируйте, иначе может случиться воспламенение.
Как взрываются литий-ионные аккумуляторы? Опять же, все снова связано с нестабильностью лития. При контакте с кислородом он тут же воспламеняется. Поэтому герметичность элемента питания очень важна. Также одной из стандартных причин возгорания может стать короткое замыкание между положительной и отрицательной пластиной. Наиболее часто это происходит из-за сочетания сильной степени износа и допущения перегрева, который негативно сказывается на целостности электролита. Разделитель призван защитить пользователя от внутреннего короткого замыкания, однако вероятность этого все равно имеется.
Что же делать, если аккумулятор вот-вот загорится или уже горит? Можно ли тушить литиевую батарею водой? Выше мы уже обратили внимание, что литий активно реагирует с кислородом, который в том числе имеется в составе воды. Поливать аккумулятор не рекомендуется, так как это может спровоцировать взрыв элемента. Пользователи, имевшие дело с воспламенением литий-ионного аккумулятора, советуют дать реакции закончится естественным способом, поместив АКБ в безопасное место, например в закрытую кастрюлю. Если же аккумулятор уже горит и взять его невозможно, очаг следует накрыть чем-то негорючим. Опять же, условная кастрюля, которой можно накрыть АКБ, отлично для этого подходит: и не допустит распространение огня, и перекроет доступ кислорода.
Поливать аккумулятор не рекомендуется, так как это может спровоцировать взрыв элемента. Пользователи, имевшие дело с воспламенением литий-ионного аккумулятора, советуют дать реакции закончится естественным способом, поместив АКБ в безопасное место, например в закрытую кастрюлю. Если же аккумулятор уже горит и взять его невозможно, очаг следует накрыть чем-то негорючим. Опять же, условная кастрюля, которой можно накрыть АКБ, отлично для этого подходит: и не допустит распространение огня, и перекроет доступ кислорода.
Принцип работы литий-ионного аккумулятора — E-Lyte Innovations GmbH
Литий-ионные батареи относятся к группе батарей, которые генерируют электрическую энергию путем преобразования химической энергии посредством окислительно-восстановительных реакций на активных материалах, т. е. отрицательном (аноде) и положительном электроде (катоде), в одном или нескольких электрически соединенных гальванических элементах. Литий-ионные батареи можно разделить на первичные (неперезаряжаемые) и вторичные (перезаряжаемые) батареи, в зависимости от того, перезаряжаются ли они электрическим током.
В обычных литий-ионных батареях ионы Li + перемещаются между положительным электродом (обычно из слоистого оксида переходного металла) и отрицательным электродом на основе графита по принципу «кресла-качалки» (см. видео) .
Термин «разрядка» используется для обозначения процесса, при котором батарея подает электрическую энергию на внешнюю нагрузку. Электролит в этой системе содержит дополнительные ионы Li + для обеспечения быстрого переноса ионного заряда внутри элемента.
Помимо ионной проводимости, электролит выполняет другие важные функции:
Поддержка образования эффективных межфазных фаз (например, межфазная фаза твердого электролита, SEI или межфазная фаза катодного электролита, CEI), которые:
Способствуют безопасности клеток – будучи инертными по отношению к другим материалам, таким как:
- Сепаратор
- Токосъемники
- Проводящие добавки, связующие
- Кожух ячейки
Шаг 1 — Исходное состояние (состояние заряда (SOC) 0%)
При разрядке ионы Li + — находятся в материале положительного электрода. Таким образом, положительный электрод является источником ионов Li + -, необходимых для преобразования электрической энергии в химическую. Чтобы позволить Ли + -ионы мигрируют от положительного электрода к отрицательному, электролит также обогащается Li + -ионами.
Таким образом, положительный электрод является источником ионов Li + -, необходимых для преобразования электрической энергии в химическую. Чтобы позволить Ли + -ионы мигрируют от положительного электрода к отрицательному, электролит также обогащается Li + -ионами.
Шаг 2 — Формирование SEI и CEI
В самом начале первого процесса зарядки электроны мигрируют из материала положительного электрода (окисление) через внешний проводник в материал отрицательного электрода (восстановление). Для обеспечения зарядовой нейтральности Li + -ионы деинтеркалируют из материала положительного электрода в электролит и мигрируют через электролит в материал отрицательного электрода для последующего хранения. В результате этих реакций на границах раздела электролит/поверхность отрицательного электрода и электролит/положительный электрод соответственно образуются граничные фазы, так называемые SEI и CEI. Эти межфазные слои образованы нерастворимыми продуктами электрохимического разложения компонентов электролита и Li + -ионы, происходящие от положительного электрода, и обеспечивают обратимый цикл батареи. После образования SEI и CEI дальнейшие ионы Li + деинтеркалируют из материала положительного электрода в электролит и мигрируют через него в материал отрицательного электрода, чтобы впоследствии включиться в последний.
Эти межфазные слои образованы нерастворимыми продуктами электрохимического разложения компонентов электролита и Li + -ионы, происходящие от положительного электрода, и обеспечивают обратимый цикл батареи. После образования SEI и CEI дальнейшие ионы Li + деинтеркалируют из материала положительного электрода в электролит и мигрируют через него в материал отрицательного электрода, чтобы впоследствии включиться в последний.
Этап 3. Электродные реакции
После формирования SEI и CEI далее Li + ионов деинтеркалируют из материала положительного электрода в электролит и мигрируют через него в материал отрицательного электрода для последующего включения в последний.
Положительный электрод:
LI M O 2 → LI (1- x ) M O 2 + x · E 9000 – 2 + x · E 9000 – + x · E 9000 – + x · E 9000 – + x · E 9000 – + x · E 9008 – + x · E 9008 – + x · E 9008 –.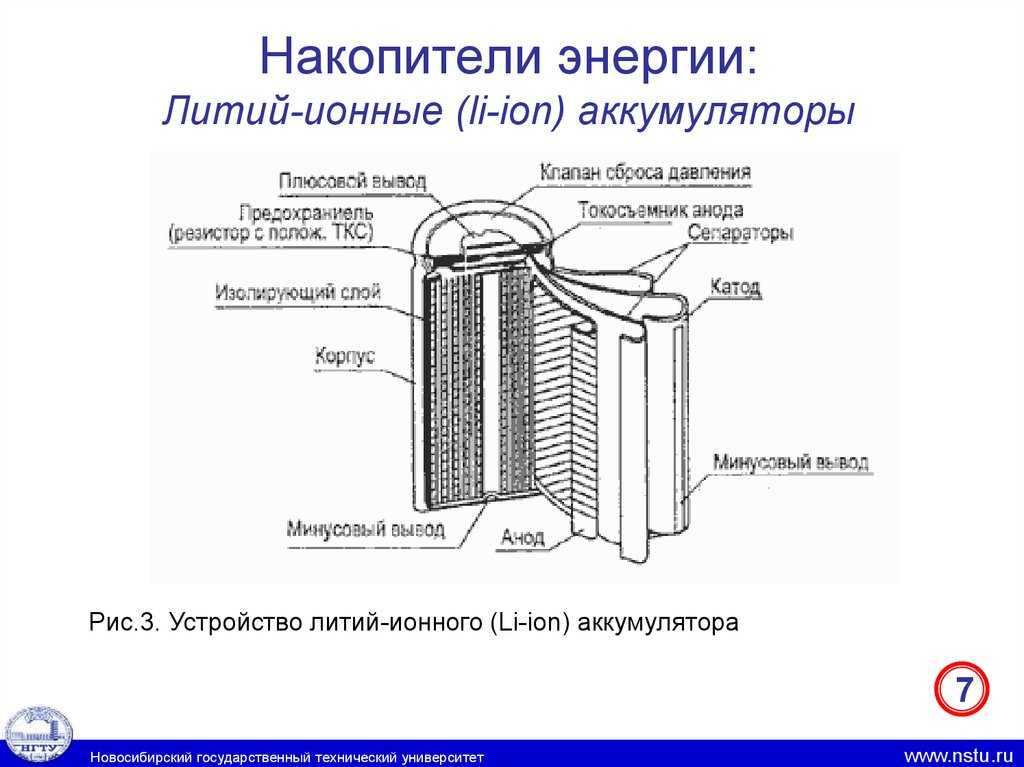 +
+
Отрицательный электрод:
C 6 + x · E — + x · LI + → LI x C 6
Общая реакция клеток:
LIT CLOT O 2 → Li x C 6 + Li (1- x ) MO 2
Шаг 4 — Изменение цвета при интеркаляции/деинтеркаляции в графит
В зависимости от количества ионов Li + , встроенных в отрицательный электрод (в зависимости от степени заряда, SOC), он меняет цвет с черного на красный (ранний SOC) на золотой (100% SOC).
Шаг 5. Выписка
При разряде происходят обратные реакции. Электродные реакции:
Положительный электрод = «катод» (восстановление)
LI (1- x ) M O 2 + x · E — + x · LI + → LI M O · LI + → LI M O 2 → LI M O 9 2
→ LI M x · LI + → LI M x · LI + → LI M x .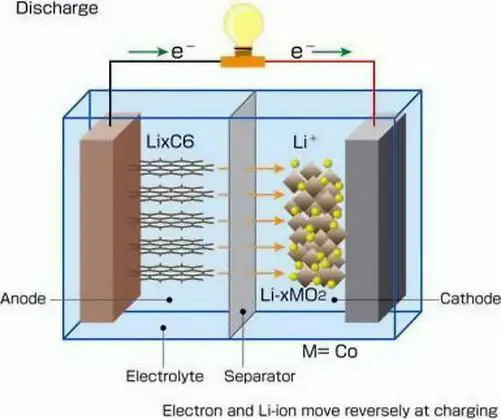 Электрод = «анод» (окисление)
Электрод = «анод» (окисление) LI x C 6 → C 6 + x · E — + x · LI +
+ x · LI + + x · li + .
Шаг 6 — Принцип кресла-качалки
После разряда (SOC 0%) ионы Li + восстанавливаются в материале положительного электрода, из которого они изначально были получены. Возвратно-поступательное движение Li + -ионов напоминает движение кресла-качалки, поэтому этот принцип получил название «принцип кресла-качалки».
Особенно первый цикл (зарядка и разрядка) связан с необратимой потерей ионов Li + в SEI и CEI, а также в материале отрицательного электрода. В результате меньше Li + -ионы теперь могут накапливаться в отрицательном электроде в следующем цикле заряда, что приводит к снижению емкости аккумулятора.
В литий-ионном аккумуляторе происходят различные процессы старения, которые снижают производительность аккумулятора в течение периода использования и сильно зависят от химического состава элемента и предполагаемого использования аккумулятора. В частности, правильный выбор электролита оказывает огромное влияние на эти механизмы старения и еще раз подчеркивает важность электролитов, изготовленных по индивидуальному заказу.
Для оптимизации литий-ионных аккумуляторов в отношении удельной энергии и плотности энергии, срока службы и безопасности было предпринято много усилий для дальнейшего расширения возможностей применения ЛИА. В частности, растущие потребности в литий-ионных батареях с высокой удельной энергией и плотностью энергии, особенно для автомобильных приложений, стимулируют исследовательские усилия во всем мире. Плотность энергии и удельная энергия аккумуляторов по определению — это количество энергии, запасенной в данной системе на единицу объема и на единицу массы соответственно. Произведение удельной емкости на среднее напряжение разряда дает удельную энергию, и это соотношение находит выражение в уравнении 1:
Произведение удельной емкости на среднее напряжение разряда дает удельную энергию, и это соотношение находит выражение в уравнении 1:
E = C · U (1)
Согласно уравнению 1 кажется разумным, что большая часть текущих исследований сосредоточена на новых материалах положительных электродов с более высокими рабочими напряжениями (подход с высоким напряжением) и/или повышенной удельной емкостью (высокопроизводительный подход). Высоковольтные катодные материалы сильно ограничены узким окном электрохимической стабильности современных электролитов на основе карбонатов (≈1,0–4,4 В против Li/Li + ) и усилить конструкцию внутренне стабильных электролитов или подходящих добавок к электролиту, позволяющих создавать высоковольтные литий-ионные батареи.
Мы с нетерпением ждем вашего сообщения
Имя
Пожалуйста, оставьте это поле пустым.
Фамилия
Пожалуйста, оставьте это поле пустым.
Компания
Адрес электронной почты
Сообщение
Я согласен с обработкой введенных данных, а также с заявлением о защите данных.
Для получения дополнительной информации см. нашу Политику конфиденциальности.
Литий-ионная батарея Принцип работы и применение — StudiousGuy
Литий-ионная батарея — это тип перезаряжаемой батареи, в которой используются заряженные частицы лития для преобразования химической энергии в электрическую. М. Стэнли Уиттингем, британо-американский химик, известен как отец-основатель литий-ионных аккумуляторов. Он разработал концепцию перезаряжаемых батарей в конце 1970-х годов. В 2019 году, М. Стэнли Уиттингем, Джон Гуденаф и Акира Йошино были удостоены Нобелевской премии по химии за свою работу. По способности к перезарядке литий-ионные аккумуляторы можно разделить на две большие категории, а именно первичные и вторичные. Первичные литий-ионные аккумуляторы не подлежат перезарядке, а вторичные литий-ионные аккумуляторы можно перезаряжать.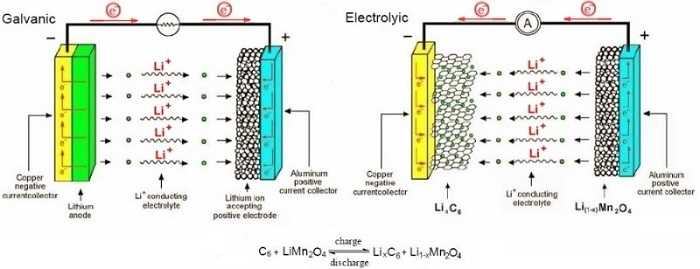
Указатель статей (Щелкните, чтобы перейти)
Принцип работы литий-ионной батареи
Литий-ионные батареи работают по принципу кресла-качалки. Здесь преобразование химической энергии в электрическую происходит с помощью окислительно-восстановительных реакций. Обычно литий-ионный аккумулятор состоит из двух или более электрически соединенных гальванических элементов. Когда батарея заряжена, ионы стремятся двигаться к отрицательному электроду или аноду. Когда аккумулятор полностью разряжается, ионы лития возвращаются обратно к положительному электроду, то есть к катоду. Это означает, что во время процесса зарядки и разрядки ионы лития перемещаются между двумя электродами батареи, поэтому принцип работы литий-ионной батареи называется принципом кресла-качалки.
Работа литий-ионной батареи
Батарея обычно состоит из двух электродов, а именно анода и катода. Катод образует положительную клемму батареи, а анод предназначен для отрицательной клеммы. Катод литий-ионной батареи в основном состоит из соединения лития, а основным элементом анода является графит. Когда батарея подключена к источнику питания, ионы лития имеют тенденцию перемещаться от катода к аноду, то есть от положительного электрода к отрицательному электроду. Это называется зарядкой аккумулятора. Во время фазы разрядки батареи движение ионов лития меняется на противоположное от анода к катоду, то есть от отрицательного электрода к положительному, и электрическая энергия передается на подключенную нагрузку.
Когда батарея подключена к источнику питания, ионы лития имеют тенденцию перемещаться от катода к аноду, то есть от положительного электрода к отрицательному электроду. Это называется зарядкой аккумулятора. Во время фазы разрядки батареи движение ионов лития меняется на противоположное от анода к катоду, то есть от отрицательного электрода к положительному, и электрическая энергия передается на подключенную нагрузку.
Использование литий-ионных аккумуляторов
Сотовые устройства
Почти все сотовые устройства, такие как мобильные телефоны, ноутбуки, беспроводные телефоны и т. д., используют литий-ионные аккумуляторы. Это связано с тем, что литий-ионные аккумуляторы компактны, легки и пригодны для повторного использования. Следовательно, они идеально подходят для портативных устройств. Кроме того, такие типы батарей обеспечивают быструю скорость зарядки, что позволяет пользователю часто получать доступ к устройствам без помех.
Power Banks
Power Bank — это портативный гаджет, который помогает пользователю удобно заряжать электронные устройства, такие как мобильные телефоны, смарт-часы и т. д., в любом месте и в любое время. Для этой цели в Power Bank обычно используются литий-ионные и литий-полимерные аккумуляторы.
д., в любом месте и в любое время. Для этой цели в Power Bank обычно используются литий-ионные и литий-полимерные аккумуляторы.
Электромобили
Ряд электромобилей, таких как электромобили, электрические велосипеды, электрические скутеры, электрические велосипеды и т. д., используют для своей работы литий-ионные батареи. Это связано с тем, что литий-ионные аккумуляторы имеют высокое отношение мощности к весу, большую устойчивость к колебаниям температуры и давления и более высокую плотность энергии, чем свинцово-кислотные аккумуляторы. Кроме того, они легкие, портативные, эффективные и более безопасные, чем традиционные батареи.
Медицинские устройства
Медицинские устройства, такие как слуховые аппараты, хирургические инструменты, диагностические аппараты, кардиостимуляторы, дефибрилляторы, роботы-помощники, инфузионные насосы, мониторы частоты сердечных сокращений и пульса и т. д., используют литий-ионные батареи для различных диагностических и цели лечения. К преимуществам использования литий-ионных аккумуляторов в медицинских гаджетах можно отнести высокое быстродействие, быструю скорость зарядки, малый вес, безопасность и др.
К преимуществам использования литий-ионных аккумуляторов в медицинских гаджетах можно отнести высокое быстродействие, быструю скорость зарядки, малый вес, безопасность и др.
Камеры
Литий-ионные аккумуляторы широко используются в цифровых зеркальных фотокамерах, поскольку они способны обеспечивать большую мощность в течение сравнительно более длительного времени, чем традиционные аккумуляторы. Кроме того, литий-ионные аккумуляторы предпочтительнее, потому что они легкие, а значит, не делают гаджет громоздким. В некоторых камерах также используются перезаряжаемые литий-ионные батареи, что позволяет пользователю повторно использовать их и повышает надежность.
ИБП
ИБП (система бесперебойного питания) — это устройство, обеспечивающее резервное питание в течение определенного периода времени в случае отключения или сбоя питания. В таких устройствах обычно используется комбинация литий-ионных аккумуляторов. Это связано с тем, что использование литий-ионных аккумуляторов в устройствах ИБП уменьшает занимаемую площадь на 50-80%. Кроме того, система ИБП на основе литий-ионных аккумуляторов весит на 60–80 % меньше, чем обычное устройство ИБП на основе свинцово-кислотных батарей.
Кроме того, система ИБП на основе литий-ионных аккумуляторов весит на 60–80 % меньше, чем обычное устройство ИБП на основе свинцово-кислотных батарей.
Роботы
Литий-ионные аккумуляторы очень популярны в области робототехники и автоматизации науки. Они используются для питания роботов-гуманоидов, а также промышленных роботов.
Преимущества литий-ионных аккумуляторов
1. Литий-ионные аккумуляторы имеют значительно более низкую скорость саморазряда по сравнению с другими типами аккумуляторов.
2. Обладают высокой плотностью энергии.
3. В литий-ионных батареях отсутствует эффект памяти.
4. Средний срок службы литий-ионных аккумуляторов в десять раз больше, чем у традиционных свинцово-кислотных аккумуляторов.
5. Высокая скорость зарядки литий-ионных аккумуляторов.
6. Литий-ионные аккумуляторы эффективно работают в экстремальных условиях, таких как высокое давление и колебания температуры.
7. Литий-ионные аккумуляторы легкие и компактные. Как правило, вес литий-ионных аккумуляторов примерно на 50-60% меньше, чем у стандартных свинцово-кислотных аккумуляторов.
Литий-ионные аккумуляторы легкие и компактные. Как правило, вес литий-ионных аккумуляторов примерно на 50-60% меньше, чем у стандартных свинцово-кислотных аккумуляторов.
8. Установка литий-ионных аккумуляторов сравнительно проста.
9. Аккумуляторы этого типа гибкие, менее громоздкие и безопасные в использовании.
10. Литий-ионные аккумуляторы доступны в различных формах и размерах.
11. Уровень напряжения литий-ионного аккумулятора не падает и поддерживается постоянно на протяжении всего использования.
12. Емкость литий-ионного аккумулятора примерно на 25-50% больше, чем у свинцово-кислотного аккумулятора.
13. Требуют минимального обслуживания.
14. Литий-ионные аккумуляторы неопасны, так как не выделяют ядовитых газов.
Недостатки литий-ионных аккумуляторов
1. Зарядная емкость литий-ионных аккумуляторов со временем снижается из-за потери ионов лития на границе твердого электролита и на границе катод-электролит.
2. Если сепаратор литий-ионных аккумуляторов поврежден, они могут стать причиной возгорания.
3. Они относительно дорогие.
4. Если в аккумуляторе закончились ионы лития, его нельзя заменить. Таким образом, батарея не может быть использована по истечении ориентировочного срока службы.
BU-204: Как работают литиевые батареи?
Пионерские работы по литиевой батарее начались в 1912 г. под руководством Г.Н. Льюисом, но только в начале 1970-х годов в продажу поступили первые неперезаряжаемые литиевые батареи. Попытки разработать перезаряжаемые литиевые батареи последовали в 1980-х годах, но потерпели неудачу из-за нестабильности металлического лития, используемого в качестве материала анода. (В металл-литиевой батарее в качестве анода используется литий, в литий-ионной — графит в качестве анода, а в катоде — активные материалы.)
Литий — самый легкий из всех металлов, обладает самым большим электрохимическим потенциалом и обеспечивает наибольшую удельную энергию на единицу веса. Аккумуляторы с металлическим литием на аноде могут обеспечить чрезвычайно высокую плотность энергии; однако в середине 1980-х годов было обнаружено, что при циклировании на аноде образуются нежелательные дендриты. Эти частицы роста проникают в сепаратор и вызывают короткое замыкание. Температура элемента быстро повышалась и приближалась к температуре плавления лития, что приводило к тепловому разгону, также известному как «вентиляция пламенем». Большое количество перезаряжаемых металлических литиевых батарей, отправленных в Японию, было отозвано в 1991 после того, как батарея в мобильном телефоне выпустила горящие газы и нанесла ожоги лицу мужчины.
Аккумуляторы с металлическим литием на аноде могут обеспечить чрезвычайно высокую плотность энергии; однако в середине 1980-х годов было обнаружено, что при циклировании на аноде образуются нежелательные дендриты. Эти частицы роста проникают в сепаратор и вызывают короткое замыкание. Температура элемента быстро повышалась и приближалась к температуре плавления лития, что приводило к тепловому разгону, также известному как «вентиляция пламенем». Большое количество перезаряжаемых металлических литиевых батарей, отправленных в Японию, было отозвано в 1991 после того, как батарея в мобильном телефоне выпустила горящие газы и нанесла ожоги лицу мужчины.
Присущая металлическому литию нестабильность, особенно во время зарядки, сместила исследования в сторону неметаллических растворов с использованием ионов лития. В 1991 году Sony выпустила на рынок первый ионно-литиевый аккумулятор, и сегодня эта химия стала самой многообещающей и быстрорастущей батареей на рынке. Хотя удельная энергия ниже, чем у металлического лития, литий-ион безопасен при условии соблюдения ограничений по напряжению и току. (См. BU-304a: Вопросы безопасности при использовании Li-ion)
(См. BU-304a: Вопросы безопасности при использовании Li-ion)
Изобретение литий-кобальт-оксидной батареи должно принадлежать Джону Б. Гуденафу (1922 г.). Говорят, что во время разработки аспирант, нанятый Nippon Telephone & Telegraph (NTT), работал с Гуденафом в США. Вскоре после прорыва студент вернулся в Японию, взяв с собой открытие. Затем, в 1991 году, Sony объявила о международном патенте на катод из оксида лития-кобальта. Последовали годы судебных тяжб, но Sony смогла сохранить патент, а Гуденаф ничего не получил за свои усилия. В знак признания вклада в разработку литий-ионных аккумуляторов Национальная инженерная академия США в 2014 году наградила Гуденафа и других участников премией Чарльза Старка Дрейпера. Институт для оказания помощи в исследовании материалов.
Ключом к превосходной удельной энергии является высокое напряжение элемента 3,60 В. Улучшения в активных материалах и электролитах могут еще больше повысить плотность энергии. Нагрузочные характеристики хорошие, а плоская кривая разряда обеспечивает эффективное использование накопленной энергии в желательном и ровном спектре напряжения 3,70–2,80 В на элемент.
В 1994 году стоимость производства литий-ионного аккумулятора в цилиндрическом элементе 18650 превышала 10 долларов США, а емкость составляла 1100 мАч. В 2001 году цена упала ниже 3 долларов, а вместимость выросла до 1,9.00 мАч. Сегодня аккумуляторы 18650 с высокой плотностью энергии обеспечивают более 3000 мАч, а стоимость снижается. Снижение стоимости, повышенная удельная энергия и отсутствие токсичных материалов проложили путь к тому, чтобы сделать литий-ионный аккумулятор общепризнанным аккумулятором для портативных устройств, тяжелой промышленности, электрических силовых агрегатов и спутников. 18650 имеет диаметр 18 мм и длину 65 мм. (См. BU-301: Взгляд на упаковку старых и новых аккумуляторов)
Литий-ионный аккумулятор не требует особого обслуживания, а это преимущество, на которое не может претендовать большинство других химических элементов. Аккумулятор не имеет памяти и не нуждается в упражнениях (преднамеренной полной разрядке), чтобы поддерживать его в хорошем состоянии. Саморазряд в два раза меньше, чем у систем на основе никеля, и это помогает использовать датчики уровня топлива. Номинальное напряжение ячейки 3,60 В может напрямую питать мобильные телефоны, планшеты и цифровые камеры, предлагая упрощение и снижение затрат по сравнению с конструкциями с несколькими ячейками. Недостатками являются необходимость в схемах защиты от злоупотреблений, а также высокая цена.
Саморазряд в два раза меньше, чем у систем на основе никеля, и это помогает использовать датчики уровня топлива. Номинальное напряжение ячейки 3,60 В может напрямую питать мобильные телефоны, планшеты и цифровые камеры, предлагая упрощение и снижение затрат по сравнению с конструкциями с несколькими ячейками. Недостатками являются необходимость в схемах защиты от злоупотреблений, а также высокая цена.
Типы литий-ионных аккумуляторов
В литий-ионных батареях используется катод (положительный электрод), анод (отрицательный электрод) и электролит в качестве проводника. (Анод разряжающейся батареи отрицательный, а катод положительный (см. BU-104b: Конструктивные блоки батареи). Катод представляет собой оксид металла, а анод состоит из пористого углерода. Во время разряда ионы перетекают от анода к катоду через электролит и сепаратор, заряд меняет направление, и ионы текут от катода к аноду.0015 Рисунок 1 иллюстрирует этот процесс.
Рисунок 1: Ионный поток в литий-ионном аккумуляторе.
Когда элемент заряжается и разряжается, ионы перемещаются между катодом (положительным электродом) и анодом (отрицательным электродом). При разряде анод подвергается окислению или потере электронов, а катод испытывает восстановление или прирост электронов. Заряд меняет направление движения. Литий-ионные аккумуляторы
бывают разных видов, но все они имеют одну общую черту — лозунг «литий-ион». Несмотря на поразительное сходство на первый взгляд, эти батареи различаются по производительности, а выбор активных материалов придает им уникальные особенности. (См. BU-205: Типы Li-ion)
Оригинальная литий-ионная батарея Sony использовала кокс в качестве анода (угольный продукт). С 1997 года большинство производителей ионно-литиевых аккумуляторов, включая Sony, перешли на графит, чтобы добиться более плоской кривой разряда. Графит — это форма углерода, обладающая долговременной циклической стабильностью и используемая в графитовых карандашах. Это самый распространенный углеродный материал, за которым следуют твердый и мягкий углерод. Углеродные нанотрубки еще не нашли коммерческого применения в литий-ионных батареях, поскольку они имеют тенденцию запутывать и влиять на производительность. Материалом будущего, который обещает улучшить характеристики литий-ионных аккумуляторов, является графен.
Углеродные нанотрубки еще не нашли коммерческого применения в литий-ионных батареях, поскольку они имеют тенденцию запутывать и влиять на производительность. Материалом будущего, который обещает улучшить характеристики литий-ионных аккумуляторов, является графен.
На рис. 2 показана кривая разряда напряжения современного литий-ионного аккумулятора с графитовым анодом и ранней коксовой версии.
Аккумулятор должен иметь плоскую кривую напряжения в рабочем диапазоне разрядки. Современный графитовый анод делает это лучше, чем ранняя коксовая версия. Предоставлено Cadex
Было опробовано несколько добавок, в том числе сплавы на основе кремния, для улучшения характеристик графитового анода. Требуется шесть атомов углерода (графита), чтобы связать один ион лития; один атом кремния может соединиться с четырьмя ионами лития. Это означает, что кремниевый анод теоретически может хранить в 10 раз больше энергии, чем графит, но расширение анода во время заряда представляет собой проблему. Поэтому аноды из чистого силикона непрактичны, и обычно к аноду на основе кремния добавляют только 3–5 процентов кремния для достижения хорошего срока службы.
Поэтому аноды из чистого силикона непрактичны, и обычно к аноду на основе кремния добавляют только 3–5 процентов кремния для достижения хорошего срока службы.
Использование наноструктурированного титаната лития в качестве добавки к аноду показывает многообещающий срок службы, хорошие возможности нагрузки, отличные низкотемпературные характеристики и превосходную безопасность, но удельная энергия низка, а стоимость высока.
Эксперименты с материалом катода и анода позволяют производителям улучшать внутренние качества, но одно усовершенствование может поставить под угрозу другое. Так называемая «энергетическая ячейка» оптимизирует удельную энергию (емкость) для достижения длительного времени работы, но при более низкой удельной мощности; «Power Cell» предлагает исключительную удельную мощность, но при меньшей мощности. «Hybrid Cell» представляет собой компромисс и предлагает понемногу и то, и другое. (Подробнее о BU-501: Основы разрядки)
Производители могут относительно легко добиться высокой удельной энергии и низкой стоимости, добавляя никель вместо более дорогого кобальта, но это делает элемент менее стабильным.