Как часто встречаются аденомы гипофиза. Что такое болезнь Кушинга и кортикотропиномы. Какова морфология кортикотропином. Каков патогенез болезни Кушинга. Как диагностировать кортикотропиномы на ранней стадии.
Распространенность аденом гипофиза
Аденомы гипофиза встречаются гораздо чаще, чем принято считать. По данным аутопсий, они обнаруживаются у 6,8-22,6% умерших от различных причин. При этом при жизни большинство из них остаются недиагностированными.
Среди всех внутричерепных новообразований аденомы гипофиза составляют около 10%. По частоте встречаемости они распределяются следующим образом:
- Пролактин-секретирующие — 39%
- Соматотропин-секретирующие — 38%
- Гормонально-неактивные — 21%
- Кортикотропиномы (АКТГ-секретирующие) — 4%
Таким образом, кортикотропиномы являются наиболее редким видом гормонально-активных аденом гипофиза. При этом они могут вызывать тяжелое эндокринное заболевание — болезнь Кушинга.

Болезнь Кушинга и кортикотропиномы
Болезнь Кушинга — это нейроэндокринное заболевание, вызванное гиперсекрецией адренокортикотропного гормона (АКТГ) аденомой гипофиза. Повышенная секреция АКТГ приводит к двусторонней гиперплазии коры надпочечников и гиперкортизолизму.
Впервые болезнь была описана Харви Кушингом в 1912 и 1932 годах. Он обнаружил связь заболевания с мельчайшими аденомами гипофиза в 8 из 10 описанных случаев.
По современным данным, аденомы гипофиза обнаруживаются у 60-90% пациентов с болезнью Кушинга. При этом в 80-90% случаев это микроаденомы размером менее 10 мм. Описаны даже кортикотропиномы диаметром 2 мм и менее.
Морфология кортикотропином
При гистологическом исследовании выделяют следующие типы кортикотропином:
- Базофильные (около 80% случаев)
- Хромофобные
- Эозинофильные
- Злокачественные (редко)

Некоторые гормонально-активные кортикотропиномы образованы хромофобными клетками, содержащими небольшое количество гранул в цитоплазме.
Встречаются также «немые» (silent) кортикотропиномы, которые содержат АКТГ, но не проявляются клинически повышенной секрецией гормона.
Патогенез болезни Кушинга
В основе патогенеза болезни Кушинга лежит нарушение регуляции секреции АКТГ и кортизола по механизму обратной связи. Клетки аденомы секретируют АКТГ автономно, без нормального суточного ритма. Это приводит к гиперсекреции кортизола корой надпочечников с нарушением его суточного ритма выработки.
Избыток глюкокортикоидов вызывает характерные симптомы болезни Кушинга:
- Усиление глюконеогенеза и липогенеза
- Остеопороз
- Гирсутизм и нарушения менструального цикла у женщин
- Артериальную гипертензию
- Мышечную слабость
Механизмы развития кортикотропином
Существуют две основные гипотезы развития кортикотропином:
- Поликлональная — в основе лежат нарушения механизмов обратной связи в системе гипоталамус-гипофиз-надпочечники
- Моноклональная — опухоль развивается из одной мутировавшей клетки
До сих пор нет единого мнения о том, является ли первичным поражение гипоталамуса с гиперстимуляцией гипофиза или заболевание связано с первичным возникновением спонтанной аденомы гипофиза.
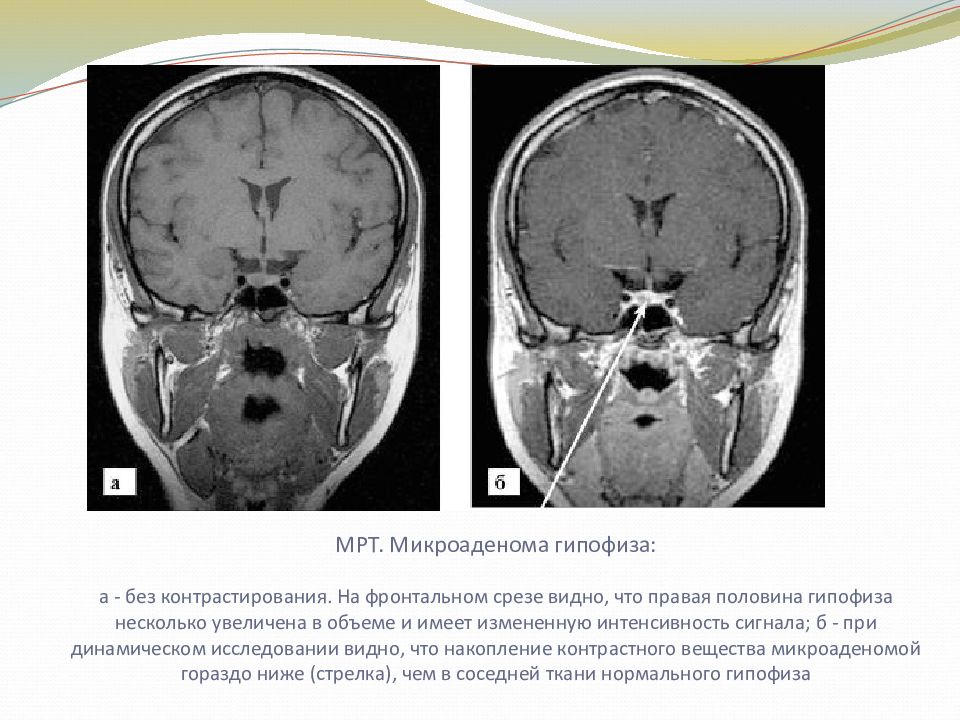
Ранняя диагностика кортикотропином
Ранняя диагностика кортикотропином имеет важное значение для эффективного лечения болезни Кушинга. Она включает следующие этапы:
- Биохимическое подтверждение эндогенного гиперкортизолизма
- Дифференциальная диагностика АКТГ-зависимого и АКТГ-независимого гиперкортизолизма
- Топическая диагностика источника гиперсекреции АКТГ
Для биохимической диагностики используются:
- Определение суточной экскреции свободного кортизола с мочой
- Ночной подавляющий тест с 1 мг дексаметазона
- Определение кортизола в слюне в 23:00
Для дифференциальной диагностики применяют:
- Определение АКТГ в плазме крови
- Большую дексаметазоновую пробу
- Стимуляционный тест с кортиколиберином
Методы топической диагностики кортикотропином
Для визуализации микроаденом гипофиза применяются следующие методы:
- Магнитно-резонансная томография (МРТ) гипофиза с контрастированием
- Компьютерная томография (КТ) гипофиза
- Селективный забор крови из нижних каменистых синусов
МРТ является наиболее информативным методом визуализации микроаденом. Она позволяет выявить опухоли размером от 2-3 мм. При отсутствии визуализации на МРТ проводится селективный забор крови из нижних каменистых синусов с определением градиента концентрации АКТГ.
Лечение кортикотропином
Основным методом лечения кортикотропином является транссфеноидальная аденомэктомия. При радикальном удалении микроаденомы эффективность операции достигает 80-90%.
При неэффективности хирургического лечения или рецидивах заболевания применяются:
- Повторное хирургическое вмешательство
- Лучевая терапия
- Медикаментозная терапия (ингибиторы стероидогенеза, антагонисты глюкокортикоидных рецепторов)
- Двусторонняя адреналэктомия
Таким образом, ранняя диагностика кортикотропином имеет ключевое значение для своевременного и эффективного лечения болезни Кушинга. Применение современных методов гормональной и топической диагностики позволяет выявлять микроаденомы гипофиза на ранних стадиях заболевания.
Городская клиническая больница им. Ф.И. Иноземцева
Надпочечники – парный орган, справа и слева они расположены над почками, лежат в забрюшинной клетчатке. Правый надпочечник треугольной формы, расположен над верхним полюсом правой почки, непосредственно примыкая к нижней полой вене. Левый надпочечник имеет полулунную форму, расположен частично над верхним полюсом левой почки, соприкасается с поджелудочной железой, селезенкой, кардиальной частью желудка. Кровоснабжаются надпочечники большим количеством артерий. Венозная кровь оттекает по центральной надпочечниковой вене (справа впадает непосредственно в нижнюю полую вену, слева – в левую почечную вену).
Гормоны надпочечников
В мозговом слое надпочечника вырабатываются:
- Адреналин – важный гормон в борьбе со стрессом. Активация данного гормона и его выработка увеличивается как при положительных эмоциях, так и стрессе, травмах. Под влиянием адреналина могут увеличиваться и расширяться зрачки, дыхание становится учащенным, увеличивается артериальное давление, ощущается прилив сил. Повышается сопротивляемость к болевым ощущениям.
- Норадреналин – гормон стресса, который считают предшественником адреналина. Оказывает меньшее воздействие на организм, участвует в регуляции артериального давления, что позволяет стимулировать работу сердечной мышцы
Корковое вещество надпочечников вырабатывает гормоны класса кортикостероидов, которые разделяют на три слоя: клубочковый, пучковый, сетчатая зона. Гормоны клубочковой зоны вырабатывают:
- Альдостерон – гормон отвечающий за обмен ионов калия и натрия в крови человека. Участвует в водно-солевом обмене, способствует увеличению циркуляции крови, повышает артериальное давление
- Кортикостерон – малоактивный гормон, участвует в водно-солевом балансе
- Дезоксикортикостерон – гормон, повышающий сопротивляемость в организме человека, придает силу мышцам и скелету, также регулирует водно-солевой баланс
Гормоны пучковой зоны надпочечников:
- Кортизол – гормон
сохраняющий энергетические ресурсы организма, участвует в углеводном обмене.
 Уровень кортизола часто подается колебаниям, так утром его намного больше чем
вечером
Уровень кортизола часто подается колебаниям, так утром его намного больше чем
вечером - Кортикостерон – (см. выше) также вырабатывается пучковой зоной
Гормоны сетчатой зоны:
- Андрогены – половые гормоны, влияющие на половые признаки: половое влечение, увеличение мышечной массы и силы, жировые отложения, уровень липидов и холестерина в крови
Исходя из вышеизложенного – гормоны надпочечников выполняют важную функцию в организме человека, их избыток либо дефицит может привести к нарушению во всем организме.
Болезни надпочечников можно разделить на патологию формы – опухоли, кисты и функции – альдостерома, кортикостерома, феохромоцитома, андростерома, эстрома. Помочь диагностировать заболевания надпочечников или выявить нарушения в их функциональности можно при помощи ряда обследований, которые назначает врач после собранного анамнеза. Для постановки диагноза врач определяет гормоны надпочечников, позволяющий выявить избыток или дефицит последних. При опухолях надпочечников основной скрининговый метод диагностики – УЗИ, однако более точную картину дает КТ или МРТ органов брюшной полости и забрюшинного пространства. Результаты обследования позволяют составить полную картину заболевания, определить причину, выявить те или иные нарушения в работе надпочечников и других органах и соответственно назначить лечение, которое может проводится как консервативным методом, так и оперативным вмешательством
Заболевания надпочечников:
Синдром Иценко-Кушинга – патологический симптомокомплекс, возникающий вследствие повышенного выделения опухолью из коры надпочечников гормона кортизола. Выработку кортизола и кортикостерона регулирует гипофиз путем выработки адренокортикотропного гормона. Деятельностью гипофиза управляют гормоны гипоталамуса – статины и либерины. Данная многоступенчатая регуляция необходима для обеспечения слаженности функций организма и обменных процессов, нарушение одного из звеньев может вызвать гиперсекрецию гормонов коры надпочечников, что приведет к развитию синдрома Иценко-Кушинга.
Синдром Конна (первичный гиперальдостеронизм, альдостерома) – симптомокомплекс, обусловленный большей продукцией альдостерона корой надпочечника. Причиной чаще всего является опухоль надпочечника, реже – гиперплазия клубочковой зоны коркового слоя. У больных уменьшается количество калия и увеличивается концентрация натрия в крови, из-за этого повышается артериальное давление.
Впервые синдром был описан ученым из Америки Конном в 1955 году, благодаря чему и получил свое название.
Симптомы: слабость, утомляемость, тахикардия, судороги, головная боль, жажда, парестезии конечностей, повышение артериального давления.
Синдром Конна
сопровождается признаками поражения сердца и сосудов, почек, мышечной ткани.
Артериальная гипертензия бывает злокачественной и устойчивой к гипотензивной
терапии.
Диагностика: исследование электролитов крови (высокий натрий, низкий калий в крови), увеличение уровня альдостерона в плазме, подсчет суточного диуреза, определение уровня ренина в крови, соотношение активности альдостерона плазмы и ренина, определение уровня альдостерона в суточной моче, КТ или МРТ органов брюшной полости – определение новообразований в надпочечниках.
Лечебные мероприятия направлены на коррекцию высокого артериального давления, метаболический расстройств, а также на предотвращение возможных осложнений, обусловленных высоким артериальным давлением и снижением калия в крови. Консервативная терапии радикально не способна улучшить состояния пациентов, полное выздоровление происходит только после оперативного удаления опухоли.
Феохромоцитома – гормонально активная опухоль, активно секретирующая адреналин и норадреналин. Феохромоцитома приводит к выбросу в кровь адреналина или норадреналина, которые приводят к развитию специфических нарушений у пациентов – стойкое кризовое повышение артериального давления (иногда более 200/100 мм.рт.ст.), не поддающееся гипотензивной терапии, учащенное сердцебиение. Чаще всего феохромоцитома представлена опухолью надпочечника. Диагностика основывается на лучевых и гормональных методах исследования. Лучевая диагностика: КТ или МРТ органов брюшной полости и забрюшинного пространства. Гормоны: производится определение уровня хромогранина А, АКТГ, альдостерона, ренина, кортизола крови, определение метанефринов, норметанефринов в суточной моче. Заподозрить феохромоцитому позволяет наличие образование в надпочечнике, повышение уровня метанефринов и норметанефринов в суточной моче. Основной метод лечения при феохромоцитоме – адреналэктомия с опухолью. Подготовке к операции уделяется отдельное внимание – задачами предоперационной подготовки пациентов с феохромоцитомой являются нормализация уровня артериального давления, устранение опасных его колебаний в течение суток, урежение сердечного ритма. В качестве основного препарата, используемого для подготовки к операции, используется доксазозин (кардура). Препарат назначается не менее, чем за 2 недели до планируемой операции. Метод доступа при оперативное лечении зависит от размеров опухоли, расположении, гормональной активности
В качестве основного препарата, используемого для подготовки к операции, используется доксазозин (кардура). Препарат назначается не менее, чем за 2 недели до планируемой операции. Метод доступа при оперативное лечении зависит от размеров опухоли, расположении, гормональной активности
Эстрома – опухоль коры надпочечника, продуцирующая в большом количестве женские половые гормоны – эстрогены. Как правило эти опухоли злокачественные. Эстромы встречаются очень редко, клинически они проявляются у лиц мужского пола импотенцией, двусторонней гинекомастией, фенимизацией телосложения, иногда гипотрофией яичек. У большинства больных наряду с феминизацией имеются признаки гиперсекрецией глюко- и минералокортикоидов. Поэтому диагностика заключается в исследовании специфических гормонов в крови, выполнение КТ или МРТ органов брюшной полости. Лечение оперативное – удаление опухоли надпочечника.
Андростерома – гормонально активная опухоль надпочечника, вырабатывающая в больших количествах мужские половые гормоны. Картина заболевания у женщин характеризуется расстройством менструального цикла (аменореей или олигоменорей), гипертрофией клитора, оволосением лица и тела, маскулинизацией фигуры, огрубением голоса, иногда облысением головы по мужскому типу. У отдельных больных могут наблюдаться гипертония и расстройства углеводного обмена в виде гипергликемии и умеренно выраженного повышения сахара в моче. У мужчин андростерома встречаются крайне редко и не проявляются какими-либо внешними признаками, поэтому диагноз у них устанавливают в поздней стадии заболевания. Диагностика заключается в выполнении КТ органов брюшной полости или МРТ органов брюшной полости, содержании высокого титра андрогенов и их метаболитов в суточной моче. Лечение – удаление опухоли надпочечника
Гормонально неактивная опухоль надпочечника – образование надпочечника, чаще всего носящая доброкачественный характер, не продуцирующая в высоком количестве гормоны. Данные опухоли надпочечника могут быть различного размера. Пациентам с гормонально неактивными образованиями в надпочечнике менее 3 см показано наблюдение, исследование гормонов в динамике. При размерах опухолей более 3 см, либо при росте опухоли более 1 см за год показано лечение оперативным путем. Диагностика включает в себя гормональные и биохимические анализы крови и мочи, КТ или МРТ органов брюшной полости.
Данные опухоли надпочечника могут быть различного размера. Пациентам с гормонально неактивными образованиями в надпочечнике менее 3 см показано наблюдение, исследование гормонов в динамике. При размерах опухолей более 3 см, либо при росте опухоли более 1 см за год показано лечение оперативным путем. Диагностика включает в себя гормональные и биохимические анализы крови и мочи, КТ или МРТ органов брюшной полости.
Хирургическое лечение заболеваний надпочечников:
В настоящее время операции на надпочечниках могут быть выполнены традиционным «открытым» доступом, либо с использованием высокотехнологических методов (эндоскопические операции). Стандартным доступом для адреналэктомии чаще всего являются люмботомия или лапаротомия – достаточно травматичные и трудоёмкие вмешательства. Так же могут использоваться такие доступы как чрездиафрагмальные, поддиафрагмальные, трансторакальные. Центр эндокринной хирургии широко использует эндоскопические методики в хирургии надпочечников, которые могут быть как лапароскопические, так и внебрюшинным доступом. Эндоскопические методики по сравнению с «открытой» операцией менее травматичные: при эндоскопических операциях 3 или 4 прокола по 1 см, пациенты меньше находятся на стационарном лечении, восстановительный сокращается в 2-3 раза. Вид оперативного вмешательства чаще всего определяется размером опухоли.
Кортикотропиномы. Ранняя диагностика и лечение (Лекция) | Семин
Аденомы гипофиза: так ли это часто?
Систематическое исследование пациентов, умерших от самых различных заболеваний, показывает наличие опухолей гипофиза в 6,8—22,6 % случаев. Фактически ни врачи, ни пациенты во многих случаях даже не подозревают об их существовании. Впервые на это обратил внимание Costello в 1929 г. Используя стандартные методы окраски аутопсий- ного материала, он разделил большинство опухолей на 4 группы: 1) хромофобные (52,8%), 2) напоминающие эозино
фильные (7,5%), 3) базофильные (27,2%), 4) смешанные (12,4%).
Это были первые шаги в изучении гипофизарных аденом. С появлением адекватных гистохимических методик хромофобные аденомы стали расценивать как секреторно-активные. Тем не менее высокая частота аденом на аутопсиях резко котрастирует с относительно низкой частотой опухолей, проявляющихся клинически.
Аденомы гипофиза в целом составляют 10 % внутричерепных новообразований. (В США опухоли мозга составляют 1,7 % всех опухолей.) Из аденом гипофиза пролактин (ПРЛ)-секретирующие встречаются с частотой 39 %, соматотропин (СТГ)-секретирующие — 38%, «гормональнонеактивные» (nonsecretory tumors)—21%, кортикотропиномы (аденомы, продуцирующие адренокортикотропный гормон — АКТГ) — 4 %.
Таким образом, аденомы гипофиза могут быть либо гормонально-активными, либо немыми (silent adenomas), что встречается нередко. До сих пор остается открытым вопрос, почему опухоли, продуцирующие гормоны, в том числе в культуре ткани, не дают клинической картины гормональной гиперпродукции. Возможно, в клетках гормонально-неактивных аденом имеются дефекты различных уровней синтеза и высвобождения гормонов, которые сами по себе трудно объяснимы.
Болезнь Кушинга (БК) и кортикотропиномы
Одним из нейроэндокринных заболеваний, возникающих из-за гиперсекреции АКТГ гормонально-активной аденомой гипофиза, является БК. Гиперсекреция АКТГ ведет к двусторонней гиперплазии коры надпочечников с гиперкортизолиз- мом. Эта болезнь была впервые описана Н. Cushing в 1912 и в 1932 гг. и впоследствии названа его именем. Н. Cushing указал на связь болезни с «minute» (мельчайших размеров) аденомами в 8 из 10 описанных случаев. При этом у 6 пациентов опухоли были образованы базофильными клетками, а у 2 — «недифференцированными». Тогда же появилось первое определение кортикотропиномы: это,. как правило, микроаденома (МА) в гипофизе нормальных (в большинстве случаев) размеров с гормональной гиперсекрецией. В настоящее время оно практически не изменилось.
По современным данным, аденомы гипофиза обнаруживаются у 60—90 % пациентов с БК, из них у 80—90 % — МА, т. е. их диаметр меньше 10 мм. Описаны также кортикотро-. пиномы диаметром 2 мм и менее. В 10 % случаев встречаются макроаденомы с увеличением турецкого седла и экстраселляр- ным распространением. Учитывая, что МА встречаются у подавляющего большинства пациентов с БК, а также то, что обнаружение кортикотропиномы на возможно ранней стадии является показателем качества диагностики, речь в основном пойдет о них.
е. их диаметр меньше 10 мм. Описаны также кортикотро-. пиномы диаметром 2 мм и менее. В 10 % случаев встречаются макроаденомы с увеличением турецкого седла и экстраселляр- ным распространением. Учитывая, что МА встречаются у подавляющего большинства пациентов с БК, а также то, что обнаружение кортикотропиномы на возможно ранней стадии является показателем качества диагностики, речь в основном пойдет о них.
Только ли БК?
В 1958 г. Nelson и соавт. сообщили о развившейся через 3 года после билатеральной адреналэктомии крупной АКТГ- секретирующей аденомы гипофиза, клинически проявляющейся гиперпигментацией, гипертонией, тошнотой, слабостью. «Классический» синдром Нельсона с резким снижением уровня кортизола и повышением концентрации АКТГ в плазме встречается в среднем у 30 % пациентов, перенесших билатеральную адреналэктомию.
Морфология
При окраске аутопсийного материала традиционными гистохимическими методами В. Б. Зайратьянц предложил разделить кортикотропиномы в зависимости от клеточного состава на следующие группы: базофильные (30 из 38 исследованных), хромофобные (2), эозинофильные (3), злокачественные (2).
Более чем в 81 % всех случаев наблюдается изменение клеточного состава передней доли с увеличением числа базофильных клеток. Поэтому мнение Н. Cushing о данной патологии как «питуитарном базофилизме» совершенно справедливо.
Таким образом, типичной находкой является микрокортикотропинома, состоящая из больших и средних размеров базофильных клеток овальной формы. Клетки окрашиваются в разной степени в реакциях PAS, ШИК и гематоксилином позитивно. Иммуногистохимически в секреторных гранулах выявляются АКТГ (в основном 4,5 кД) и связанные с ним пептиды: p-липотропин, а-меланоцитстимулирующий гормон (а-МСГ) и p-эндорфины, т. е. дериваты проопиомелЗно- кортина (ПОМК). При электронной микроскопии клетки кортикотропиномы данного типа имеют хорошо развитый шероховатый эндоплазматический ретикулум (ЭПР), выраженный комплекс Гольджи, миожестйо сферических секреторных гранул электронной плотности от 250 до 700 нм, часто выстроенных вдоль клеточной мембраны. Такие клетки обычно формируют узелковую массу, отличающуюся от нормальной ткани гипофиза.
Такие клетки обычно формируют узелковую массу, отличающуюся от нормальной ткани гипофиза.
Некоторые гормонально-активные кортикотропиномы образованы хромофобными клетками, которые содержат небольшое количество слабо PAS-позитивных гранул в цитоплазме. Изредка подобные клетки PAS-негативные. Тем не менее хромофобные опухоли содержат иммунореактивный АКТГ и связанные пептиды. Это показывает, что они также состоят из кортикотрофов или образовались из них. При изучении с помощью электронного микроскопа видны редкие гранулы, так что клетки хромофобных аденом выглядят «как бы менее дифференцированными» в сравнении с густо гранулированными базофильными кортикотрофами.
Немые (silent) кортикотропиномы представлены базофильными или хромофобными клетками с АКТГ и связанными пептидами. Однако какие-либо клинические или биохимические свидетельства повышенной секреции АКТГ отсутствуют. Во многих случаях немые кортикотропиномы морфологически ничем не отличаются от гормонально-активных. Тем не менее некоторые авторы обращают внимание на относительное увеличение числа и размеров лизосом клеток этих аденом, повышенную аутофагию или недоразвитый комплекс Гольджи, что предполагает дефекты синтеза и высвобождения гормонов. Другие кортикотрофы немых аденом не содержат микрофиламентов и имеют необычные каплевидные секреторные гранулы. Считается, что указанные морфологические типы клеток silent-кортикотропином представляют собой либо субклон типичных кортикотрофов, либо совершенно особый тип клеток.
Гиалин Crooke
Аденомы гипофиза при БК обычно окружены клетками с резкими гиалиновыми изменениями типа Crooke, описанными впервые в 1948 г. и представляющими собой аккумуляцию PAS-, гематоксилиннегативных гомогенных микрофиламентов 1-го типа. В самих кортикотрофах гиалин Crooke отсутствует либо крайне редок. Так как гиалиновые изменения связаны с высоким уровнем кортикостероидов в сыворотке крови, они не наблюдаются при синдроме Нельсона.
Кортикотропиномы развиваются не только в передней доле
- S. Lamberts и соавт., S. Stewen и соавт. указывают на возможность развития кортикотропином из двух источников:
- большая часть аденом развивается в передней доле и соответствует «классическому» описанию; 2) существуют также кортикотропиномы интермедианной (промежуточной) доли, содержащие так называемую «неопухолевую паренхиму». Под этим подразумевают аргирофильные нервные волокна, окрашивающиеся по Bodian — Grimelius. Они-то и натолкнули исследователей на мысль об особом происхождении данных аденом. A. McNicol критикует подобное разграничение опухолей, так как аргирофильные волокна содержатся и в аденомах передней доли гипофиза.
В отдельных случаях в интермедианной доле гипофиза встречаются множественные МА и/или гнезда гиперплазированных клеток. Интермедианные кортикотропиномы, как правило, резистентны к дексаметазону, уменьшают выделение АКТГ в ответ на бромкриптин и увеличивают его секрецию после стимуляции тиреотропин-рилизинг-гормоном.
- S. Lamberts и S. Stewen отмечают, что кортикотропиномы могут образовываться в задней доле, zona cystica, что, впрочем, бывает довольно редко.
Развитие кортикотропином в прямом смысле «где попало» можно объяснить обнаружением АКТГ практически во всех структурах головного мозга, что даже заставляет говорить о его нейротрансмиттерной функции. Вполне возможно, что АКТГ там синтезируется de novo in situ.
Патогенез БК •
В гипофизе человека в норме содержится 50 ЕД (250 мкг) АКТГ. Скорость его секреции 1—5 ЕД (5—25 мкг) в сутки. При БК клетки МА, как и нормальные кортикотрофы, секретируют АКТГ периодически (7—9 имп/3 ч). У здоровых лиц наименьший уровень АКТГ определяется в конце дня и непосредственно перед сном, наибольший — в 6—8 ч, в момент пробуждения. При состояниях, характеризующихся автономной секрецией АКТГ, его концентрация повышается во второй половине дня или в начале сна, т. е. также отмечается периодичность.
е. также отмечается периодичность.
В ответ на АКТГ-стимуляцию в коре надпочечников :екретируются глюкокортикоиды (ГК), которые по механизму обратной связи влияют на гипоталамус (так называемая «длинная петля» — «long-loop feedback»). Сам АКТГ также связан с гипоталамусом обратной связью («короткая петля» — «short-loop feedback»). Взаимодействие механизмов обратной связи, секреции кортикотропин-рилизинг-гормона (КРГ) гипоталамусом и контроль синтеза АКТГ и ГК нарушаются при БК. Отсутствие циркадных ритмов и бесконтрольная гиперсекреция АКТГ опухолью в условиях нарушения обратной связи вызывают гиперсекрецию кортизола с извращением ее ритма.
Интересными являются данные изучения преобразования ПОМК в кортикотропиномах человека (в основном радио- лигандными методами). В абсолютном большинстве аденом дериваты ПОМК идентичны таковым в нормальной ткани гипофиза, что говорит о ненарушенном процессе деградации ПОМК. В противоположность этому опухоли при эктопированном АКТГ-синдроме часто продуцируют аномальные фрагменты, такие как уЗ-МСГ, hp-MCr5-22, кортикотропин- подобный пептид промежуточной доли (в англоязычной литературе — CLIP — corticotropin like intermediary-lobe peptide). В некоторых эктопированных опухолях до 90% ПОМК превращается в CLIP, который является показателем степени нарушения преобразования ПОМК. Обилием фрагментов ПОМК, регулирующих пигментообразование, объясняется гиперпигментация при эктопированном АКТГ-синдроме.
При гиперкортизолизме происходит усиление глюконеогенеза, а синтезируемая глюкоза идет на образование жиров. Избыток ГК также тормозит синтез коллагенового и мукополисахаридного матрикса, угнетая процесс костеобразования, и вместе с усиленной резорбцией костной ткани ведет к остеопорозу.
В патогенезе БК имеет значение гиперсекреция адреналовых андрогенов (дегидроэпиандростерона, его сульфата и андростерона), которые конвертируются в тестостерон на периферии. Повышение концентрации андрогенов ведет к гирсутизму и дисменорее у женщин. Kurisaka полагает, что контролировать продукцию пептидов в кортикотрофах могут как андрогены, так и эстрогены. Он же продемонстрировал позитивную окраску эстрогеновых рецепторов в 25—35 % исследованных кортикотропином.
Kurisaka полагает, что контролировать продукцию пептидов в кортикотрофах могут как андрогены, так и эстрогены. Он же продемонстрировал позитивную окраску эстрогеновых рецепторов в 25—35 % исследованных кортикотропином.
Увеличение секреции пролактина также приводит к дисменорее. Интересен факт присутствия АКТГ и ПРЛ в одной МА. S. Lamberts и соавт. считают возможным происхождение подобных опухолей из интермедианной доли.
Уровень альдостеро’на обычно не меняется. Ренин-ангио- тензиновая система, как правило, интактна.
Механизмы развития кортикотропином
Н. Schulte обращает внимание на две из них: 1) поликлональный, в основе — аберрации обратной связи; 2) моноклональный, в основе — мутация в одной клетке, ведущая к «клональной экспансии» («clonal expansion»).
Никакой корреляции между клональным строением и клиническими проявлениями не выявлено.
Секреторная активность и клеточная дифференцировка определяются не только гипоталамическими рилизинг-гор- монами, но и локально продуцируемыми паракринными факторами, связанными с холинергической системой. Стимуляция холинорецепторов ведет к усилению выброса АКТГ. Подобный эффект вызывается стимуляцией а-адренорецепторов, в то время как 0-адреномиметические вещества ингибируют АКТГ. Биоаминэргическая регуляция секреции КРГ и АКТГ плохо изучена. Серотонин, например, как стимулирует, так и ингибирует синтез АКТГ в аденомах.
До сих пор не решен вопрос о том, возникает ли БК из-за первичного поражения ЦНС с гиперстимуляцией аденогипофиза КРГ или заболевание связано с первичной спонтанной кортикотропиномой.
Гипотезу гипоталамического происхождения БК подтверждают следующие факты:
- на аутопсии иногда находят поражения паравентрику- лярных и супраоптических ядер;
- нередко обнаруживают гиперплазию кортикотрофов без аденомы;
- концентрация АКТГ возрастает в ответ на введение КРГ;
- нарушение периодичности секреции СТГ и ПРЛ свиде
тельствует о гипоталамической стимуляции различных клеток передней доли; »
- рецидивы болезни после удаления МА также являются аргументами в пользу гипоталамической стимуляции.

Сторонники гипотезы первично гипофизарного происхождения МА обращают внимание на следующие моменты:
- высокую частоту гипофизарных МА и 2) на развитие вторичной надпочечниковой недостаточности вслед за селективной аденомэктомией с сохранением или повышением секреции других гормонов гипофиза у 80 % пациентов, что, по их мнению, говорит о первостепенной роли гипофизарных нарушений при БК.
Примечательно, что среди западных исследователей вторая гипотеза является более распространенной.
Как поставить диагноз?
Важным шагом в постановке диагноза является биохимическое подтверждение эндогенного гиперкортизолизма. Это означает необходимость исключения ятрогенного гиперкортизолизма, алкоголизма, нарушения функции почек, т. е. состояний, при которых нарушается «метаболизм стероидов» и развивается псевдосиндром Кушинга. Далее представляется целесообразным использовать следующий алгоритм (см. схему).
Алгоритм диагностики БК.
Упомянутые выше методики являются широко известными и подробное их описание здесь вряд ли целесообразно, за исключением БОИГ-метода, который пока не используется в клиниках нашей страны, но довольно широко распространен за рубежом.
Что такое БОИ Г?
Особое место в диагностике микрокортикотропином занимает билатеральное одновременное измерение уровня гормонов (БОИГ) в sinus petrosus inferior после стимуляции КРГ. Предварительные исследования позволяют говорить, что секретируемые гормоны из локализованных латерально МА выделяются преимущественно в ипсилатеральный нижний каменистый синус. Очевидно, что БОИГ может служить средством топической диагностики МА. Для катетеризации может быть использован чрескожный билатеральный феморальный доступ. АКТГ определяется радиолигандным методом, порог: 3—5 пг/мл. При этом 7 из 10 гистологически подтвержденных МА имеют повышенный уровень АКТГ в синусах, дренирующих пораженную сторону гипофиза (гипофизарный градиент АКТГ). БОИГ достоверно диагностирует МА в 86— 90 % случаев. При данной методике возможно также определение градиента ПРЛ. Н. Schulte даже делает вывод, что у всех пациентов с микрокортикотропиномой после введения КРГ следует ожидать градиента как АКТГ, так и ПРЛ в ипсилатеральных каменистых синусах. Как отмечают Т. Hawlet и соавт., иногда приходится сталкиваться с нетипичным строением каменистых синусов, что может служить причиной технических трудностей при исследовании. Эти авторы предлагают измерять градиент АКТГ, ПРЛ и ТТГ одновременно, так как при КРГ-стимуляции наблюдается мультигормональ- ный ответ. Данный эффект объясняется «паракринной акцией» кортикотрофов или вызванным КРГ возрастанием гипофизарного кровотока, ведущего к подмешиванию питуитарной венозной крови в нижний каменистый синус.
БОИГ достоверно диагностирует МА в 86— 90 % случаев. При данной методике возможно также определение градиента ПРЛ. Н. Schulte даже делает вывод, что у всех пациентов с микрокортикотропиномой после введения КРГ следует ожидать градиента как АКТГ, так и ПРЛ в ипсилатеральных каменистых синусах. Как отмечают Т. Hawlet и соавт., иногда приходится сталкиваться с нетипичным строением каменистых синусов, что может служить причиной технических трудностей при исследовании. Эти авторы предлагают измерять градиент АКТГ, ПРЛ и ТТГ одновременно, так как при КРГ-стимуляции наблюдается мультигормональ- ный ответ. Данный эффект объясняется «паракринной акцией» кортикотрофов или вызванным КРГ возрастанием гипофизарного кровотока, ведущего к подмешиванию питуитарной венозной крови в нижний каменистый синус.
Традиционная рентгенология и БК
Обычные снимки турецкого седла при БК, как правило, не выявляют патологию, за исключением 10 % пациентов с макроаденомами. Сопоставление количеств кортикотропином, подтвержденных на аутопсии, данными традиционных рентгенологических исследований (снимок черепа в боковой проекции или прицельный снимок турецкого седла), показывает, что эти методы эффективны только в 18 % случаев. Тем не менее о них не следует забывать совсем.
Диагностика БК и реформация в радиологии
В настоящее время использование динамической компьютерной томографии (КТ) позволяет распознавать МА в виде участка с пониженной плотностью в 50—60 % случаев. Основной недостаток КТ — низкая разрешающая способность, из-за чего 25— 30 % МА не диагностируются. В последнее время стали использовать высокоразрешающую КТ (тонкослойная техника) с толщиной среза 1,5 мм. Применение тонкослойной техники и динамической КТ с введением контраста помогает визуализировать мельчайшие поражения гипофиза и гипоталамуса.
Магнитно-резонансная томография (МРТ) является более чувствительной процедурой. МРТ обеспечивает визуализацию МА более чем в 80 % случаев, причем у 10 из 42 пациентов МА могут быть подтверждены только при помощи МРТ, так как она дает мультипланарный образ гипофиза. Дополнительное использование гадолиния повышает чувствительность метода, хотя возможны ложноотрицательные результаты. В ряде случаев не определяется локализация МА как при МРТ, так и при КТ. В целом оба метода диагностики эквивалентны по эффективности и дополняют друг друга.
Дополнительное использование гадолиния повышает чувствительность метода, хотя возможны ложноотрицательные результаты. В ряде случаев не определяется локализация МА как при МРТ, так и при КТ. В целом оба метода диагностики эквивалентны по эффективности и дополняют друг друга.
Таким образом, диагностика БК основывается на: I) оценке клинико-гормональных критериев; 2) данных МРТ и КТ; 3) результатах БОИГ (см. таблицу).
Заметим, что хиазмальный синдром и другие неврологи ческие расстройства из-за сдавления растущей опухольк соседних структур практически не встречается. Гораздо боль шее влияние вызывают гормональные эффекты.
Хирургическое лечение
За последние 15 лет были достигнуты определенные успех! в изучении гипофизарных гормонов, в диагностике адено» с помощью радиологических методов, включая КТ и МРТ. Вс, это позволяет обнаружить МА и, что самое главное, ради кально удалить опухоль, ликвидировать гормональный дисба ланс. Это делает хирургическое лечение БК основным и пато генетическим.
Преимущества и недостатки хирургического лечения Наиболее результативным методом удаления МА являете! транссфеноидальная микрохирургия (ТСХ). Впервые ТС) была предложена Schloffer в 1906 г. Н. Cushing разработав сублабиальный транссфеноидальный доступ с подслизиста резекцией носовой перегородки. Широкое применение в кли нической практике метод ТСХ получил благодаря J. Hard; и его ученику и последователю G. Guiot.
Преимущества ТСХ:
- подход физиологичен и безопасен, малотравматичен
- разрезы невидимы, нет косметических дефектов;
Клиническая картина БК, по данным Н. Im ига (Ed). The
pituitary gland.— N. Y.: Raven Press, 1985.— P. 441.
Симптомы | Часто- |
та, % | |
Общие: | |
ожирение | 85 |
гипертензия | 75 |
головная боль | 10 |
Поражения кожи: | |
гиперемия лица | 80 |
гирсутизм | 75 |
грибковые поражения кожи | 50 |
стрии | 50 |
акнэ | 35 |
кровоподтеки | 35 |
гиперпигментация | 5 |
Нейропсихические | 85 |
Дисфункция гонад: | |
дисменорея | 75 |
импотенция, снижение либидо | 65 |
Костно-мышечные: | |
остеопороз | 80 |
боли в спине | 65 |
слабость | 50 |
Метаболические: | |
нарушение толерантности к | |
глюкозе | 75 |
диабет | 20 |
нефролитиаз | 15 |
полиурия | 10 |
- хорошо переносится даже ослабленными и пожилыми пациентами;
- хорошая визуализация гипофиза и его поражений во время операции;
- декомпрессия турецкого седла, при этом если опухоль рецидивирует, она имеет тенденцию расти в основную пазуху, а не супраееллярно;
- довольно низкая частота осложнений и смертность.

Недостатки ТСХ:
- операционное поле ограниченных размеров;
- обычно не виден n. opticus;
- возможность перелома перфорированной пластинки решетчатой кости с последующим развитием назальной ликвореи;
- мешающие операции кровотечения из венозных синусов dura mater.
Из послеоперационных осложнений в литературе описываются: ликворея (1—8%), несахарный диабет через 3—6 дней после операции (48%) из-за повреждения задней доли во время вмешательства, менингит (0,1 %), синуситы, причем чаще после предшествующей радиотерапии, возникновение микотической аневризмы супраклиноидной порции внутренней сонной артерии как результат супраселлярной инфекции после ТСХ; паралич глазодвигательного нерва (0,1 %), перфорация носовой перегородки, абсцесс турецкого седла.
Смертность при ТСХ менее 3 %.
Результаты ТСХ. Селективная аденомэктомия в 74—96 % глучаев сопровождается быстрой ликвидацией гормональных нарушений (т. е. прекращением гиперсекреции АКТГ), восстановлением функции гипофиза в целом. Аналогичные данные получены Mayo Clinic: у пациентов, которым была произведена ТСХ, хорошие результаты наблюдаются у 90 % при условии, что МА была гистологически верифицирована. В слу- наях с гистологическим подтверждением длительная ремиссия достигается в 50 % случаев.
Десятилетний срок без рецидивов отмечается у 8—10% Зольных.
После ТСХ у 11 из 12 пациентов наблюдают транзиторную дторичную надпочечниковую недостаточность с симптомами истероидного изъятия». Примечательно, что:
- гиперкортизолизм из-за кортикотропиномы подавляет :екрецию АКТГ, СТГ, липотропина, подавление сохраняется 1екоторое время после ТСХ и исчезает постепенно у боль- цинства пациентов;
- после удаления кортикотропиномы отсутствуют призна- :и продолжающихся гипоталамических нарушений;
- время восстановления нормального кортизолового отве- ■а на АКТГ 1,5—24 мес, в среднем 14 мес.
Есть данные о супрессивном действии избытка ГК на ответ ТТГ и его нормализацию после ТСХ.
Таким образом, если в 1983 г. в США двусторонняя адреналэктомия оставалась методом выбора при лечении БК, то в настоящее время ТСХ — метод номер один.
Рецидивы БК после хирургического лечения
Несмотря на очевидные успехи ТСХ, у 20—25 % пациентов возникают рецидивы в течение 10 лет. По данным Вг. Guil- haume и соавт., рецидивы через 2—3 года имели место у 6 из 42 пациентов. Рецидивы связаны: с неполным удалением МА, со структурой аденомы: чаще рецидивируют интермедианные опухоли (их особенности см. в разделе «Морфология»).
В настоящее время в институте нейрохирургии им. Н. Н. Бурденко РАМН осуществляется лечение БК. Оперировано 20 больных с результатами, аналогичными описанным выше.
К сожалению, до последнего времени диагностика МА в нашей стране была недостаточной в связи с отсутствием адекватных радиолигандных методов и низкой разрешающей способностью имевшихся в наличии аппаратов КТ и МРТ. Некоторые положительные сдвиги в этой области способствовали более широкому применению хирургического лечения данной патологии в России.
Неинвазивные методы лечения
Помимо хирургического лечения, возможно применение радиотерапии. Традиционные методы дистанционной радиотерапии решают проблему снижения уровня АКТГ и кортизола только у 50 % больных, эффект не всегда длителен. Результативность повторного облучения низка, так как возникает радиорезистентность. В 1,7 % случаев наблюдаются осложнения: нарушение зрения, атрофия зрительного нерва. Т. Rahn и соавт. отметили 2-летнюю ремиссию у 85 % пациентов после стереотаксической радиохирургии. По более жестким критериям подобная ремиссия встречается только в 50 % случаев.
Наиболее результативным методом радиотерапии является протонное облучение гипофиза, так как протоны максимально поглощаются опухолевой тканью и практически не влияют на здоровую ткань железы. Особенности данного метода: 1) малый объем разрушаемой ткани; 2) следует учитывать топографоанатомические взаимоотношения структур селлярной области; 3) аденогипофиз в 3—5 раз менее чувствителен к радиотерапии, чем иные структуры ЦНС, а кортикотропиномы вообще наиболее радиорезистентные опухоли.
Показания к протонотерапии: МА с высокой патологической секрецией АКТГ без изменения формы и размеров седла; нарушения циркадных ритмов секреции АКТГ при отсутствии убедительных признаков МА.
Перед процедурой необходим дифференциальный диагноз с эктопированным АКТГ-синдромом.
У 85 % пациентов после лечения наблюдается полная или частичная ремиссия. Объективное улучшение состояния (снижение массы, нормализация циркадных ритмов секреции АКТГ) наступает через 6—8 мес. Можно утверждать, что протонотерапия дает низкий процент рецидивов и приводит к быстрому выздоровлению. В нашей стране на сегодняшний день «протонная гипофизэктомия» является, пожалуй, самым популярным из современных методов лечения БК. Разработки в этой области (Е. И. Марова) признаны многими ведущими эндокринологами.
ТСХ и радиотерапия дополняют друг друга. Недостаток селективной аденомэктомии — развитие рецидивов у 15 % больных и более. При совместном применении ТСХ и контактного облучения с использованием Au или Yt, вводимых в гипофиз транссфеноидально, рецидивы перестают быть острой проблемой: успех может быть достигнут в 77 % случаев. Однако лечение может осложниться гипопитуитаризмом.
Фармакотерапия
Фармакотерапия БК в настоящее время является наименее разработанным способом лечения данного заболевания. Вместе с тем совместное применение фармакологических препаратов и радиотерапии довольно эффективно. Так, хлодитан, снижая уровень ГК в плазме крови через механизм обратной связи, увеличивает секрецию АКТГ кортикотропиномами и повышает их чувствительность к облучению (так как при гиперфункции чувствительность к радиации возрастает). Рекомендуется назначать хлодитан в течение 2 мес до облучения и 2 мес после облучения.
В последнее время для лечения БК предлагается октреотид (SMS-201—995) — синтетический аналог соматостатина. На сегодняшний день зарегистрирован лишь один случай успешного лечения БК октреотидом. Гипотетически октреотид способен редуцировать биологически активную форму АКТГ или превращать ее в менее активную форму.
Другие гормоны и препараты также могут влиять на кортикотропиномы, например in vitro прямой ингибирующий эффект дают ципрогептадин, бромкриптин (только в случаях со смешанными АКТГ и ПРЛ-секретирующими МА), допамин, некоторые а-адренергические препараты. Ингибиторы стероидогенеза, такие как метирапон, амнноглутамид, уменьшают секрецию кортизола надпочечниками. Перечисленные препараты используются и в нашей стране в качестве дополнительной терапии при недостаточной эффективности протоно- терапии или рецидивах МА.
В заключение отметим, что ни один из упомянутых препаратов не нашел широкого применения для лечения БК и если фармакотерапия используется, то только в комбинации с другими более эффективными радиологическими и хирургическими методами, описанными в данной статье.
1. Марова Е. И., Бухман А. И., Кирпатовская Л. Е. // Пробл. эндокринол.— 1986.— Т. 32, № 6.— С. 66—71.
2. Марова Е. И., Старкова Н. Т., Кирпатовская Л. Е. // Мед. радиол.— 1987.— Т. 32, № 8.— С. 42—49.
3. Опухоли гипофиза и хиазмально-селлярной области / Под ред. Б. А. Самотокина, В. А. Хилько.— Л., 1985.
4. Синдром Иценко — Кушинга / Под ред. В. Г. Баранова.— Л., 1988.
5. Теппермен Дж., Теппермен X. Физиология обмена веществ и эндокринной системы: Пер. с англ.— М., 1989.
6. Allolio В., Winkelmann U7., Schulte Н. М. // J. endocr. Invest.— 1991,— Vol. 14, N 2,— Suppl. 1,— P. 86.
7. Bachelot I., Fabre M., Bessac L. et al. // Ibid.— P. 112. Bertagna X., De Keyzer Y. // Molecular and Clinical Advances in Pituitary Disorders / Eds. Sh. Melmed, R. J. Robbins.— Boston, 1991,— P. 3—13.
Bachelot I., Fabre M., Bessac L. et al. // Ibid.— P. 112. Bertagna X., De Keyzer Y. // Molecular and Clinical Advances in Pituitary Disorders / Eds. Sh. Melmed, R. J. Robbins.— Boston, 1991,— P. 3—13.
8. Bigos S. Th., Somma M., Rasio Eu. et al. // J. clin. Endocr.— 1980,— Vol. 50,— P. 348—354.
9. Bochicchio D., Ambrosi B., Ferrario R. et al. // J. endocr. Invest.— 1991.— Vol. 14, N 2,— Suppl. 1.— P. 37.
10. Boggan /. E., Tyrrell J. B., Wilson С. B. // J. Neurosurg.— 1983,- Vol. 59.— P. 195-200.
11. Bonneville J. F., Cattin F., Gorczyca W., Hardy J. // J. endocr. Invest.— 1991.— Vol. 14, N 2,— Suppl. 1,— P. 40.
12. Burch W. 11 New Engl. J. Med — 1983,— Vol. 308, N 2,— P. 103—104.
13. Burke C. W., Tadams С. B., Esiri M. M., Bevan J. C. // Clin. Endocr. (Oxf.).— 1990.- Vol. 33,- P. 525-537.
14. Candrina R.. Galli G., Bollati A. // J. Neurol. Neurosurg.
15. Psychiat.— 1988,— Vol. 51, N 7,— P. 1005—1006.
16. Clark J. D. A., Wheatley T., Stewart S., Edvards О. M. // Ibid.- 1987,- Vol. 50, N 8 — P. 1079-1080.
17. Colombo P., Amdrosi B., Bochicchio D. et al. // J. endocr. Invest.— 1991.— Vol. 14, N 2.— Suppl. 1.— P. 78. Denef C. // Ibid.- P. 5.
14, N 2.— Suppl. 1.— P. 78. Denef C. // Ibid.- P. 5.
18. Fink U., Fink В. K-, Oecklen R. 11 Ibid.— P. 13.
19. Fitzgerald P. A., Aron D. C., Findling J. W. et al. // J. clin. Endocr.— 1986.— Vol. 54.— P. 413—423.
20. Gandon J. // Advanac. in Biosci.— 1988.— Vol. 69.— P. 38. Giovanelli A., Losa M., Baiguini M., Ducati A. // J. endocr. Invest.— 1991.— Vol. 14, N 2.— Suppl. 1.— P. 14.
21. Graziano E., Chiarini V., Cremonini N. et al. // Ibid.— P. 122. Grigsby P. W., Simpson J. R., Emami B. N. et al. // Int. J.
22. Radiat. Oncol. Biol. Phys.— 1989.— Vol. 16, N 6.— P. 1411 — 1417.
23. Guilhaume Br., Bertagna X., Thomsen M. et al. // J. clin. Endocr.— 1988 — Vol. 66, N 5.— P. 1056-1064.
24. Hawlet T. A., McNally H. G.. Bolia A. // J. endocr. Invest.— 1991,— Vol. 14, N 2.— Suppl. I.— P. 38.
25. Je/fcoate W. J. 11 Brit. med. J.— 1988,—Vol. 296, N 6617.— P. 227—228.
26. Kirpatovskaja L. E., Marova E. I. // J. endocr. Invest.— 1991.— Vol. 14, N 2,— Suppl. I.— P. 129.
27. Lamberts S. W. J., de Lange S. A., Stefanko S. Z. // J. clin. Endocr.— 1982.— Vol. 54,— P. 286—291.
28. Lamberts S. W. J., Stefanco S. Z. // Advanc. in Biosci.— 1988.— Vol. 69.— P. 341—348.
Lamberts S. W. J., Stefanco S. Z. // Advanc. in Biosci.— 1988.— Vol. 69.— P. 341—348.
29. Laws E. R. // Endocr. Metab. Clin. N. Amer.— 1987.— Vol. 16, N 3.— P. 647—663.
30. Loli P., Scialfa G., Boccardi E. et al. // J. endocr. Invest.— 1991,— Vol. 14, N 2,— Suppl. 1.— P. 85.
31. Lorcy Y. 11 Ibid.— P. 121 — 122.
32. Mampalan T. J., Tyrrell J. B., Wilson С. B. // Ann. intern. Med.— 1988,—Vol. 109.—P. 487—493.
33. McCance D. R., Fannin T. F., Gordon D. S. et al. // J. endocr. Invest.— 1991,— Vol. 14, N 2.— Suppl. 1,— P. 11.
34. Melby J. С. II Ann. intern. Med.— 1988.— Vol. 109, N 6.— P. 445—446.
35. Mohr G. II Canad. J. neurol. Sci.— 1990.— Vol. 17, N 1.— P. 62—68.
36. Molitch M. E. II The Pituitary Adenoma / Eds. K. D. Post et al.— New York; London, 1980,— P. 119—139.
37. Nicholson M. W., Doo G., Schroffner W. // Hawaii med. J.— Vol. 48, N 2,— P. 12—15.
38. Oldfield E. N.. Chrousos G. P., Schulte H. M. et al. // New EngL J. Med.— 1985.— Vol. 312.— P. 100—103.
39. Onishi H., Но H., Kuroda E. et al. // Surg. Neurol.— 1989.— Vol. 31, N 2 — P. 149—154.
// Surg. Neurol.— 1989.— Vol. 31, N 2 — P. 149—154.
40. Rahn T., Thoren M., Werner S. // J. endocr. Invest.— 1991.— Vol. 14, N 2,— Suppl. 1,— P. 15.
41. Reichlin S. II The Pituitary Adenoma / Eds. K. D. Post et al.— New York; London, 1980.— P. 29—45.
42. Reichlin S. // J. endocr. Invest.— 1991.— Vol. 14, N 2.— Suppl. 1.— P. 3.
43. Roger P., Tabarin A., Corcuff J. B., Navarranne A. // Ibid.— P. 84.
44. Salassa R. M., Laws E. R., Carpenter P. C., Northcut R. C. // Mayo Clin. Proc.— 1978.— Vol. 53.— P. 24— 28.
45. Schulte H. M., Allolio B., Gunter R. II/. et al. // Advanc. In Biosci.— 1988,—Vol. 69,— P. 363—366.
46. Schulte H. M., Allolio B., Doppman J. L., Oldfield E. H. // J. endocr. Invest.— 1991.— Vol. 14, N 2.— Suppl. 1.— P. 12.
47. Schulte H. M„ Oldfield E. H„ Allolio B. et al. // Ibid.- Р. 33.
48. Suda T., Demura H., Demura R. et al. // J. clin. Endocr.— 1980 — Vol. 51.— P. 1048-1053.
49. Tindall G. T., Herring C. J., Clark R. V. et al. // J. Neurosurg.— Vol. 72, N 3.— P. 363—369.
50. Tyrrell J. B., Brooks R. M., Fitzgerald P. A., Wilson С. B. // New Engl. J. Med.— 1978,— Vol. 298.— P. 753—758.
B., Brooks R. M., Fitzgerald P. A., Wilson С. B. // New Engl. J. Med.— 1978,— Vol. 298.— P. 753—758.
51. Woodhouse N. J. Y., Dagogo-Jack S., Ahmed M. // J. endocr. Invest.—1991,—Vol. 14, N 2.—Suppl. 1.—P. 121.
52. Zancaner F., Griner A. C., Picozzi P. et al. // Ibid.— P. 125.
53. Zimmerman R. M. // Semin, in Roentgenol.— 1990.— Vol. 25, N 2,— P. 147—197.
Нейроэндокринные опухоли негипофизарной локализации, продуцирующие АКТГ: клинические, морфологические, иммуногистохимические характеристики
На правах рукописи
Воронкова Ия Александровна
НЕЙРОЭНДОКРИННЫЕ ОПУХОЛИ НЕГИПОФИЗАРНОЙ ЛОКАЛИЗАЦИИ, ПРОДУЦИРУЮЩИЕ АКТГ: КЛИНИЧЕСКИЕ, МОРФОЛОГИЧЕСКИЕ, ИММУНОГИСТОХИМИЧЕСКИЕ ХАРАКТЕРИСТИКИ
14.01.02 — эндокринология 14.03.02 — патологическая анатомия
Автореферат диссертации на соискание ученой степени кандидата медицинских наук
9 ЯНВ 2Щ
Москва-2013
005544296
Работа выполнена в Федеральном государственном бюджетном учреждении «Эндокринологический научный цент» Министерства Здравоохранения Российской Федерации (директор — академик РАН и РАМН, профессор, доктор медицинских наук Дедов Иван Иванович)
Научные руководители:
Марова Евгения Ивановна
доктор медицинских наук, профессор
Гуревич Лариса Евсеевна
доктор биологических наук, профессор
Официальные оппоненты: Астафьева Людмила Игоревна
доктор медицинских наук, старший научный сотрудник VIII нейрохирургического отделения НИИ нейрохирургии им. H.H. Бурденко РАМН
Делекторская Вера Владимировна
доктор медицинских наук, заведующая лабораторией гистохимии и электронной микроскопии ФГБУ «Российский онкологический научный центр» им. H.H. Блохина РАМН
H.H. Блохина РАМН
Ведущая организация:
Государственное бюджетное образовательное учреждение высшего профессионального образования Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации.
Защита диссертации состоится « »_2014 года в _ часов на заседании
Диссертационного Совета Д 208.126.01 в ФГБУ «Эндокринологический научный центр» Министерства Здравоохранения Российской Федерации по адресу: 117036, Москва, ул. Дмитрия Ульянова, д. 11.
С диссертацией можно ознакомиться в библиотеке Федерального государственного бюджетного учреждения «Эндокринологический научный цент» Министерства Здравоохранения Российской Федерации.
Автореферат разослан « »_2013 года
Ученый секретарь Диссертационного Совета, доктор медицинских наук
Суркова Е.В.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Термин «Нейроэндокринные опухоли» (НЭО) объединяет гетерогенную группу новообразований из клеток нейроэндокринной системы.
Нейроэндокринные опухоли являются редкими заболеваниями, однако в последнее время во всем мире отмечено значительное увеличение количества пациентов с этой патологией (в 1973 — 1,09 случая на 100000 населения, а в 2004 уже 5, 25 на 100000) (Yao James С., 2008). Особое место в этой группе новообразований занимают «функционирующие» НЭО, проявляющиеся яркой клинической симптоматикой, которая обусловлена повышенной продукцией того или иного гормона.
Данная работа посвящена проблеме НЭО, сопровождающихся клиникой гиперкортицизма, связанной с избыточной секрецией клетками опухоли адренокортикотропного гормона (АКТГ), про-АКТГ или кортикотропинрелизинг гормона (КРГ). Данная патология очень редка -всего 4-12 случаев на 10 млн. населения (Марова Е.И., 2002; Бритвин Т.А.,2003; Kola Blerina, 2008). Тяжесть состояния пациентов, обусловленная широким спектром действия на различные органы и системы избытка кортизола, вырабатываемого под действием усиленной стимуляции коркового слоя надпочечника пептидами, секретируемыми клетками НЭО, зачастую вводит в заблуждение специалистов. Средний срок от первого обращения до верификации АКТГ-эктопического синдрома (АКТГ-ЭС) составляет 5-7 лет. Но и после постановки диагноза и установления первичного очага локализации НЭО, продуцирующей АКТГ, возникает множество вопросов по ведению данных пациентов.
Средний срок от первого обращения до верификации АКТГ-эктопического синдрома (АКТГ-ЭС) составляет 5-7 лет. Но и после постановки диагноза и установления первичного очага локализации НЭО, продуцирующей АКТГ, возникает множество вопросов по ведению данных пациентов.
В настоящее время в диагностике и лечении пациентов с АКТГ-секретирующими НЭО участвуют врачи многих специальностей, что диктует необходимость мультидисциплинарного подхода к изучению этой проблемы.
Учитывая все сказанное, изучение всех клинических и морфологических аспектов данной патологии является необходимым условием для выработки алгоритма своевременной диагностики и успешного ведения пациентов с НЭО внегипофизарной локализации, продуцирующих АКТГ.
Цель исследования
Изучить клинические, морфологические, иммунофенотипеческие особенности АКТГ-продуцирующих НЭО внегипофизарного происхождения, определить критерии оценки злокачественного потенциала и прогноза
данных опухолей и разработать тактику послеоперационного ведения пациентов.
Задачи исследования
1. Изучить клинические и лабораторные характеристики больных с АКТГ- эктопированным синдромом.
2. Проанализировать морфологические особенности НЭО с АКТГ-эктопированным синдромом.
3. С помощью иммуногистохимического метода исследовать экспрессию общих нейроэндокринных маркеров: хромогранина А (ХрА) (маркер специфических эндокринных гранул), синаптофизина (маркер мелких везикул с нейротрансмитгерами), СБ 56 (мембранный гликопротеид нейроадгезии).
4. Установить характер гормональной активности АКТГ-продуцирующих НЭО с помощью антител к следующим гормонам: адренокортикотропному (АКТГ), кортикотропинрелизинг гормону (КРГ), пролактину (ПРЛ), соматотропному (СТГ), лютеинизирующему (ЛГ) и фолликулстимулирующему (ФСГ), паратиреоидному гормону (ПТГ) и кальците нину.
5. Изучить особенности иммунофенотипа НЭО с АКТГ-ЭС, которые характеризуют злокачественный потенциал этих опухолей (пролиферативную активность опухолевых клеток — индекс метки К>67, экспрессию цитокератина-19 — белка входящего в состав промежуточных микрофиламентов цитоскелета) и выработать на этом основании критерии прогноза клинического течения АКТГ-ЭС.
6. Изучить особенности экспрессии рецепторов к соматостатину (РССТ) в АКТГ-продуцирующих НЭО.
Материалы и методы исследования
Материалом исследования послужили истории болезней 47 пациентов с АКТГ-ЭС, наблюдавшихся в ФГБУ «Эндокринологический научный цент» Министерства Здравоохранения Российской Федерации (директор -академик РАН и РАМН, профессор, доктор медицинских наук Дедов Иван Иванович) в период с 2000 по 2012 годы.
Обследование данных больных проводилось на базе отделения нейроэндокринологии и остеопатий ФГБУ «Эндокринологический научный центр» МЗ РФ (зав.отдел. — д.м.н., проф. Рожинская Л.Я.). Хирургическое удаление НЭО, продуцирующей АКТГ, было выполнено 40 пациентам, с последующим морфологическим исследованием удаленной ткани.
Период наблюдения пациентов после хирургического вмешательства составил от 1 года до 11лет.
Гормональное обследование и проведение стимуляционных тестов.
Исследования гормонов в крови и в суточной моче проведены в гормональной лаборатории ФГБУ «Эндокринологический научный центр» МЗ РФ (руководитель д.м.н., профессор Гончаров Н.П.). Определение уровня калия крови выполнено в биохимической лаборатории ФГБУ ЭНЦ (руководитель Ильин А.В.) на аппарате Architect plus.
С целью подтверждения АКТГ-зависимого гиперкортицизма был исследован суточный ритм секреции АКТГ в цельной крови с EDTA и кортизола в сыворотке крови в 8.00 и 23.00 часа на иммунохемилюминесцентном анализаторе Vitros 3600. Избыточными уровнями АКТГ считали выше 66,0 пг/мл в 8.00 и 30,0 пг/мл в 23.00 часа, кортизола — выше 626,0 нмоль/л в 8.00 и 270 нмоль/л в 23.00 часа.
Определение уровня свободного кортизола в слюне и моче производилось на автоматическом элекгрохемшломинесцентном анализаторе Cobas Е601 («ROCHE»). В пользу гиперкортицизма свидетельствовал уровень кортизола в слюне вечером более 9,4 нмоль/л. Избыточным уровнем свободного кортизола в моче считали уровень, превышающий 413 нмоль/ сутки. Определение уровней тропных гормонов гипофиза и других биологически активных веществ проводилось на аппарате Vitros 3600.
Определение уровней тропных гормонов гипофиза и других биологически активных веществ проводилось на аппарате Vitros 3600.
Малую пробу с дексаметазоном выполняли для подтверждения эндогенного гиперкортицизма. Далее проводили дифференциальную диагностику АКТГ-ЭС и болезни Иценко-Кушинга. С этой целью выполняли большую пробу с дексаметазоном, периферический тест с десмопрессином (11 пациентов) и селективный забор крови из нижних каменистых синусов со стимуляцией десмопрессином и оценкой градиента пролактина (21 случай).
Визуализационные методы исследования
Определение локализации АКТГ-секретирующих опухолей проходило в отделе лучевой диагностики ФГБУ «Эндокринологический научный центр» МЗ РФ (руководитель д.м.н. Ремизов О.В.). Пациентам выполняли мультиспиральную компьютерную томографию (МСКТ) органов грудной клетки и/или органов брюшной полости с контрастированием.
Хирургическое лечение
Пациентам с АКТГ-эктопическими НЭО легких производили лобэктомию или резекцию доли, в которой находилось новообразование, в хирургическом торакальном отделении Национального Медико-хирургического центра им. Н. И. Пирогова (руководитель д.м.н., профессор
Аблицов А.Ю.). Пациентке с НЭО левого надпочечника (феохромоцитома) выполнили адреналэктомию, пациенткам с НЭО, локализовавшимися в желудочно-кишечном тракте, провели гемиколэктомии, больным с опухолями тимуса — удаление новообразований переднего средостения в отделении эндокринной хирургии ФГБУ «Эндокринологический научный центр» МЗ РФ (зав. отдел, д.м.н., профессор Кузнецов Н.С.) и на базе отделения торакальной онкологии торакоабдоминального отдела Российского Онкологического Научного Центра им. H.H. Блохина (руководитель д.м.н., проф. Полоцкий Б.Е.).
Морфологическое исследование.
Морфологические исследования проведены в отделении патоморфологии ФГБУ «Эндокринологический научный центр» МЗ РФ (зав.отдел Молчков Р.В.) и на базе отделения патологической анатомии ГБУЗ МО «Московский областной научно-исследовательский клинический институт им М. Ф. Владимирского» (рук.отд. д.м.н., проф. Казанцева И.А.). Морфологический анализ операционного материала включал гистологический и иммуногистохимический методы исследования.
Ф. Владимирского» (рук.отд. д.м.н., проф. Казанцева И.А.). Морфологический анализ операционного материала включал гистологический и иммуногистохимический методы исследования.
Операционный материал фиксировали в 10% растворе формалина, затем заливали в парафин по обычной методике.
Серийные срезы толщиной 3-5 мкм депарафинировали по стандартной схеме и окрашивали гематоксилином и эозином.
Морфологическая верификация диагноза НЭО легких и бронхов, вилочковой железы проведена в соответствии с гистологической классификацией ВОЗ 2004 г., желудочно-кишечного тракта в соответствии с классификацией ВОЗ 2010г.
Иммуногистохимическое (ИГХ) исследование выполнили на операционном материале 40 пациентов. Характеристика использованных антител приведена в таблице 1. Использовались антитела к общим нейроэндокринным маркерам (хромагранину A, CD56, синаптофизину), к тропным гомонам гипофиза (АКТГ, СТГ, ПРЛ, ЛГ, ФСГ) и гормонам, участвующим в фосфорно-кальциевом обмене (ПТГ и капьцитонину), а также к КРГ (новообразования, экспрессирующие КРГ включены в исследование ретроспективно (Лапшина A.M., 2009)), маркеру ядер пролиферирующих клеток Ki-67, цитокератину-19 и рецепторам к соматостатину (РССТ 1-5).
Антитело характеристика Фирма производитель разведение Положительный контроль
АКТГ Мы ши ное/моноклонап ьное NovoCastra 1:200 Гипофиз
КРГ Мышиное/моноклонал ьное ABD serotec 1:100 Гипофиз
ПРЛ Мы шиное/моноклональное Dako 1:300 Гипофиз
СТГ Мышиное/моноклональное Dako 1:400 Гипофиз
ЛГ Мы ш иное/мо но кю нач ьное Dako 1:50 Гипофиз
ФСГ Мы ши ное/моноклонал ьное Dab 1:50 Гипофиз
Кальцитонин МышиноеМоликлональное Dako 1:5000 Медул1ярный рак щитовидной железы
ПТГ Мы шиное/моноклональное Novo Castra 1:200 Аденома окоющитовидной железы
КІ-67 Мышиное/моноклональное Dako 1:100 Лимфатический узел
Синаптофизин Мышиное/моноклональное Dako 1:20 Мозговой слой надпочечника
ХрА Мыишное/моноклональное Dako 1:100 Мозговой слой надпочечника
Цитокератин-19 Мышиное/моноклональное Dako 1:50 Бронхиальный эпителий
РССТ1 Кроли ч ье/поликл опальное Gramsch laboratories 1:5000 Островковые клетки поджелудочной железы
РССТ2 Кроличье/моноклона! ьное Epitomics 1:200 Островковые клетки поджелудочной железы
РССТЗ Кроличье/поликлональное Noxus biological 1:4000 Островковые клетки поджелудочной железы
РССТ4 Крол и ч ьеМ оли клона. 4 ьное Gramsch laboratories 1:1000 Островковые клетки поджелудочной железы
4 ьное Gramsch laboratories 1:1000 Островковые клетки поджелудочной железы
РССТ5 Кроли ч ье/моноклональное Epitomics 1:200 Островковые клетки поджелудочной железы
Оценка экспрессии маркеров.
Экспрессия цитоплазматических маркеров ХрА, Синаптофизина, АКТГ, КРГ, СТГ, ПРЛ, ЛГ, ФСГ, кальцитонина, ЦК 19, мембранного маркера CD56 проводилась полуколичественным методом: 1«+» окрашивание единичных клеток (менее 30% клеток опухоли), 2«+» — 3060% клеток опухоли, 3«+» — 60-90% , 4 «+» — более 90% клеток НЭО.
Индекс метки Ki-67 (для оценки пролиферативной активности клеток) рассчитывался по формуле: среднее число меченых ядер на 100 опухолевых клеток, которое вычисляется при просчете 2000 клеток опухоли, с обязательным учетом участков максимальной экспрессии маркера («горячих точек»).
Оценка экспрессии рецепторов к соматостатину в опухолевых клетках проводилась по шкале, предложенной Marco Volante и соавт.: 0 баллов -отсутствие экспрессии, 1балл — только цитоплазматическое окрашивание, 2
7
балла- полное или частичное окрашивание мембраны до 50% опухолевых клеток, независимо от наличия цитоплазматического и 3 балла — полное мембранное окрашивание более 50% опухолевых клеток, независимо от наличия цитоплазматического. Положительной следует считать только экспрессию с интенсивностью 2 и 3 балла. (Marco Volante, 2007).
Статистическая обработка полученных результатов выполнена с помощью программы Microsoft Office Excel 2003, STATISTICA for Windows v.6.0. и статистической программы R. Описание количественных данных представлено в виде среднего (М) и стандартного отклонения (S), медианы (Me), моды (Mo) и квартилей (25 и 75 процентили, Q25-75). Представление качественных признаков выполнено в виде долей. Сравнительный анализ двух независимых групп проведен по количественному признаку с помощью критерия Манна-Уитни, по качественному признаку — с использованием двустороннего точного критерия Фишера, нескольких групп с помощью Н-критерия Крускала-Уоллиса. Взаимосвязь изученных признаков определена с помощью коэффициента корреляции Спирмена (rs). Прогнозирование рисков выполнено с помощью регрессии Кокса.
Взаимосвязь изученных признаков определена с помощью коэффициента корреляции Спирмена (rs). Прогнозирование рисков выполнено с помощью регрессии Кокса.
Научная новизна
Впервые выполнена комплексная клиническо-морфологическия и иммуногистохимическая характеристика нейроэндокринных опухолей, продуцирующих АКТГ. Получены данные о наиболее информативных маркерах для прогнозирования клинического течения АКТГ-секретирующих нейроэндокринных опухолей.
Практическая значимость
В работе показаны наиболее чувствительные фармакологические тесты для диагностики АКТГ-ЭС. Выявлено, что часть НЭО с АКТГ-ЭС являются мультигормональными и способны продуцировать сразу несколько гормонов. Исследован статус экспрессии рецепторов к соматостатину 1-5 подтипа в НЭО, продуцирующих АКТГ, что дает возможность рассмотрения вопроса о применении биотерапии для лечения данной группы пациентов. Определены морфологические критерии оценки экспрессии рецепторов соматостатина при проведении иммуногистохимического исследования НЭО, секретирующих АКТГ.
Основные положения, выносимые на защиту 1. АКТГ-ЭС — заболевание возникающее у лиц наиболее трудоспособного возраста, протекающее как с нарастанием симптомов гиперкортицизма, так и в ряде случаев циклически, а в
некоторых случаях сочетающееся с клиникой карциноидного синдрома.
2. НЭО с эктопической секрецией АКТГ и/или КРГ вариабельны по локализации, морфологическим особенностям, характеристикам их иммунофенотипа и гормональной продукции, а часть из них обладает способностью к мультигормональной активности.
3. НЭО с АКТГ-ЭС в трети случаев дают метастазы как региональные, так и отдаленные.
4. Факторами неблагоприятного прогноза АКТГ-ЭС являются высокий индекс пролиферации Ki-67 и локализация первичного очага в тимусе.
5. Наличие рецепторов к соматостатину в НЭО, секретирующих АКТГ, дает возможность рассмотрения вопроса о применении биотерапии для лечения данной группы пациентов.
Апробация работы и публикации
Апробация диссертации состоялась на межотделенческой научной конференции в ФГБУ «Эндокринологический научный центр» МЗ РФ 21 ноября 2013 года (протокол №10).
Результаты исследования доложены на Конгрессе Европейской Нейроэндокринологической Ассоциации (2010 г., Германия, Берлин), на 9 ежегодной Европейской конференции посвященной НЭО (Дания, Копенгаген, 2012), на 25 Европейском Конгрессе патологов (Португалия, Лиссабон, 2013).
По теме диссертации опубликовано 10 печатных работ, в том числе 3 в журналах, которые включены в перечень российских рецензируемых научных журналов и изданий для опубликования основных научных результатов диссертаций и 1 в зарубежном научном издании. Результаты исследования внедрены в клиническую практику отделения нейроэндокринологии и остеопатий и отделения патоморфологии ФГБУ «Эндокринологический научный центр» МЗ РФ.
Объем и структура диссертации
Диссертация изложена на 150 страницах, иллюстрирована 13 таблицами и 34 рисунками, состоит из введения, обзора литературы, 6 основных глав, заключения, выводов, практических рекомендаций и списка литературы, включающего 18 отечественных и 114 зарубежных источников.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Клинико-лабораторная характеристика пациентов с АКТГ-эктопическим синдромом
Клинические проявления АКТГ-ЭС
В исследование было включено 47 пациентов с АКТГ-ЭС, из них 29 женщин и 18 мужчин (соотношение м/ж = 1/1,6). Заболевание возникало у лиц наиболее трудоспособного возраста, средний возраст женщин составил 43±14,1(М ±S) лет, мужчин 37± 17,2 (М ±S) лет. Чаще болели женщины и мужчины репродуктивного возраста (для женщин Мо 31 год, а для мужчин 22 года).
Длительность заболевания с момента появления первых признаков до постановки диагноза составила от 3 месяцев до 15 лет (Ме 24 мес., Мо 12 мес.). А от постановки диагноза до определения первичного очага гиперсекреции АКТГ максимум проходило 4 года.
В клинической картине пациентов с АКТГ-ЭС преобладали симптомы гиперкортицизма: артериальная гипертензия (93,75%), мышечная слабость проксимальных отделов нижних конечностей (81,25%), гиперпигментация (79%), увеличение веса (77%), остеопения и остеопороз (66%), стрии (62,5%), сахарный диабет (60,4%), аменорея у женщин (58,6%), гипокалиемия (52%), нарушение иммунитета (45,8%), переломы (45%).
Клиника карциноидного синдрома, проявляющаяся приступами дрожи в теле, чувством жара, обильным мочеиспусканием, ночными кошмарами, наблюдалась у 3 пациентов.
Циклическое течение гиперкортицизма было зафиксировано в 3 случаях. Все три случая наблюдались у женщин. В 2 случаях цикличность течения была установлена на основании анализа клинических данных (анамнез был подтвержден фотографиями пациенток, документировано фиксировавших изменения внешности). В одном случае циклическое течение АКТГ-ЭС было подтверждено также лабораторными тестами. Длина циклов гиперкортицизма была различна и варьировала от 2 до 11 месяцев, с промежутками нормальной секреции кортизола от 2 недель до 3 лет.
Лабораторная диагностика
Нарушение ритма секреции АКТГ и кортизола отмечалось у всех пациентов. При этом в ряде случаев в утренние часы уровни данных гормонов не превышали физиологических показателей. Данное явление отмечено в 6% для кортизола и в 12% АКТГ. В 11 часов вечера у всех пациентов уровни исследуемых гормонов превышали референсные значения (рис. 1А и Б).
АКТГ
кортизол
…….;…….*…..
И
8.00
Ме=13б,5 0(25-75)= 100,5-208,3 пг/мл
23.00
Ме=132,0
0(25-75)»
107,0-196,1
пг/мл
3000 1300
I
8.00 23.00
| 125*-75* ~7~ Римм без «ьЛр.
…..I………
5
X
0
8.00 23.00
8.00
Ме=1070,0 <3(25-75) = 888,0-1488,0 нмоль/л
23. 00 Ме=1080,0
00 Ме=1080,0
пг/мл,
0(25-75)=
814,0-1490.0
нмоль/л
3 28%.75% __ Размах ба* ашб| • Выброси ■ Крайние точки
Рисунок 1. Распределение уровней АКТГ в 8.00 и 23.00 у 47 пациентов с АКТГ-ЭС (А). Распределение уровней кортизола в 8.00 и 23.00 у 47 пациентов с АКТГ-ЭС (Б).
Свободный кортизол в суточной моче (38 пациентов) и слюне (11 больных) был повышен у всех пациентов, которым данные исследование проводились. При этом медиана для свободного кортизола мочи и слюны была в 6 раз выше верхней границы нормы данных показателей (рис. ЗА и Б).
О ■ < о (Сбросы 0
И 0
Рисунок 2. Распределение уровней свободного кортизола в суточной моче у 38 пациентов (А) и слюне у 11 больных (Б).
Данные о чувствительности фармакологических диагностических тестов для АКТГ-ЭС, полученные в нашем исследовании, сопоставимы с данными литературы. Так чувствительность для большой дексаметазоновой пробы в нашем исследовании 81%, в литературных источниках — 71% (Балаболкин М.И.,2008). Для периферического теста с десмопрессином чувствительность составила 91% в данной работе, что точно совпадает с данными №етап Ь.К. и соавт. (№етап Ь.К., 1993). При селективном заборе крови из нижних каменистых синусов со стимуляцией десмопрессином и оценкой градиента пролактина мы получили 100% чувствительность, что сочетается с данными Рожинской Л.Я. и соат. (Рожинская Л.Я., 2011).
Топическая диагностика
Инструментальная диагностика, направленная на выявление очага гиперсекреции АКТГ, включала в себя проведение ультразвукового исследования органов брюшной полости, забрюшинного пространства и органов малого таза, эзофагогастродуоденоскопии, колоноскопии, мультиспиральной компьютерной томографии органов грудной и брюшной полостей, позитронно-эмиссионной томографии, октреоскана.
Локализация НЭО с АКТГ-ЭС очень разнообразна. Чаще всего первичный очаг локализовался в правом легком (19 случаев, 39,6%), реже подобные опухоли обнаруживали в левом легком (13 случаев, 27%), тимусе (6 случаев, 13%), поджелудочной железе (2 случая, 4,2%), очень редко в аппендиксе, слепой кишке и левом надпочечнике (по 1 случаю, 2%).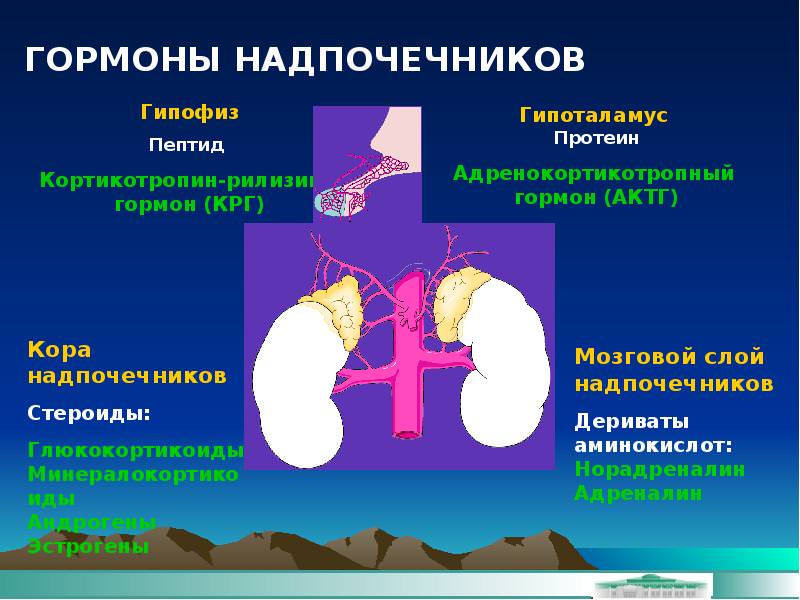 У 4 пациентов (8,6%) источник АКТГ-ЭС установить не удалось
У 4 пациентов (8,6%) источник АКТГ-ЭС установить не удалось
Морфологическое исследование
При гистологическом исследовании НЭО легких от 31 пациента, в большинстве случаев, у 20 пациентов (64,5%) были верифицированы типичные карциноиды (ТКЛ), в 10 случаях (32,2%) — атипичные карциноиды (АТКЛ), в 1 случае (3,3%) мелкоклеточный рак легкого (МКРЛ).
При гистологическом исследовании 6 НЭО тимуса было выявлено 4 (66,6%) атипичных карциноида (АТКТ) и 2 (33,4%) низко дифференцированные нейроэндокринные карциномы (НД НЭК, крупноклеточный и мелкоклеточный варианты) и ни одного типичного карциноида (ТКТ).
НЭО желудочно-кишечного были представлены 2 опухолями: НЭО аппендикса, в2 (с прорастанием в слепую кишку, жировою клетчатку и метастазами в лимфатические узлы брыжейки), и НЭО слепой кишки в1 — с метастазами в лимфатические узлы брыжейки, инвазией подвздошной кишки, жировой клетчатки, но при Кь67 равным 0.
В левом надпочечнике была выявлена одна феохромоцитома (ФХЦ) с АКТГ-ЭС, которая была не только источником эктопической секреции АКТГ, но и по данным анализа суточной мочи на метанефрин, норметанефрин, продуцировала адреналин и норадреналин.
Иммуногистохимическое исследование
Иммунофенотип 25 АКТГ-продуцирующих НЭО определяли с помощью ИГХ метода. Исследовали экспрессию в клетках опухолей общих нейроэндокринных маркеров: хромогранина А, синаптофизина, С056. Во всех случаях отмечалась интенсивная цитоплазматическая экспрессия ХрА и синаптофизина. Мембранная экспрессия С056 наблюдалась во всех случаях, кроме 4 (16%). Не было обнаружено корреляции между особенностями экспрессии нейроэндокринных маркеров и степенью дифференцировки клеток опухоли, но это можно объяснить целым рядом факторов — малой выборкой исследованных НЭО, особенно их низкодифференцированных вариантов, а также различной локализацией первичного очага.
Иммуногистохимическое исследование 37 НЭО выявило, что причиной гиперпродукции кортизола в 76% случаях являлась секреция опухолью АКТГ, в 8% КРГ, а в 16% АКТГ+КРГ (таблица 2).
Экспрессия АКТГ в большинстве случаев была интенсивной, составив 2,5 — 4 балла, и лишь в одном случае (феохромоцитома) этот гормон экспрессировался и единичными клетками опухоли.
Таблица 2. Экспрессия АКТГ и КРГ в НЭО с АКТГ-ЭС в зависимости от локализации первичного очага и степени дифференцировки опухоли.
нэо Экспрессия
АКТГ | КРГ | АКТГ+КРГ
N случаев
ткл 16 1
АТКЛ 5 2 3
АТКТ 3 1
НД НЭК тимуса крупноклеточная 1
НД НЭК тимуса мелкоклеточная 1
НЭО аппендикса, 02-3 1
НЭО слепой кишки 1
ФХЦ I
МКРЛ 1
ТКЛ — типичный карциноид легкого; АТКЛ — атипичный карциноид легкого; АТКТ — атипичный карциноид тимуса; ФХЦ — феохромоцитома; НД НЭК — низкодифференцированная нейроэндокринная карцинома; МКРЛ — мелкоклеточный рак легкого.
С целью определения спектра гормонов, продуцируемых НЭО, было проведено ИГХ исследование с использованием антител к тропным гипофизарным гормонам, ПТГ, кальцитонину и в 1 случае — к серотонину. По результатам исследования стало очевидно, что 76% НЭО могут экспрессировать одновременно несколько гормонов. Экспрессия двух гормонов выявлена в 45,5% случаев, трех гормонов — в 36%, а четырех — в 18,5%. При этом каждый гормон из этой панели, за исключением ПТГ, встречался хотя бы в одной из исследованных опухолей. Чаще всего в НЭО с АКТГ-ЭС наблюдались сочетания АКТГ+СТГ, АКТГ+кальцитонин, АКТГ+ СТГ+ПРЛ (таблица 3).
В нашем исследовании была выявлена слабая взаимосвязь между экспрессией в клетках НЭО гормонов ПРЛ и СТГ и повышением их активных форм в крови пациентов (г5=0,516 (для ПРЛ) и п=0,416 (для СТГ), р<0,05).
Определение индекса метки маркера ядер пролиферирующих клеток Кл-67 проводилось в 26 случаях. Для НЭО легких в 13 ТКЛ индекс К>67 был низким, варьируя в пределах от 0 до 5% (Ме = 1,0%; 0,25-2,5 [С>25-75]), а в 4 АТКЛ он составил 5%, 8,3%, 11% и 16,4%. При этом было выявлено статистически значимое различие между уровнем индекса Кл-67 для типичных и атипичных карцинидов легких (в соответствии с критерием Манна-Уитни, р=0,004).
При этом было выявлено статистически значимое различие между уровнем индекса Кл-67 для типичных и атипичных карцинидов легких (в соответствии с критерием Манна-Уитни, р=0,004).
В высокодифференцированных АТКТ индекс пролиферации И-67 определяли в 3 случаях: в 2 случаях он был равен 10%, в одном — 15%. В низкодифференцированной крупноклеточной НЭК тимуса индекс КЬ67 был равен 33%, а в мелкоклеточной составил 17,5%, с индексом пролиферации, достигающим 50% в метастазах данного варианта НД НЭК тимуса.
В опухоли аппендикса индекс К1-67 составил 18,7%, а в опухоли слепой кишки, несмотря на распространенность образования, не поддавался определению и был оценен как 0. В ФХЦ надпочечника индекс Ю-67 был невысоким и равным 4%.
Таблица 3. Ко-экспрессия различных гормонов в 29 НЭО с клиникой гиперкортицизма.
Экспрессия Маркеры Гистологические варианты НЭО различных локализаций
легкое тимус | н/п жкт
ТКЛ АТКЛ АТКТ НД НЭК тимуса мелкоюіето чная НДНЭК тимуса крупноклет очная Ф X ц НЭО аппе ндик са, Є2-3 НЭО слепой кишки
моногормональная N случаев
АКТГ 3 1 2
КРГ 1
бигормональная
АКТГ+КРГ 1
АКТГ+СТГ 3 1 1 1
АКТГ+кальцитонин 2
АКТГ+ серотонин 1
полигормональная
АКТГ+КРГ+СТГ 2
АКТГ+СТГ+ФСГ 1 1
АКТГ+СТГ+ кальцитонин 2 1
АКТГ+СТГ+ПРЛ 1
АКТГ+СТГ+ПРЛ+ кальцитонин 1 1
АКТГ+СТГ+ПРЛ+ЛГ 1
КРГ+АКТГ+СТГ+ПРЛ 1
ТКЛ-типичный карциноид легкого; АТКЛ — атипичный карциноид легкого; АТКТ — атипичный карциноид тимуса; ФХЦ -феохромоцитома; НД НЭК — низкодифференцированная нейроэндокринная карцинома; н/п — надпочечник
Для оценки рецепторного статуса 24 пациентам было выполнено ИГХ исследование с антителами (АТ) к рецепторам соматостатина 1-5 подтипов. ИГХ реакция с АТ к РССТ считалась положительной лишь при наличии мембранного окрашивания (2 и 3 балла). В ходе данного этапа исследования было выявлено, что в половине случаев (54%) нейроэндокринные опухоли, продуцирующие АКТГ, способны экспрессировать рецепторы к соматостатину различных подтипов. Как видно из таблицы 4, в НЭО легких преобладали РССТ2 (55%), реже встречались РССТ 3 и 5 подтипов. В АТКТ с равной частотой (33%) были выявлены РССТ 2 и 5 подтипов. В мелкоклеточной НД НЭК отсутствовали РССТ, а в крупноклеточной наблюдалась экспрессия РССТ2. В НЭО слепой кишки наблюдалась экспрессия РССТ5, а в НЭО аппендикса отсутствовала экспрессия всех типов РССТ. Ткань феохромоцитома имела очаговую экспрессию РССТ2.
ИГХ реакция с АТ к РССТ считалась положительной лишь при наличии мембранного окрашивания (2 и 3 балла). В ходе данного этапа исследования было выявлено, что в половине случаев (54%) нейроэндокринные опухоли, продуцирующие АКТГ, способны экспрессировать рецепторы к соматостатину различных подтипов. Как видно из таблицы 4, в НЭО легких преобладали РССТ2 (55%), реже встречались РССТ 3 и 5 подтипов. В АТКТ с равной частотой (33%) были выявлены РССТ 2 и 5 подтипов. В мелкоклеточной НД НЭК отсутствовали РССТ, а в крупноклеточной наблюдалась экспрессия РССТ2. В НЭО слепой кишки наблюдалась экспрессия РССТ5, а в НЭО аппендикса отсутствовала экспрессия всех типов РССТ. Ткань феохромоцитома имела очаговую экспрессию РССТ2.
Одновременная экспрессия нескольких подтипов РССТ выявлена в 31% случае, которая была представлена ко-экспрессией РССТ 2 и 3 подтипов и РССТ 2 и 5 подтипов с равной частотой встречаемости.
Таблица 4. Оценка экспрессии рецепторов к соматостатину в НЭО с АКТГ-ЭС различной локализации и степени дифференцировки.
Маркеры Оценка ИГХ реакции Гистологические варианты НЭО различных локализаций
легкое тимус н/п жкт
Т К Л А Т К Л А Т К Т нднэк тимуса мелкоклеточная НДНЭК тимуса Крупноклеточная ф X ц НЭО аппендикса, Є2-3 НЭО слепой кишки
N случаев
РССТ1 «-» 12 4 2 1 1 1 1
«+»
РССТ2 5 2 2 1 1 1
«+» 7 2 1 1 1
РССТЗ 11 4 2 1 1 1 1 1
«+» 2
РССТ4 12 4 2 1 1 1 1 1
«+»
РССТ5 11 4 2 1 1 1 1
«+» 1 1 1
ТКЛ — типичный карциноид легкого; АТКЛ — атипичный карциноид легкого; АТКТ -атипичный карциноид тимуса; ФХЦ — феохромоцитома; НД НЭК -низкодифференцированная нейроэндокринная карцинома; н/п — надпочечник. «-» -отрицательная реакция, «+»- положительная реакция.
Невысокая частота встречаемости экспрессии РССТ2 и РССТ5 в НЭО, секретирующих АКТГ, возможно связана с влиянием гиперкортицизма. Сильное подавляющее действие избыточного количества глюкокортикоидов на экспрессию РССТ2 и незначительное на РССТ5 было продемонстрировано в работе С. de Bruin и соавт. В этом же исследовании показан другой интересный аспект — увеличение экспрессии РССТ2 уже через 2-4 дня после снятия глюкокортикоидной экспозиции (de Bruin С, 2009).
Сильное подавляющее действие избыточного количества глюкокортикоидов на экспрессию РССТ2 и незначительное на РССТ5 было продемонстрировано в работе С. de Bruin и соавт. В этом же исследовании показан другой интересный аспект — увеличение экспрессии РССТ2 уже через 2-4 дня после снятия глюкокортикоидной экспозиции (de Bruin С, 2009).
Неблагоприятные варианты течения АКТГ-эктопироваиного синдрома.
Метастатическое поражение было отмечено в 32% случаев (15 пациентов). Все НЭО тимуса, включенные в исследование, давали метастазы, с наличием очагов отсева НЭО и/или инвазией окружающих тканей в 67% случаев на момент диагностики заболевания. Метастазы НЭО легких были обнаружены в 16% случаев после удаления опухоли. В 1 случае мы верифицировали отдаленные метастазы в кости НЭО с АКТГ-ЭС с неустановленным первичным очагом.
НЭО аппендикса, слепой кишки имели метастазы в лимфатические узлы брыжейки на момент диагностики. НЭО поджелудочной железы дала очаги отсева в печень.
Локализация метастазов НЭО была разнообразной. В 3,5 раза чаще, чем отдаленные метастазы, наблюдалось поражение регионарных лимфатических узлов и инвазия окружающих тканей. Отдаленные метастазы были выявлены в 8,5% случаев (у 4 пациентов), одинаково часто в кости скелета и печень (таблица 5).
Таблица 5. Местонахождение первичного очага, его морфологическое строение и локализация метастазов из него.
Локализация первичного очага (количество и морфологический вариант строения НЭО) N (%) случаев с метастазами на момент диагностики АКТГ-ЭС N (%) случаев возникновения рецидивов после проведения радикального хирургического лечения Локализация метастазов
Тимус (4 АТКТ, 2 НД НЭК тимуса) 4 (67%) 2 (33%) • кости скелета • перикард • нижняя доля правого легкого • лимфатические узлы правой подмышечной области
Легкие (ЗТКЛ, 2АТКЛ) 0 5 (16%) • средостение • печень • плевра
Червеобразный отросток (1 НЭО аппендикса, 02-3) 0 1 • лимфатические узлы брыжейки
Слепая кишка (1 НЭО слепой кишки) 0 1
Головка поджелудочной железы (1 морфологический вариант не известен) 0 1 • печень
Локализация первичного очага не установлена (1 случай) 0 1 • кости скелета
ТКЛ — типичный карциноид легкого; АТКЛ — атипичный карциноид легкого; АТКТ -атипичный карциноид тимуса; НД НЭК — низкодифференцированная нейроэндокринная карцинома
Рецидивы АКТГ-ЭС возникли у 20% пациентов после проведения радикального хирургического лечения. При этом возврат симптомов заболевания отмечался как при типичных, так и атипичных карциноидах легкого после периода ремиссии длительностью от 15 до 50 мес. Половина случаев с локализацией первичного очага в тимусе имела рецидив АКТГ-ЭС после хирургического лечения в период от 16 до 48 мес.
При этом возврат симптомов заболевания отмечался как при типичных, так и атипичных карциноидах легкого после периода ремиссии длительностью от 15 до 50 мес. Половина случаев с локализацией первичного очага в тимусе имела рецидив АКТГ-ЭС после хирургического лечения в период от 16 до 48 мес.
Одним из исходов хирургического лечения является возникновение вторичной надпочечниковой недостаточности, в результате длительно
существующей гиперкортизолэмии, которая приводит к блокаде гипоталамо-гипофизариой системы. Длительность вторичной надпочечниковой недостаточности может варьировать от нескольких месяцев до ряда лет. В данном исследовании вторичная надпочечниковая недостаточность после проведения радикального хирургического лечения наступала у большей части пациентов в ранний послеоперационный период, что требовало назначения заместительной терапии глюкокортикостероидами.
Летальные исходы заболевания мы наблюдали в 8 случаях (17 %), вне зависимости от возраста пациентов (от 30 до 77 лет). У пациентов преклонного возраста (70 и 77 лет) смерть наступала до проведения операционного лечения АКТГ-ЭС, вследствие тромбоэмболии легочной артерии (ТЭЛА), которой предшествовали артериальная гипертензия, нарушение ритма, миокардиодистрофия и хроническая сердечная недостаточность. У пациентов среднего возраста смертельные случаи наблюдались в первые дни после операции (до 13 сут.), причем как после удаления первичного очага и его метастатических отсевов, так и после двухсторонней адреналэктомии (2 пациента). Причиной летальных исходов у лиц молодого и среднего возраста являлась ТЭЛА, синдром диссеминированного внутрисосудистого свёртывания, полиорганная недостаточности при неоперабельных НЭО. В двух случаях причину смерти уточнить не удалось.
Факторы риска возникновения рецидива АКТГ-ЭС
С целью выявления клинических симптомов, являющихся предикторами неблагоприятного течения заболевания (рецидивы и метастазы на момент диагностики), был проведен многофакторный кластерный анализ. По результатом которого существенных различий в клинических проявлениях АКТГ-ЭС в зависимости от течения заболевания не найдено.
Несмотря на то, что экспрессия КРГ отмечалась чаще в НЭО с потенциально более агрессивным поведением, так отмечена положительная реакция с антителами к КРГ в МКРЛ, в 50% АТКЛ и 25% АТКТ, тогда как в ТКЛ экспрессия КРГ зафиксирована лишь в одном случае (6%), статистически значимого различия по группам получить в данном случае не удалось (х2, р=0.0922426; точный метод Фишера, р=0.0907093), что возможно связано с малой выборкой.
Достоверной корреляции между локализацией первичного очага, степенью дифференцировки НЭО, полигормональной экспрессией, экспрессией РССТ и агрессивностью заболевания установлено не было.
Однако следует обратить особое внимание на НЭО тимуса, поскольку при данной локализации у пациентов в 100% случаев были выявлены метастазы.
Индекс пролиферации Ю-67 в АКТГ-продуцирующих НЭО у пациентов с более агрессивным клиническим течением был выше, чем в опухолях пациентов без метастазов и рецидивов заболевания (по критерию Манна-Уитни, р=0,0059; г5=0,5б, р <0,05), что возможно связано с тем, что к первой группе относились более агрессивные НЭО (НД НЭК тимуса, атипичные карциноиды тимуса и легких, НЭО червеобразного отростка, С2-3).
При изучении ожидаемого времени наступления рецидива в зависимости от значения индекса пролиферации в карциноидах легкого (выбрана данная группа, как наиболее многочисленная, N=26 пациентов) выявлено, что с увеличением значения КЬ67 сокращалось и время до наступления рецидива. У пациентов со значениями индекса Кь67 около 25% рецидив можно ожидать с вероятностью 95% в течение 1 года после удаления первичного очага, а в группе со значением этого индекса около 20% — в течение 1,5 лет. Рецидив с вероятностью 90% и 50% возникнет через 3 года у пациентов с индексом Кь67 равным 15% и 10%, соответственно. Возникновение рецидива в течение 5 лет после радикального хирургического лечения с вероятностью 22% можно ожидать у пациентов со значением индекса Кь67 опухоли равном 5%, и с вероятностью до 20% — при его значениях 0-3%. Однако следует отметить, что в виду малой выборки 95% доверительный интервал значительно увеличивается для высоких значений индекса пролиферации Кл-67, что снижает прогностическую ценность выводов, относящихся к большим значениям этого индекса (15-25%).
………..-1-……………I
I
Н-+…..■+■ -•+■•
……..4 ■■
…….+»
………….•+
•»»……+
—Н
—НН—-+—н———-ь————
•-+•—-к
-Г»
20
ч~нн—+—+————-
———————+
н-»1
Т»
40
60
—I— 100
—Г-120
Месяцу
К)67
— 0%
—- 1% …….. 3%
…… 5о/о
— 10% —- 15%
— 20%
25%
Рисунок 3. Вероятность развития рецидива при различных значениях индекса пролиферации Кл-67 для карциноидов легких с АКТГ-ЭС с момента хирургического удаления первичного очага (сечение регрессии Кокса при Кь67=соп51).
Статистический анализа данных с помощью регрессии Кокса при фиксированном времени выявил, что с вероятностью 50% рецидив заболевания можно ожидать в течении 1 года после радикального удаления первичного очага у пациентов с индексом Кл-67 равным 18%, в течение 2 лет с индексом 12% и в течение 5 лет с уровнем маркера пролиферации 9% (р=0,04588) (рас.4)
«¡67 [%]
Рисунок 4. Вероятность развития рецидива при различных уровнях индекса пролиферации К>67 для карциноидов легких с АКТГ-ЭС (сечение регрессии Кокса при 1=сош1).
В качестве фактора прогноза АКТГ-ЭС была исследована особенность экспрессии цитокератина 19 (белка входящего в состав промежуточных микрофиламентов цитоскелета) в НЭО, продуцирующих АКТГ. Полученное значение г5 = 0,039 близко к уровню 0,4, который является статистически значимым, что позволяет предполагать, что ЦК-19, при условии набора более многочисленной и репрезентативной группы НЭО, секртирующих АКТГ, может являться потенциальным маркером менее благоприятного течения заболевания.
ВЫВОДЫ
1. Клинические проявления АКТГ-эктопированного синдрома характеризуются симптомами гиперкортицизма, которые в большинстве случаев отличаются прогрессирующим течением, но в 6% случаев могут иметь циклическое течение и в ряде случаев (6%) сочетаться с клиникой карциноидного синдрома.
2. Локализация первичного очага при АКТГ-эктопированном синдроме разнообразна, с преимущественным расположением в легких (67%; 32 случая), реже в тимусе (13%; 6 пациентов), поджелудочной железе (4,2%; 2 больных), в аппендиксе и слепой кишке (по 2%; по 1 случаю), в надпочечнике (2%; 1 больной). Источник гиперсекреции АКТГ установить не удалось у 4 пациентов (8,6%).
3. Нейроэндокринные опухоли, секретирующие АКТГ, дают метастазы в трети случаев (15 пациентов), с преимущественным поражением регионарных лимфатических узлов и инвазией окружающей ткани (в 3,5 раза чаще, чем отдаленные метастазы).
4. Рецидивы АКТГ- эктопического синдрома после радикального хирургического лечения возникают в 20% случаев (8 из 40 пациентов). В нейроэндокринных опухолях тимуса рецидивы зафиксированы в 50% случаев после периода ремиссии длительностью от 16 до 48 мес. Рецидивы после удаления первичного очага в легких диагностировали в 16% случаев через 15 -50 мес. как при типичных (3 случая), так и атипичных карциноидах (2 случая).
5. Морфологическое строение нейроэндокринных опухолей с АКТГ-эктопическим синдромом разнообразно и представлено типичными (50%; 20 случаев) и атипичными карциноидами легких (25%; 10 больных), атипичными карциноидами тимуса (10%; 4 пациента), феохромоцитомой (2,5%; 1 случай), нейроэндокринными опухолями аппендикса (С2-3) и слепой кишки (по 2,5%; по 1 случаю), низко дифференцированными нейроэндокринными карциномами тимуса (по 2,5%; 1 случай мелкоклеточной и 1 крупноклеточной карциномы) и мелкоклеточным раком легкого (2,5%; 1 пациент).
6. Нейроэндокринные опухоли, продуцирующие АКТГ, способны вырабатывать по данным иммуногистохимического исследования не только АКТГ (в 76% случаев) и КРГ (у 8% пациентов), или их сочетание (в 16%), но и обладают в большинстве случаев (76%) полигормональной активностью с секрецией как тропных гормонов гипофиза, так и кальцитонина, с наиболее частым сочетанием ко-экспрессии АКТГ+ соматотропный гормон (62%; 18 больных), АКТГ+ кальцитонин (26,5%; 7 случаев) и АКТГ+ соматотропный гормон + пролактин (13,8%; 4 случая).
7. Маркер пролиферации Кг-67 прогностически значим для карциноидов легких. Рецидив заболевания можно ожидать в 50% случаев в течение 1 года после радикального удаления первичного очага при индексе К1-67 равном 18%, в течение 2 лет с индексом 12% и в течение 5 лет с уровнем маркера пролиферации 9%.
8. Экспрессия в клетках опухоли цитокератина 19 может являться потенциальным фактором прогноза рецидива АКТГ-ЭС.
9. Нейроэндокринные опухоли, продуцирующие АКТГ, в 54% случаев могут экспрессировать рецепторы к соматостатину (РССТ) разных подтипов, которые можно выявить иммуногистохимическим методом. Чаще всего встречаются рецепторы 2 подтипа (70%), а ко-экспрессия нескольких подтипов рецепторов, а именно РССТ2 и 5 и РССТ2 и 3 подтипов, наблюдается в 31% случае.
10. Достоверной корреляции между локализацией первичного очага НЭО, продуцирующей АКТГ, степенью дифференцировки НЭО, полигормональной активностью, экспрессией различных подтипов рецепторов к соматостатину и наличием метастазов установлено не было.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Пациентам с симптомами эндогенного гиперкортицизма необходимо проводить поиск источника АКТГ-ЭС с использованием всех доступных диагностических процедур: проводить стимуляционные фармакологические пробы с десмопрессином, использовать методы визуализации (мультиспиральную компьютерную томографию с контрастированием и ультразвуковой метод исследования, магниторезонансную томографию).
2. После радикального удаления первичного очага НЭО следует проводить мониторинг уровней АКТГ и кортизола в первые дни после оперативного лечения, ввиду развития у данных пациентов вторичной надпочечниковой недостаточности. Далее рекомендуется анализировать уровни данных гормонов каждые 3 мес. с целью титрования дозы глюкокортикостероидов, а также выполнять визуализационные методы исследования каждые 6 мес. с целью поиска возможного рецидива АКТГ-эктопического синдрома и метастазов НЭО, секретирующей АКТГ.
3. Только выявление мембранного типа экспрессии рецепторов к соматостатину с интенсивностью 2-3 балла можно оценивать как положительный результат, который может обосновать назначение аналогов соматостатина пациентам с АКТГ-ЭС при невозможности радикального удаления опухоли и при распространенных опухолях с метастазами.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Циклический синдром Кушинга / Марова Е.И., Воронкова И.А. // Проблемы эндокринологии,- 2010.- 56(4). — С.47-51.
2. Характеристики нейроэндокинных опухолей негипофизарной локализации, продуцирующих АКТГ / Воронкова И. А., Марова Е. И., Арапова С. Д., Дзеранова Л. К., Рожинская Л. Я.,Белая Ж. Е., Лапшина А. М., Колесникова Г. С. // Бюллетень ФЦСКЭ им В.А. Алмазова, «Алмазовские чтения 2011»,- 2011. — С.100-101.
3. АКТГ-продуцирующая феохромоцитома. Клинический случай / Н.С. Кузнецов, Е.И. Марова, Н.В. Латкина, Е.А. Добрева, В.В. Крылов, Л.Е. Кац, О.В. Ремизов, И.А. Воронкова // Эндокринная хирургия.- 2012.4,- С. 43-45.
4. Гистологические и иммуногистохимические характеристики АКТГ-секретирующих опухолей / А. М. Лапшина, И.А. Воронкова, Е.И. Марова//Архив патологии,- 2013. — 3 -С.8-13.
5. АКТГ-эктопический синдром, циклического течения; нейроэндокринная опухоль червеобразного отростка / И.А. Воронкова, С.Д. Арапова, Е.И. Марова, Н.С. Кузнецов, А.Ю. Абросимов, Л.Я.Рожинская // Проблемы эндокринологии. -2013.-4,- С. 23-27.
6. Comparative study of the ACTH-secreting pituitary and extrapituitary tumors immunohistochemical features / Marova E.I., Lapshina A.M., Abrosimov A.Yu., GrigorMev A.Yu., Kuznetsov N.S., Voronkova I.A. // Abstract book European NeuroEndocrine Association. — 2010. — PC 87.
7. The case of cyclic ectopic Cushing’s syndrome, well differentiated neuroendocrine carcinoma of appendix / Voronkova I. A., Arapova, I.A. N.S. Kuznetsov, A.Yu. Abrosimov, E.I. Marova, L.Ya. Rozhinskaya // Abstract book European NeuroEndocrine Association.- 2010. — PC 43.
8. The characteristic of the ACTH-secreting extrapituitary neuroendocrine tumors / G.S. Kolesnikova, A.M. Lapshina, I.A. Voronkova, E.I. Marova, S.D. Arapova, N.P. Goncharov, and I.I. Dedov // Virchows Arhiv. 23rd European congress of pathology. — 2011. — S 223.
9. CK19 Expression in ACTH-producing extrapituitary neuroendocrine neoplasms is a negative prognostic factor / Gurevich L., Voronkova I., Marova E., Korsakova N., Britvin Т., Ustinova E., Dreval A., Mazurin V., Frolov A., Panteleeva E. // Abstract book 9th Annual ENETS Conference. -2012.-B10.
lO.The case of ectopic Cushing’s syndrome, neuroendocrine tumor of the cecum / Voronkova I.A., Gurevich L.E., Marova E. I., Rojinskaya L.Ya. // 25 European Congress of pathologists.-2013,- PS-02-033.
СПИСОК СОКРАЩЕНИЙ АКТГ- адренокортикотропный гормон АКТГ-ЭС — АКТГ-эктопический синдром АТКЛ -атипичный карциноид легкого АТКТ- атипичный карциноид тимуса ИГХ — иммуногистохимическое исследование КРГ- кортикотропин релизинг гормон ЛГ — лютеинизирующий гормон МСКТ- мультиспиральная компьютерная томография МКРЛ — мелкоклеточный рак легкого НЭО — нейроэндокринная опухоль ПРЛ — пролактин ЦК 19- цито кератин 19 СТГ — соматотропный гормон ТКЛ — типичный карциноид легкого ТЭЛА -тромбоэмболия легочной артерии ФСГ- фолликулстимулирующий гормон ФХЦ — феохромоцитома.
Подписано в печать: 26.12.2013 Объём: 1 п. л. Тираж: 100 экз. Заказ № 236 Отпечатано в типографии «Реглет» 119526, г. Москва, ул. Бауманская, д. 33, ар. 1 +7(495)979-98-99, www.reglet.ru
Создан новый метод выращивания цианобактерий в марсианских условиях
Компания NASA в сотрудничестве с другими ведущими космическими агентствами планирует отправить первую миссию с людьми на Марс в начале 2030-х годов.
Астронавтам на Марсе понадобятся кислород, вода, пища и другие расходные материалы, их нужно научиться хранить или добывать на Марсе, так как импортировать их с Земли будет очень затратно.
Для этого ученые впервые разработали биотехнологию, с помощью которой цианобактерии Anabaena можно выращивать только с использованием марсианских газов, воды и других питательных веществ, а также при низком давлении. Это значительно облегчает разработку устойчивых биологических систем жизнеобеспечения.
Цианобактерии уже давно рассматриваются в качестве кандидатов для обеспечения биологической жизнедеятельности в космических полетах. Все виды бактерий производят кислород с помощью фотосинтеза, а цианобактерии могут фиксировать атмосферный азот в питательные вещества.
Однако трудность заключается в том, что они не могут расти непосредственно в марсианской атмосфере, где общее давление составляет менее 1% от Земного — от 6 до 11 ГПа: это слишком мало для присутствия жидкой воды, в то время как парциальное давление газообразного азота — от 0,2 до 0,3 ГПа — это недостаточно для их метаболизма.
Но воссоздание атмосферы как на Земле было бы слишком дорого: газы нужно было бы импортировать. Поэтому исследователи искали золотую середину: атмосферу, близкую к Марсианской, которая позволяет цианобактериям хорошо расти.
Так ученые разработали биореактор под названием Atmos, в котором цианобактерии могут размножаться и жить в искусственных атмосферах при низком давлении. Atmos имеет девять сосудов объемом 1 л из стекла и стали, каждый из которых стерилен, может нагреваться и изменять давление по необходимости.
Авторы выбрали штамм азотфиксирующих цианобактерий Anabaena sp. PCC 7938, потому что предварительные испытания показали, что он будет особенно хорошо использовать марсианские ресурсы, а также активно размножаться.
Исследователи пришли к выводу, что азотфиксирующие, продуцирующие кислород цианобактерии можно вырастить на Марсе при низком давлении в контролируемых условиях с использованием исключительно местных ингредиентов.
Источник: ХАЙТЕК
№AN118FOL, Исследование на уровень фолиевой кислоты (витамина В9) для собак и кошек: показатели, норма
Фолиевая кислота необходима в процессах регуляции функций органов гемопоэза, повышает содержание холина в печени, влияет на активность иммунной системы.
Фолиевая кислота и ее активные производные (ди-, три-, полиглутоматы и другие) объединены в группу фолатов.
- Описание исследования на уровень фолиевой кислоты
- Преаналитические требования
- Интерпретация результата
Дрожжи, печень и лиственные растения являются основными источниками этого водорастворимого витамина. Ни животные, ни бактерии не могут выжить без источника фолиевой кислоты. Животные не могут синтезировать фолиевую кислоту и, следовательно, усваивают предварительно синтезированную фолиевую кислоту из корма.
В отличие от животных, бактерии не могут усваивать фолиевую кислоту из внешней среды и, следовательно, в них сформировались ферментативные механизмы для синтеза фолиевой кислоты из птеридина, ПАБК и глутамата. Различие между животными и бактериями в их способности усваивать и синтезировать фолиевую кислоту, было использовано для разработки селективных антибиотиков сульфонамидного ряда, выступающих в качестве конкурентных ингибиторов участия ПАБК в бактериальном биосинтезе фолиевой кислоты.
Фолиевая кислота в кормах, как правило, присутствует в плохо абсорбируемой форме полиглютамата (конъюгированная форма).
Деконъюгация полиглютамата в моноглутамат осуществляется ферментом щеточной каемки микроворсинок, секретируемым в тощем отделе кишечника. В проксимальном отделе тонкого кишечника поглощение фолатов происходит с помощью специфических переносчиков. Заболевания проксимального отдела или всего тонкого кишечника (например, воспалительные заболевания кишечника) могут уменьшить абсорбцию фолатов, которое происходит либо в результате нарушения деконъюгации полиглютамата, либо за счет уменьшения числа белков-переносчиков фолатов, что приводит к снижению концентрации фолатов в сыворотке крови. В крови небольшая часть фолатов связываются со специфическими белками и быстро используются печенью и другими органами. Поступление фолатов в клетки является активным процессом. Кобаламин (В12) участвует в клеточном захвате моноглутамата и внутриклеточной трансформации в полиглутамат.
Функциональный дефицит фолиевой кислоты также может возникать в случаях дефицита кобаламина, а концентрация фолиевой кислоты в сыворотке крови у этих животных может быть нормальной или даже увеличена, в результате снижения использования фолиевой кислоты. Треть поступившего в клетку фолата, находится в митохондриях. Основными метаболически активными формами фолата являются: 5-метилтетрагидрофолат, 10-формилтетрагидрофолат и тетрагидрофолат, которые переносят одноуглеродные остатки в жизненно важных для организма реакциях, в том числе, в процессе синтеза ДНК.
Бактерии, присутствующие в дистальном отделе тонкой и толстой кишки продуцируют большое количество фолатов, которые, как правило, выделяется с калом. Переносчики фолатов, ответственные за их абсорбцию расположены исключительно в проксимальном отделе тонкого кишечника и, таким образом, фолат, образующийся в дистальных отделах кишечника, не будет поглощен. Если фолат-продуцирующие бактерии мигрируют вверх в проксимальный отдел тонкой кишки, фолиевая кислота бактериального происхождения может абсорбироваться хозяином, что вызывает повышенные концентрации сывороточного фолата. Синтезировать фолиевую кислоту может большое число видов бактерий и, таким образом, избыточный бактериальный рост в тонком кишечнике может привести к значительному увеличению концентрации фолиевой кислоты в сыворотке крови.
У собак с ЭНПЖ (эндокринной недостаточностью поджелудочной железы) отмечается пониженная секреция антибактериальных продуктов, и как следствие, последующий избыточный бактериальный рост в тонком отделе кишечника, который приводит к увеличению сывороточной концентрации фолиевой кислоты. Избыточная концентрация фолатов в крови снижает активность NK-клеток.
Клиническое значение увеличения концентрации фолиевой кислоты в сыворотке крови у кошек остается неясной.
Проксимальный отдел тонкой кишки уязвим к повреждениям, которые могут вызвать антигены (определенные белки рациона), в повышенной концентрации поступающие при пероральном приеме в эту область. Примером может служить целиакия (глютеновая энтеропатия) у ирландских сеттеров. Абсорбция фолиевой кислоты лучше происходит при более низком значении рН, которая может быть обусловлена либо избыточной секрецией желудочного сока, либо пониженной секреции бикарбоната. Последнее можно рассматривать в случаях ЭНПЖ.
Преаналитика:
Для получения более точных результатов животные перед исследованием должны находиться на голодной диете не менее 12 часов. Образец стабилен 5 дней при температуре хранения +2°С…+8°С; сохраняет стабильность 6 недель при замораживании -17С…-23С.
Интерпретация:
Результаты исследования содержат информацию исключительно для врачей. Диагноз ставится на основании комплексной оценки различных показателей, дополнительных сведений и зависит от методов диагностики.
Единицы измерения в лаборатории VET UNION: нг/мл
Референсные значения:
- Собаки: 7.7 — 25 нг/мл
- Кошки: 9 — 22 нг/мл
Результаты исследования имеют значение в случае, если функция поджелудочной железы не нарушена и имеется хроническое истощение резервов витамина В12 и фолиевой кислоты. Сочетание снижения уровня витамина B12 и увеличение концентрации фолата в крови, при нормальной экзокринной функции поджелудочной железы, предполагает избыточный бактериальный рост в тонком кишечнике, также известный как антибиотик-ассоциированная диарея или бактериальный дисбактериоз.
Повышение показателя:
- Избыточный бактериальный рост в тонком кишечнике (собаки).
- Повышение потребление фолиевой кислоты (добавки).
- ЭНПЖ (увеличение фолата при ЭНПЖ предлагает избыточный бактериальный рост в тонком кишечнике; улучшение абсорбции фолата в результате снижения уровня рН).
Понижение показателя:
- Заболевания проксимального отдела тонкой кишки или диффузные заболевания тонкой кишки (воспалительное заболевание кишечника, лимфома, грибковые заболевания).
- Применение некоторых лекарственных средств (например, фенитоин, сульфасалазин).
- Снижение концентрации фолиевой кислоты в сыворотке крови в результате мальабсорбции, указывает на тяжесть заболевания и истощение запасов в организме.
- Снижение использования фолата и последующее повышение концентрации фолиевой кислоты в сыворотке крови может происходить вторично по отношению к тяжелой гипоальбуминемии. Кобаламин необходим для превращения производных фолиевой кислоты в активную форму (тетрагидрофолат), необходимого для синтеза ДНК. Увеличение в сыворотке фолиевой кислоты наблюдается у кошек с тяжелой гипоальбуминемией.
Содержание цитокинов в крови новорожденных от матерей с онкологическими заболеваниями, получавших противоопухолевую химиотерапию во время беременности
ФГБУ Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздрава России, Москва
Цель исследования. Определить содержание цитокинов, хемокинов, ростовых факторов в периферической крови женщин с онкологическими заболеваниями, принимавших противоопухолевую химиотерапию во время беременности, и в крови их новорожденных.
Материал и методы. Методом мультиплексного анализа проведена оценка содержания 27 факторов в плазме крови женщин, принимавших противоопухолевые химиопрепараты во время беременности, а также в пуповинной и венозной крови их детей. Группу сравнения составили женщины с физиологическим течением беременности и их новорожденные.
Результаты. У женщин с онкологическими заболеваниями, принимавших противоопухолевые химиопрепараты во время беременности, снижена цитокин-продуцирующая способность иммунных клеток относительно соответствующих показателей в группе сравнения. Применяемые матерью лекарственные средства не оказали существенного влияния на уровень цитокинов в пуповинной крови новорожденных. К концу неонатального периода концентрация IL-6, IL-8, IL-9, IL-12, MCP-1, MIP-1β, VEGF, GM-CSF в крови детей снижается по сравнению со значениями в возрасте 3 суток жизни.
Заключение. Применение противоопухолевых химиопрепаратов во время беременности снижает секреторную активность клеток иммунной системы женщин и не оказывает существенного влияния на уровень цитокинов, хемокинов и ростовых факторов в плазме пуповинной крови новорожденных.
Частота выявления онкологических заболеваний во время беременности неуклонно растет: в настоящее время в развитых странах данный показатель составляет 1:1000 [1]. Наиболее распространенными злокачественными заболеваниями, сопряженными с беременностью, являются: рак молочной железы (РМЖ), гематологические болезни, рак шейки матки, рак яичника, рак щитовидной железы. Первое место по частоте выявления занимают РМЖ (10–30:100000) и гемобластозы (10–60:100000 беременных женщин) [2]. Принимая во внимание тот факт, что формирование эффективного противоопухолевого иммунного ответа происходит на Th2-фоне [3], а успешное пролонгирование беременности возможно при условии сдерживания цитотоксического иммунного ответа и поляризации иммунного ответа по Th3-пути [4], оценка баланса провоспалительных и противовоспалительных цитокинов в периферической крови беременных женщин с онкологическими заболеваниями представляет несомненный интерес.
В настоящее время большое внимание уделяется возможности применения противоопухолевых химиопрепаратов у женщин с онкологическими заболеваниями в течение беременности [5–7]. Противоопухолевые средства способны оказывать выраженное стимулирующее влияние на цитокин-продуцирующую активность иммунных клеток как напрямую, так и за счет активирующего влияния антигенов, появляющихся вследствие разрушения опухолевых клеток [8]. Доказано, что избыточный провоспалительный фон у женщин с РМЖ может оказывать существенное негативное влияние на их когнитивные функции после противоопухолевого лечения [9]. Спектр применяемых во время беременности химиопрепаратов ограничен, поскольку многие из них имеют малую молекулярную массу, липидорастворимы и неионизированы, что благоприятствует их пассивному прохождению через плацентарный барьер. Тем не менее, концентрация их в крови плода находится на низком уровне, что объясняется снижением всасывания препаратов в желудочно-кишечном тракте матери, изменением их фармакокинетики вследствие формирования особого гормонального фона, особенностями гемодинамики (увеличение объема жидкости в организме беременной женщины, приводящее к снижению концентрации препарата и увеличению периода его полувыведения), а также наличием плацентарных белков, регулирующих содержание лекарственных веществ в крови плода [5]. Применение химиопрепаратов в I триместре беременности оказывает наиболее выраженный тератогенный эффект: возможно повреждение сердца, нервной трубки, органов слуха и зрения у плода [10]. В то же время, во II и III триместре основные этапы органогенеза завершены, и риск развития пороков у плода минимален [5]. Однако вопрос о влиянии противоопухолевых лекарственных средств на иммунную систему плода и новорожденного изучен недостаточно.
Цель исследования: определить содержание цитокинов, хемокинов, ростовых факторов в периферической крови женщин с онкологическими заболеваниями, принимавших противоопухолевую химиотерапию во время беременности, и в крови их новорожденных.
Материал и методы исследования
В проспективное когортное исследование включены 10 беременных женщин с онкологическими заболеваниями, получавших химиотерапию во время беременности, и их новорожденные дети. Группу сравнения составили 9 женщин с физиологическим течением беременности и их новорожденные. Осуществляли забор периферической венозной крови у женщин перед родоразрешением, крови из вены пуповины и периферической крови новорожденных в возрасте 3 суток и 1 месяца жизни. Содержание цитокинов в плазме определяли мультиплексным методом на анализаторе Bioplex 200 (Bio-Rad, USA) с применением коммерческого набора (Bio-Rad, USA). Оценивали уровень провоспалительных (интерферон (IFN)γ, фактор некроза опухоли (TNF)α, интерлейкины (IL)-1b, IL-2, IL-6, IL-9, IL-12, IL-15, IL-17) и противовоспалительных (IL-4, IL-5, IL-10, IL-13, антагонист рецептора IL-1 (IL-1Ra)) цитокинов, хемокинов (IL-8, моноцитарный (MCP-1) и эозинофильный (Eotaxin) хемотаксические факторы, макрофагальные белки воспаления (MIP-1α, MIP-1β), хемокин, экспрессируемый и секретируемый Т-клетками при активации (RANTES), индуцируемый интерфероном-γ белок (IP-10)) и ростовых факторов (васкуло-эндотелиальный (VEGF) и тромбоцитарный (PDGF bb) факторы роста, основной фактор роста фибробластов (FGF-b), колониестимулирующие факторы (G-CSF, GM-CSF), IL-7).
Жукова А.С., Макиева М.И., Ванько Л.В., Вторушина В.В., Матвеева Н.К., Цой Т.А., Волочаева М.В., Тимофеева Л.А., Кречетова Л.В., Зубков В.В., Шмаков Р.Г.
Альдостерон-рениновое соотношение (альдостерон, ренин, соотношение)
Метод определения №205 «Альдостерон» и №206 «Ренин (прямой метод)» – см. описания соответствующих тестов, АРС – расчет.Исследуемый материал Плазма крови (ЭДТА)
Доступен выезд на дом
Онлайн-регистрацияИспользуется в целях скрининга и диагностики первичного гиперальдостеронизма.
Состав профиля:- альдостерон, плазма;
- ренин, плазма;
- альдостерон-рениновое соотношение (расчет).
Первичный гиперальдостеронизм – собирательный диагноз, характеризующий состояния с повышенным уровнем альдостерона, секреция которого относительно независима от ренин-ангиотензиновой системы и натриевой нагрузки. Повышение уровня альдостерона является причиной артериальной гипертензии, сердечно-сосудистых расстройств, задержки натрия и ускоренного выделения калия (что приводит к гипокалиемии). Причиной первичного гиперальдостеронизма могут быть аденома надпочечника, односторонняя или двусторонняя надпочечниковая гиперплазия, в редких случаях – наследственно обусловленный гиперальдостеронизм.
Ранее предполагалось, что частота встречаемости первичного гиперальдостеронизма составляет менее 1% пациентов с эссенциальной гипертензией, и считалось, что гипокалиемия является обязательным критерием этого диагноза. Данные, накопленные к настоящему времени, привели к пересмотру этих представлений. Исследования показали, что первичный гиперальдостеронизм отмечается более чем у 10% пациентов с артериальной гипертензией, являющейся наиболее частым и общим проявлением данной патологии, а гипокалиемия обнаруживается при тяжелом течении заболевания (концентрации калия в сыворотке крови менее 3,5 ммоль/л определяется у половины больных с альдостерон-продуцирующей аденомой и у 17% пациентов с идиопатическим гиперальдостеронизмом).
Диагностика первичного гиперальдостеронизма имеет большое значение, как из-за его распространенности, так и в связи с более высокой частотой сердечно-сосудистых поражений по сравнению с эссенциальной артериальной гипертензией (при аналогичной степени повышения артериального давления). Своевременный диагноз позволяет применить адекватное лечение и улучшить качество жизни пациента.
В настоящее время экспертами рекомендован трехступенчатый подход к диагностике первичного гиперальдостеронизма (скрининг, подтверждение диагноза, определение специфического подтипа патологии). Для первичного гиперальдостеронизма характерно высокое содержание альдостерона в крови при низком уровне ренина. Но показатели распределения альдостерона и ренина в нормальной популяции и группах пациентов с эссенциальной гипертензией или первичным гиперальдостеронизмом в значительной степени перекрываются. Поэтому в качестве начального скринингового исследования рекомендовано определение альдостерон-ренинового соотношения (АРС). Диагностическая информативность АРС превосходит информативность отдельно применяемых показателей – уровней альдостерона, калия (оба теста характеризуются низкой чувствительностью при скрининге), ренина (низкая специфичность).
Отрицательный результат скрининговой оценки АРС свидетельствует об отсутствии первичного гиперальдостеронизма. При получении положительного результата по АРС рекомендовано проведение одного из подтверждающих тестов. В подтверждающем тесте с солевой нагрузкой в виде инфузии физиологического раствора уровень альдостерона после инфузии менее 50 пг/мл свидетельствует о низкой вероятности первичного гиперальдостеронизма, уровень альдостерона более 100 пг/мл – о высокой вероятности этого диагноза (подробнее о вариантах подтверждающих тестов см. «Клинические рекомендации по материалам консенсуса по первичному гиперальдостеронизму».Кроме увеличенного значения альдостерон-ренинового соотношения, некоторые эксперты рассматривают в качестве дополнительного критерия обязательное наличие достаточно высокого уровня альдостерона (>150 пг/мл). Другие специалисты считают, что следует избегать формального значения границы нормы для альдостерона, но необходимо учитывать, что существует повышенная вероятность ложноположительного результата альдостерон-ренинового соотношения при низком уровне ренина. Таким образом, не существует жестких указаний по диагностическому значению АРС. Важно понимать все относительные преимущества и недостатки методики, принимать во внимание влияющие на результат АРС факторы для корректной индивидуальной интерпретации данных.
Исследование АРС на фоне приема некоторых лекарственных препаратов или несоблюдение правил взятия крови могут исказить результаты. Поэтому его следует проводить после соответствующей подготовки (см. ниже). При интерпретации результатов следует учитывать, что, как и для других биохимических тестов, в этом исследовании возможно получение ложноположительных или ложноотрицательных результатов. В случае сомнения в правильности результата исследование необходимо повторить. Влияние приема лекарств и других условий – см. табл. в разделе «Интерпретация».
Литература
- Клинические рекомендации по материалам консенсуса по первичному гиперальдостеронизму. Российская ассоциация эндокринологов, ФГБУ ЭНЦ МЗ России. 2008. http://www.endocrincentr.ru/images/material-images/2008(1).pdf.
- Funder J.W., Carey R.M., Fardella C., Gomez-Sanchez C.E., Mantero F., Stowasser M., Young W.F. Jr., Montori V.M. Case detection, diagnosis, and treatment of patients with primary aldosteronism: An endocrine society clinical practice guideline. Journal of Clinical Endocrinology and Metabolism. 2008;93(9):3266-3281.
- Материалы фирмы DiaSorin.
Раздел 3.23 — Кредиты для квалификационных скважин с низкой продуктивностью, 34 Tex. Admin. Код § 3.23
Ток через Рег. 46, №15; 9 апреля 2021 г.
Раздел 3.23 — Кредиты для квалификационных низкодебитных скважин (a) Определения. Следующие слова и термины, когда они используются в этом разделе, имеют следующие значения, если контекст явно не указывает иное. (1) Комиссия — Железнодорожная комиссия Техаса. (2) Оператор — лицо, ответственное в соответствии с законом или правилами комиссии за физическую эксплуатацию ствола скважины или аренду. (3) Средняя налогооблагаемая цена на газ — Средняя цена на газ за предыдущие три месяца с использованием индекса цен, указанного в Налоговом кодексе, § 201.059 (b). Среднее значение будет вычислено путем деления цены закрытия на каждый рыночный день на общее количество рыночных дней за трехмесячный период. Затем эта средняя цена будет скорректирована до долларов 2005 года. (4) Квалификационная низкодебитная скважина — Газовая скважина, добывающая не более 90 млн куб. Футов газа в сутки, за исключением газа, сжигаемого в факелах в соответствии с правилами комиссии, в течение трехмесячного периода до даты начала освобождение.В целях квалификации скважины добыча в день определяется путем вычисления средней дневной добычи из скважины с использованием большего из значений месячной добычи из скважины, указанных в ежемесячных отчетах по добыче скважин, представленных в комиссию, и ежемесячной добычи из скважины. также сообщается в отчетах производителя, предоставленных контроллеру в соответствии с § 201.203 Налогового кодекса (Отчет производителя), включая любые поправки, внесенные в эти отчеты. (b) Для каждой скважины, подпадающей под действие этого раздела, контролеру потребуется следующая информация от оператора скважины. (1) Копии ежемесячных производственных отчетов, сдаваемых в комиссию по аренде на трехмесячный период. (2) Если аренда объединена, оператор должен предоставить копии ежемесячных производственных отчетов, представленных в комиссию по объединенной аренде, и распределение производства по каждой аренде в разрешении на объединение с подтверждающей документацией за трехмесячный период до до даты начала освобождения. Подтверждающая документация может включать, помимо прочего, отчет о состоянии газовой скважины G-10 железнодорожной комиссии Техаса для договоров аренды, или инженерное исследование пластов в стволе скважины, или замерные испытания, проведенные по договорам аренды. (3) Заполненное заявление контролера об освобождении скважины. (4) Дата, когда по договору аренды соблюдены трехмесячные ограничения по добыче, которые квалифицируют скважину как низкодебитную. (5) Заявление о том, уплачен ли налог на газ в течение периодов после даты вступления в силу освобождения, и имя стороны, уплатившей налог. (c) Среднемесячная налогооблагаемая цена на газ будет опубликована в Техасском регистре в месяц, следующий за месяцем фактической добычи.Эта публикация уведомит налогоплательщика о праве на освобождение за месяц до даты подачи отчета. Налоговый кодекс, § 201.059 (c), (d) и (e) будет использоваться для определения кредита, применимого за каждый отчетный месяц. (1) Если среднемесячная налогооблагаемая цена на газ превышает 3,50 долларов США за тысячу кубических футов, в этом отчетном месяце освобождения не будет. (2) Если среднемесячная налогооблагаемая цена на газ составляет более 3,00 долларов США за куб.м, но не более 3,50 долларов США за куб.м., будет предоставлен кредит в размере 25% для газа, проданного из квалифицированной скважины за этот отчетный месяц. (3) Если среднемесячная налогооблагаемая цена на газ составляет более 2,50 долларов США за кубометр, но не более 3 долларов США за кубометр, будет предоставлен кредит в размере 50% для газа, проданного из квалифицированной скважины в этом отчетном месяце. (4) Если среднемесячная налогооблагаемая цена на газ не превышает 2,50 долларов США за тысячу кубических футов, будет предоставлен 100% кредит для газа, проданного из квалифицированной скважины за этот отчетный месяц. (d) Если налог уплачивается по полной ставке, предусмотренной главой 201 Налогового кодекса, на газ, добытый на дату или после даты вступления в силу освобождения от налога, но до даты утверждения контролером заявки на освобождение от налога, Оператор имеет право на зачет налогов, подлежащих уплате в соответствии с главой 201 Налогового кодекса, в сумме, равной зачету, утвержденному на этот период.Чтобы получить кредит, оператор или сторона, уплачивающая налог, должны обратиться к контролеру, заполнив исправленные отчеты. Если сторона, не являющаяся оператором, перечислила налог, оператор должен предоставить стороне, которая уплатила налог, копию утвержденной формы заявления контролера, которая квалифицировала скважину для освобождения от налога.34 Tex. Admin. Кодекс § 3.23
Положения этого §3.23 вступили в силу 27 декабря 2006 г., 31 TexReg 10346; с поправками, вступающими в силу 6 ноября 2011 г., 36 TexReg 7345; С поправками, внесенными Техасским регистром, том 45, номер 06, 7 февраля 2020 г., TexReg 917, эфф.11 февраля 2020 г.Нефть в Нью-Мексико, природный газ и метан Не контролируют низкопродуктивные скважины, сообщает EDF
Согласно анализу, проведенному Фондом защиты окружающей среды (EDF), проект правил штата Нью-Мексико, ограничивающих выбросы метана в нефтегазовом секторе, должен быть усилен за счет устранения лазеек для низкодебитных скважин.
Предлагаемые правила были обнародованы в июле Департаментом окружающей среды Нью-Мексико (NMED) и Департаментом энергетики, полезных ископаемых и природных ресурсов (EMNRD).
EDF в пятницу опубликовала обновленную оценку выбросов метана из нефти и газа в штате, согласно которой годовые выбросы оцениваются в 1,1 миллиона метрических тонн. Это соответствует краткосрочному воздействию на климат 25 угольных электростанций и примерно в пять раз выше, чем предполагают текущие данные Агентства по охране окружающей среды, сообщает EDF.
Помимо метана, промышленность также выбрасывает около 337 500 метрических тонн образующих смог летучих органических соединений (ЛОС) ежегодно, как выяснили исследователи.
В исследовании смоделировано влияние отмены исключений, которые в настоящее время включены в проект правил.
Правила NMED и EMNRD в том виде, в каком они написаны, будут объединены для сокращения выбросов метана на 21% в масштабе штата, «по сравнению с возможным сокращением на 56% с набором комплексных политик, доказавших свою рентабельность в других нефтегазодобывающих регионах». Команда EDF найдена.
Что касается летучих органических соединений, которые выбрасываются вместе с метаном при нефтегазовых операциях, предлагаемые правила приведут к сокращению выбросов на 19% против возможных 58%, заявили исследователи.
Средства контроля метана, предложенные NMED, не применяются к низкопродуктивным скважинам или скважинам с определенными пороговыми значениями загрязнения, что означает, что 95% буровых площадок в Нью-Мексико будут освобождены от этого, сказал EDF, добавив: «Это серьезно ограничивает возможные частичные сокращения загрязнения. штата, подверженного риску превышения федеральных стандартов по озону ».
Анализ «ясно показывает, что агентство должно устранить предлагаемые лазейки», чтобы выполнить миссию Департамента окружающей среды по защите News Mexicans от загрязнения, сказал Голдштейн.
EDF использовала прошедшие экспертную оценку спутниковые данные в сочетании с обширными исследовательскими исследованиями для проведения последней оценки выбросов.
«Благодаря невероятным масштабам и частоте спутниковых наблюдений, а также обширным и постоянным полевым исследованиям EDF в Пермском бассейне, ученые теперь имеют беспрецедентное представление о выбросах с месторождений и Нью-Мексико, а также о том, что потребуется для их сокращения», — заявили исследователи. .
Влияние на экономику
EDF оценивает стоимость потерянного метана, основного компонента природного газа, ежегодно составляет 271 миллион долларов в Нью-Мексико, что эквивалентно 43 миллионам долларов потерянных налогов и доходов штата.
Администрация губернатора Мишель Лухан Гришам «имеет прекрасную возможность принять значимые меры безопасности, которые устранят лазейки и максимизируют выгоды для здоровья и климата», — сказал Джон Голдштейн из EDF, директор по регуляторным и законодательным вопросам. «Эти данные ясно говорят о том, что необходимы более активные действия для защиты сообществ и семей по всему штату и достижения цели губернатора по установлению ведущих правил нации…
«Существуют надежные и рентабельные решения для сокращения выбросов, и как наука, так и экономика указывают на важность принятия надежных окончательных правил.”
Анализ, проведенный Synapse Energy Economics Inc., предлагаемых EDF комплексных мер по контролю метана показал, что они являются «чрезвычайно рентабельными, обеспечивая 30% окупаемости инвестиций для жителей Новой Зеландии, включая 1,2 миллиарда долларов на предотвращение затрат, связанных с отсутствием качества воздуха, и 126 миллионов долларов на пользу для здоровья человека. . »
Лухан Гришам в 2019 году издал распоряжение о сокращении выбросов парниковых газов (ПГ) как минимум на 45% к 2030 году по сравнению с уровнями 2005 года и обязывающее NMED и EMNRD ввести в действие обязательные меры контроля над метаном в масштабах штата для нефтегазовых компаний.
Губернатор Колорадо Джаред Полис также нацелен на дальнейшее сокращение выбросов метана в рамках недавно обнародованной Дорожной карты сокращения выбросов парниковых газов, которая нацелена на сокращение общего загрязнения парниковыми газами на 50% к 2030 году по сравнению с уровнями 2005 года.
На федеральном уровне администрация Трампа стремилась отменить контроль над метаном времен Обамы посредством действий исполнительной власти и в судах. Ожидается, что избранный президент Джозеф Р. Байден-младший возглавит новую инициативу по ограничению выбросов парниковых газов, когда он вступит в должность в январе.
9 Фонды, приносящие доход для низкодоходной рыночной среды
Размер текста
Время мечтатьЧто в наши дни почти так же сложно забить, как вакцинация против Covid-19? Даже жестче, чем новейшая игровая консоль? Инвестиции, приносящие действительно высокий доход.
Облигации с высокой доходностью больше не соответствуют этому ярлыку.Нежелательные облигации впервые упали ниже 4%, сообщает Barron’s Alexandra Scaggs. Корпоративный долг инвестиционного уровня в среднем приносит менее 2%, в то время как казначейские выпуски приносят в среднем менее 1% из-за более коротких сроков погашения, привязанных к 0-0,25%, намеченной Федеральной резервной системой для ставки по однодневным федеральным фондам. После вычета инфляции реальные процентные ставки намного ниже нуля, а пятилетние TIPS или казначейские ценные бумаги с защитой от инфляции дают минус 1.90%.
По словам одного из ветеранов рынка облигаций, это превратило «рай для заемщиков» в ад на земле для инвесторов, которые зависят от текущего дохода. (Для этой статьи он должен скрывать свою личность в целях соблюдения требований, учитывая, что он идентифицировал отдельные ценные бумаги Barron’s . Вы легко узнаете его как человека, которого часто цитируют в финансовой прессе и видят по телевидению.)
Для обеспечения того, что он описывает как «чрезмерную» доходность, он использует групповые фонды закрытого типа вместе с одним торгуемым на бирже фондом, которые платят более 8%.
CEF выпускают определенное количество акций, которые могут торговаться выше или, чаще, ниже их базовой стоимости чистых активов. Кроме того, большинство CEF используют кредитное плечо, занимая деньги под сверхнизкие краткосрочные процентные ставки для увеличения активов, которые они могут купить.
Это увеличивает доходность портфелей при условии, что они приносят больше, чем затраты по займам. Поскольку ФРС удерживает краткосрочные ставки на низком уровне, вероятно, до 2023 года, этот ключевой риск кредитного плеча сводится к минимуму. Действительно, структуры с использованием заемных средств обращают подавление процентных ставок центральным банком в пользу инвестора.
Наш эксперт отбирает список CEF, чтобы выбрать те, которые имеют устойчивое распространение. Он выбирает фонды, которые инвестируют в облигации, конвертируемые облигации, акции и инвестиционные фонды в недвижимость. Он также выбирает те, которые выписывают или продают опционы колл против портфелей для получения дохода. Но он избегает большинства энергетических фондов, которые, по его словам, по большей части неэффективны.
Он согласился поделиться некоторыми из своих выборов с читателями Barron. Это эклектичный список, но он подчеркивает, что диверсификация фондов для снижения их риска также важна.Их ликвидность также важна, особенно для его институциональных клиентов.
Источники: Cefconnect.com, сайты фондов.
Константа в группе — высокая доходность, варьирующаяся от средних 8% до двузначных величин, выше 11%.Они также не полагаются на облигации для получения прибыли, обычно используя ценные бумаги с фиксированной доходностью в качестве диверсификатора. Некоторые также торгуют со значительными скидками по отношению к чистой стоимости активов, что обеспечивает запас прочности, а также возможность прироста капитала, если эти скидки сузятся.
Как уже отмечалось, написание опционов является неотъемлемой частью многих стратегий фондов. Продажа опционов приносит текущий доход, но ограничивает потенциал роста портфеля.
Это демонстрируется Global X Nasdaq-100 с покрытием Cal l биржевой фонд (тикер: QYLD), который вернул примерно 10.06% за последние 12 месяцев, по данным Morningstar. Но Invesco QQQ Trust (QQQ), который отслеживает эти 100 крупнейших нефинансовых акций Nasdaq — технологических звезд, которые возглавили ралли, — за этот период принес 46,55%.
Однако целью этой стратегии является доход, а не прирост капитала. Эти средства тоже небезопасны. Но инвесторам, ищущим источник дохода в этой падающей доходности среде, они должны принести облегчение.
Исправления и дополнения: Тикер для фонда Kayne Anderson MLP / Midstream — KYN.В более ранней версии таблицы в этой статье было неверно указано, что это MYN.
Напишите Randall W. Forsyth по адресу [email protected]
Определение низкозатратного производителя
Что такое производитель с низкими издержками?
Низкозатратный производитель — это компания, которая предоставляет товары или услуги по низкой цене. В целом производители с низкими издержками используют эффект масштаба для реализации своей стратегии низких цен. Потребители, чувствительные к изменениям цен, с большей вероятностью будут делать покупки в магазинах, предлагающих самые низкие цены, особенно если товар или услуга относительно однородны.
У производителей с низкими издержками есть другой вариант: устанавливать цены на товары или услуги на том же уровне, что и у их конкурентов, и поддерживать более высокую маржу.
Как работают производители с низкими издержками
Производитель с низкими издержками может изготовить товар-заменитель или предоставить услугу-заменитель по более низкой цене, чем другие компании. Они могут устанавливать цены на свои товары на уровне рыночных или чуть ниже рыночных, что подрывает конкуренцию. Поступая таким образом, компании могут увеличить свою долю на рынке и увеличить прибыль.
Эти товары и услуги обычно являются основными продуктами питания, пользующимися большим спросом. У них, как правило, есть легкодоступные заменители, предлагаемые многими конкурентами на рынке. Потребительские товары, производимые дешевыми производителями, обычно включают предметы домашнего обихода, чистящие средства, продукты питания, напитки — любые предметы, которые потребители не могут вырезать. Специальные товары, такие как ювелирные изделия, элитные автомобили и некоторые виды одежды, как правило, не производятся дешевыми производителями.
В отличие от своих более крупных конкурентов, многие производители с низкими издержками стремятся сосредоточиться на одном или нескольких различных потребительских сегментах, что может помочь им снизить свои затраты, увеличить долю рынка и сохранить высокую прибыль.
Возьмем, к примеру, сеть супермаркетов Aldi. Его площадь намного меньше, чем у среднего супермаркета, но он по-прежнему может конкурировать со своими именитыми конкурентами в крупных масштабах. Он предлагает гораздо меньший выбор товаров, большинство из которых производится под его родовой торговой маркой, и компания может снизить цены намного ниже своих конкурентов. Пройдите по его проходам, и вы заметите, что там есть вещи, которые люди обычно покупают на регулярной основе.
Как стать недорогим производителем
Требования к тому, чтобы стать производителем с низкими издержками, велики, поскольку существует довольно высокий барьер для входа на рынок.Быть конкурентоспособным на рынке означает привлекать капитал или иметь достаточно резервов для достижения достаточно большой экономии от масштаба, чтобы обеспечить явное ценовое преимущество перед конкурентами. Это требование — одна из причин, по которой многие компании не могут быть производителями с низкими издержками.
Для того, чтобы стать производителем с низкими издержками, существует высокий барьер для входа, поскольку для этого требуется большой капитал.
Как только это будет достигнуто, компаниям необходимо будет инвестировать в технологии, которые позволят снизить производственные затраты, одновременно увеличивая объем производства.Важное предостережение заключается в том, что фирмы должны следить за спросом и не жертвовать своим брендом.
Ключевые выводы
- Производитель с низкими издержками — это компания, которая использует эффект масштаба для предоставления товаров или услуг по низкой цене.
- Эти товары и услуги обычно являются основными продуктами питания, пользующимися большим спросом, такими как предметы домашнего обихода, продукты питания и напитки.
- Чтобы стать производителем с низкими издержками, требуется большой капитал и другие технологические достижения для увеличения производства и сокращения затрат.
- Walmart — один из самых известных производителей недорогих товаров в мире.
Пример недорогого производителя
Walmart, вероятно, лучший пример недорогого производителя с огромной экономией на масштабе. Компания управляет 11 443 розничными точками под разными знаменами в 24 странах. У Walmart есть несколько стратегий, которые не позволяют конкурировать с конкурентами. Он может снизить стоимость продаваемых товаров, приобретая и покупая самостоятельно.А из-за своего огромного присутствия Walmart может в значительной степени контролировать своих поставщиков.
Компания также может осуществлять распространение через довольно недорогую сеть и вложила значительные средства в свои технологии, чтобы идти в ногу со своей клиентской базой. Это дает компании преимущество, позволяя ей лучше обслуживать потребителей, совершающих покупки в магазинах и в Интернете.
Низкосерийное производство — обзор
2.10 Резюме результатов главы
В этой главе излагаются элементарные принципы инженерной экономики с фундаментальными техническими и экономическими характеристиками производства AM.На основе этого упрощенного анализа определены следующие коммерчески надежные возможности для применения AM.
Пакетные сценарии (Рис. 2.4 — Зона 1 )При относительно низких объемах производства удельные затраты AM ниже, чем при традиционном производстве. Коммерческие сценарии с поддержкой серийного производства включают предпроизводственную разработку, производство единичных единиц и серийное производство небольшими партиями.
Сценарии с учетом сложности (рис.2.4 — Зона 2 )Затраты, связанные с высокой геометрической сложностью, потенциально ниже для методов AM, чем для традиционного производства. Сценарии с учетом сложности включают топологически оптимизированные системы и серийное производство геометрии высокой сложности.
Приложения сверхвысокой сложности (Рис. 2.4 — Зона 3 )Предельная сложность традиционного производства меньше, чем для методов AM. Эти сценарии предоставляют уникальную возможность для производства дорогостоящих конструкций, в которых традиционные методы производства невозможны любой ценой.Приложения включают в себя решетчатые структуры высокой сложности, функционально интегрированные конструкции и генеративно оптимизированные конструкции.
Массовая настройка ( раздел 2.3.4 )AM обеспечивает значительную гибкость и автоматизацию производства. Эти возможности позволяют создать новую парадигму массовой настройки, при которой объем производства квалифицируется как массовое производство, но изготовленный продукт настраивается в соответствии с требованиями к дизайну конкретного продукта. Коммерческая реализация массовой настройки требует понимания экономики генеративных методов проектирования таким образом, чтобы инвестиции в автономные инструменты DFAM были экономически вознаграждены.
Эти выявленные возможности не исключают друг друга и могут быть объединены для увеличения коммерческой выгоды. В частности, эти расширенные коммерческие возможности включают мелкосерийное производство для сценариев высокой или сверхвысокой сложности. Эти сценарии извлекают выгоду из экономического преимущества как небольшого объема, так и высокой сложности и потенциально могут принести значительную коммерческую выгоду, например, медицинские имплантаты, ориентированные на пациента (глава 7), и фантомы для радиационной дозиметрии, созданные генеративным способом (глава 9).
Эта глава начинается с упрощенного анализа инженерной экономики (раздел 2.1). Это упрощение обеспечивает полезный экономический инструмент DFAM для управления экономическими аспектами многих приложений AM. Более детальное понимание AM позволяет выявить определенные недостатки в отношении этих результатов, которые необходимо учитывать при анализе экономических показателей предлагаемого сценария AM. Эти предостережения включают следующее.
Парадокс снижения стоимости при увеличении сложностиВ ответ на повышенную сложность AM может фактически обеспечить снижение стоимости продукта.Это снижение затрат происходит из-за снижения производственных затрат, особенно связанных с уменьшением использования материала и машинного времени. Такое поведение парадоксально по сравнению с традиционным производством и может обеспечить экономическое преимущество для компонентов со значительной сложностью конструкции. Эту возможность следует рассматривать параллельно с рассмотрением потенциально ошибочной независимости AM от затрат (раздел 2.5), чтобы избежать завышенного прогноза стоимости продуктов AM высокой сложности.
Парадокс пересечения объемов для оптимальной стоимостиAM предоставляет значительные возможности для предпроизводственной проверки и концептуального проектирования.Для таких сценариев, когда фактический объем производства точно не известен, существуют экономические выгоды от сохранения производства AM по мере роста производства, в том числе: снижение экономического барьера для входа на рынок для производителей с ограниченным стартовым капиталом; экономический риск-менеджмент при неопределенных объемах производства; а также возможность беспрепятственного изменения атрибутов дизайна продукта в процессе производства. Кроме того, если рассматривается переход к методам TM, соответствующие экономические показатели должны быть пересчитаны во время ввода TM в эксплуатацию , что приведет к расширенному порогу, для которого методы AM являются оптимальными (Раздел 2.7).
Ошибочное предположение о независимости затрат AMУпрощенное представление инженерной экономики для AM и традиционных методов основано на затратах на проектирование, обеспечивающих незначительный вклад в себестоимость единицы (раздел 2.8). Случаи, для которых это предположение действительно, существуют, однако отсутствие этих идеализированных условий может привести к недооценке производственных затрат, и этого можно избежать, используя технические инструменты DFAM и методы генеративного проектирования для управления вкладом затрат на проектирование, как показано в Главы 3 и 7 Глава 3 Глава 7 соответственно.
В этой главе представлен стратегический обзор технико-экономических ограничений конструкции , связанных с методами AM. Основная цель состоит в том, чтобы систематически предупреждать проектировщиков и коммерческих менеджеров о технических ограничениях и , связанных с экономическими ограничениями, присущими надежному коммерческому внедрению технологии AM. Важно понимать упрощенный экономический анализ таким образом, чтобы возможности AM были четко сформулированы для потенциальных клиентов, тем самым увеличивая коммерческий pull для применения AM.Однако крайне важно, чтобы специалисты-практики AM знали об ограничениях этого упрощенного экономического анализа, чтобы они могли предотвратить ошибочные коммерческие решения и продвигать передовые возможности для технологий AM.
Критичность проницательного технико-экономического понимания дизайна высока, поскольку без этого понимания коммерческие предприятия терпят неудачу или достигают успеха лишь от случая к случаю, что приводит к краху доверия отрасли к лежащей в основе технологии AM. Несмотря на эту критичность, существует относительно мало исследований в области технико-экономического проектирования, возможно, из-за многодисциплинарного характера требуемой технической и экономической экспертизы.Для тех исследовательских групп, которые способны внести свой вклад в это требование, существуют значительные возможности для создания технико-экономических инструментов DFAM, включая экспертные системы бухгалтерского учета, которые воплощают тонкое понимание возможностей и потенциальных ловушек для потенциальных приложений AM; системы, которые иллюстрируют (и количественно определяют) относительные экономические риски и возможности, связанные с эволюционным и революционным проектированием; опубликовал тематические исследования об опыте успешных (и неудачных) коммерческих предприятий AM; и исследование динамических эффектов, связанных с коммерческим применением AM, включая, например, парадокс пересечения объемов, который возникает при рассмотрении перехода производства AM к TM.
Спросите эксперта: возможно, потребуется разделить участок с малопродуктивным пионом.
Мы быстро приближаемся к зиме, но есть проблемы с садоводством, которые вызывают у вас сомнения. Если у вас есть вопросы, обратитесь к Ask an Expert, онлайн-инструменту вопросов и ответов, предоставляемому Консультационной службой Университета штата Орегон. Преподаватели ОГУ и мастера-садовники отвечают на запросы в течение двух рабочих дней, обычно меньше. Чтобы задать вопрос, просто зайдите на сайт OSU Extension , введите его и укажите округ, в котором вы живете.Вот некоторые из них, которые задают другие садоводы. Что твое?
Q: На некоторых из моих пионов не было ни одного или большого количества цветков. У них были здоровые на вид листья и другие части растения. Вероятно, они прожили в одном и том же месте более 10 лет. Что я могу сделать сейчас, чтобы на этих растениях появилось больше цветков, или мне нужно выкопать их и посадить новые? — Округ Малтнома
A: Две наиболее вероятные причины того, что эти прекрасные растения перестают цвести, заключаются в том, что они слишком глубоко засыпаны или слишком большие кусты.И то, и другое может быть связано с вашим долгоживущим патчем.
Это простые проблемы, которые нужно преодолеть, и они принесут вам больше цветов. Со временем вокруг кроны могут накапливаться почва, листья и мульча. Растение, которое изначально было посажено на один-два дюйма ниже поверхности, теперь может иметь глубину четырех дюймов. Слишком большой куст можно разделить новыми растениями для вас или друзей.
Перемещение и деление пионов обычно проводят осенью. Это дает корням возможность немного подрасти за зиму до начала весеннего роста.Если вы находитесь в более теплом или более защищенном месте, вы можете сделать это сейчас и добавить слой мульчи вокруг растений для дополнительной защиты. (снимая его с кроны весной, конечно)
Поднимите все растение и стряхните с него немного почвы. Определите «глаза», которые будут способствовать росту весной. Разделите корону ножом или ножницами так, чтобы на каждой секции было от трех до пяти глазков и несколько хороших корней. Затем снова посадите на прежнее место, на новые места или в контейнер, чтобы поделиться с другими садоводами.Убедитесь, что верхняя часть кроны находится всего на 1-2 дюйма ниже уровня почвы.
Приходите весной, примените дозу корма для роз / цветов, как указано на упаковке.
Еще одна мысль — деревья в вашем или соседнем дворе, возможно, добавляли тени этому месту, уменьшая потребность пионов в солнечном свете. Если проблема в тени, комок можно переместить в более солнечное место.
Для получения дополнительной информации от любителя пионов ознакомьтесь с этой статьей. — Клаудиа Грот, главный садовник OSU
Служба расширения RugosaOSU
В: Я пытаюсь укротить стоянку роз ругоза, которая оставалась разрастаться годами.В прошлом году я сократил их примерно с 8 футов до 5 или 6. Они энергично отреагировали ростом на дне. Могу ли я подрезать их до уровня бедер? Или мне следует продолжать делать работу постепенно? — Округ Марион
A: Роза Rugosa охватывает широкий спектр сортов с различными характеристиками, но ваш сорт выглядит так, как будто он цветет на древесине текущего сезона, поскольку плоды появляются на кончиках побегов там, где должны были быть цветы, что характерно для растения, которые цветут на новой древесине. Таким образом, было бы нормально обрезать их сейчас, так как вы не будете обрезать цветочные почки.
Другой вопрос — может ли обрезка сейчас вызвать повреждение зимой. Однако эти растения настолько выносливы, что очень маловероятно, что в наших краях сейчас может произойти какая-либо травма от холода, поэтому я думаю, что небольшая обрезка для вашего предложения будет хорошей. — Нил Белл, садовод по расширению OSU
В: Я являюсь хозяином автодомов в Benton Oaks RV Park, который принадлежит и управляется округом Бентон. Нам подарили довольно большой компостер год назад, и никто толком не знает, как им пользоваться.Я попросил переместить его на мой сайт и использовать. Мы производим так много пищевых отходов, живя в жилых автофургонах, поскольку в наших холодильниках так мало места, и когда мы сбрасываем мусорный контейнер в компактор, я замечаю, сколько тратится впустую, что, по моему мнению, можно компостировать. Я просто не знаю, с чего начать, и все, что можно и что нельзя делать. Мы действительно хотели бы в конечном итоге производить компост в больших количествах, потому что мы закупаем так много мульчи и удобрений для ухода за нашими участками. Если я смогу показать, что это выполнимо и устойчиво, это будет иметь большое значение для достижения этой цели.Есть ли кто-нибудь, кто захочет показать мне, как это начать? — Округ Бентон
О: Я тоже живу в округе Бентон и имею более чем 20-летний опыт работы с переворачивающимся компостером, который я использую в основном для пищевых отходов.
- Поскольку пищевые отходы влажные, начните с заполнения компостера на 2/3 абсорбирующим веществом — в вашем случае использованные подстилки для стойл были бы идеальными. Если в подстилку входят моча и навоз, тем лучше. Другие абсорбирующие материалы включают лиственные листья и измельченную офисную бумагу.
- Добавляйте пищевые отходы по мере их образования и переворачивайте при каждом добавлении.
- Поскольку он находится над землей, не стоит беспокоиться о том, что дикие животные могут попасть в него. В то же время, поскольку воздух может циркулировать вокруг массы материала в стакане, мне не удалось заставить мой нагреться. Нагревание ускоряет процесс компостирования.
Лично, когда материалы в стакане очень мусорные и мокрые, я выгружаю их в стационарный компостер. Я предполагаю, что Republic Services предоставляет услуги по вывозу мусора на территорию ярмарки.Если да, то почему бы не посмотреть, не выдадут ли вам компостер Earth Machine? Затем компост можно перевернуть в достаточной степени, чтобы стабилизировать легко компостируемые материалы (еда, навоз, моча). Для получения дополнительной информации о компостировании перейдите к этой статье. — Линда Брюэр, почвовед из ОГУ
Как справиться с низким запасом грудного молока
Предполагая, что вы кормите ребенка грудью, «если вы кормите грудью часто, каждые два часа и у вашего ребенка хороший захват, но он не набирает вес, тогда у вас, вероятно, мало запасов », — сказал Виснер.Родителям часто советуют вести журнал мокрых и грязных подгузников в качестве заместителя для кормления, но, по словам Виснера, ребенок может производить нужное количество подгузников, но все равно не получать вполне достаточно молока . Вот почему, по словам Виснера, ключевым моментом является взвешивание вашего ребенка голым на тех же весах. Доктор Шульвольф также рассказал о том, как трудно понять, сколько грудного ребенка потребляет, и рекомендовал ранние и частые проверки веса. Розен подчеркнул важность посещения педиатра на третий день жизни ребенка.«Многие матери не обращаются к педиатру раньше, чем через два-три дня после того, как вернутся домой из больницы, — когда ребенку исполнится четыре или пять дней, — и за это время многое может пойти не так», — сказала она.
Если у вас мало молока, воспользуйтесь добавкой грудного молока или смеси
«Если у кого-то мало молока, мы говорим, что сначала кормите ребенка, затем защитите молоко и наслаждайтесь», — сказала Мелисса Морелли-Уолш, IBCLC, CNM сертифицированный консультант по грудному вскармливанию и сертифицированная медсестра-акушерка в Нью-Йоркском университете в Лангоне.Вы можете дополнить рацион ребенка своим собственным грудным молоком (путем сцеживания), донорским молоком или смесью. «У младенцев всегда остается немного молока после кормления. С помощью сцеживания его можно получить, а также стимулирует организм производить больше молока », — сказал Розен. Нью-Йоркский университет недавно начал предлагать донорское молоко новорожденным, нуждающимся в добавках. По словам Виснера, молочная смесь также может помочь в кормлении грудью, отметив, что очень голодный ребенок не будет кормить грудью так же хорошо, как тот, которого кормят. Исследование, проведенное в 2018 году, показало, что очень раннее употребление молочных смесей, до начала продуктивности зрелого молока, не мешает исключительно грудному вскармливанию в 1 месяц.
Чтобы сохранить отношения грудного вскармливания, дополнительное молоко следует предлагать в небольших количествах после сеанса медсестры, возможно, используя технику ритмичного кормления из бутылочки (более медленное кормление с широкой соской из бутылочки, которая включает в себя много удержания и связывания, аналогичные к сестринскому опыту). Доктор Шульвольф рекомендовал использовать формулу стратегически. «Вы можете использовать смесь среди ночи — партнеру нравится поддерживать связь с ребенком, кормя из бутылочки, а мама наслаждается четырехчасовым сном», — сказала она.
[Как кормить смесью грудного молока и смеси ]
Лечить проблемы со здоровьем и повышать спрос для увеличения предложения
Если у вас мало запасов, вы должны сначала лечить любые предполагаемые медицинские проблемы, — сказал Виснер. . Возможно, вам придется начать прием лекарств, если у вас проблемы с щитовидной железой, или сменить лекарство, если у вас P.C.O.S. или диабет. Задержка плаценты, которая может мешать снабжению, может быть обнаружена и ее необходимо удалить. Если у вас есть I.G.T., консультант по грудному вскармливанию, может помочь определить, какой объем молока вам подходит.
Затем увеличьте подачу за счет частого кормления с последующим сцеживанием. «Это классический спрос и предложение», — сказал Морелли-Уолш. Выкачивание удаляет остатки молока и, таким образом, создает на него дополнительный спрос. В некоторых случаях недостаток молока возникает и усугубляется, когда ребенок плохо выводит молоко. У ребенка может быть уздечка языка — состояние, при котором полоса ткани прикрепляет кончик языка ко дну рта, затрудняя сосание; уздечка языка может быть исправлена процедурой, при которой ткань разрезается.Плохой захват или просто слабая сосательная способность также могут создавать проблемы. По словам Розена, сцеживание от двух до трех унций после кормления — вероятный признак того, что ваш ребенок плохо сосет, а у ребенка, родившегося до 39 недель беременности, повышенный риск.
Квалифицированный консультант по грудному вскармливанию может помочь вам составить план увеличения количества корма и кормления вашего ребенка с учетом специфики вашей ситуации. По словам Розена, взвешенные кормления за 24-часовой период могут точно показать, сколько ест ваш ребенок. «Вам нужно гораздо больше поддержки и участия, чем пятиминутное посещение консультанта по грудному вскармливанию в больнице», — сказал Розен.
Установленный запас может уменьшиться, если количество сеансов кормления сократится, что может произойти, когда мать вернется к работе или ребенок начнет спать дольше по ночам. Девон Клемент, послеродовая доула и основатель компании «Mama’s Best Friend», компании по уходу за новорожденными, сказала, что, когда это случилось с одним из ее клиентов, «мы добавили сеанс сцеживания перед тем, как мама пошла спать, и ранним утром перед тем, как лечить ребенка. ребенок проснулся », и ее запасы вернулись.Что касается печенья, чая и трав в период лактации? Нет никаких доказательств того, что они помогают, но также нет доказательств того, что они могут навредить, если только мать не отдает предпочтение питью чая в период кормления грудью, а не частым сеансам кормления.

