Что такое ретросинтез в органической химии. Как применять ретросинтетический анализ для решения задач. Какие ключевые вопросы нужно задавать при выполнении ретросинтеза. На что обращать внимание при планировании синтеза органических соединений.
Что такое ретросинтез и почему он важен в органической химии
Ретросинтез — это мощный инструмент планирования синтеза сложных органических молекул. Суть метода заключается в мысленном расчленении целевой молекулы на более простые фрагменты, двигаясь от продукта к исходным веществам. Такой обратный анализ позволяет определить оптимальный путь синтеза.
Ключевые преимущества ретросинтетического подхода:
- Позволяет разбить сложную задачу на простые этапы
- Помогает выявить ключевые промежуточные соединения
- Дает возможность рассмотреть разные пути синтеза и выбрать лучший
- Развивает навыки стратегического мышления в органической химии
Овладение методом ретросинтеза крайне важно для успешного решения задач по органическому синтезу. Это незаменимый инструмент как для студентов, так и для опытных химиков-синтетиков.
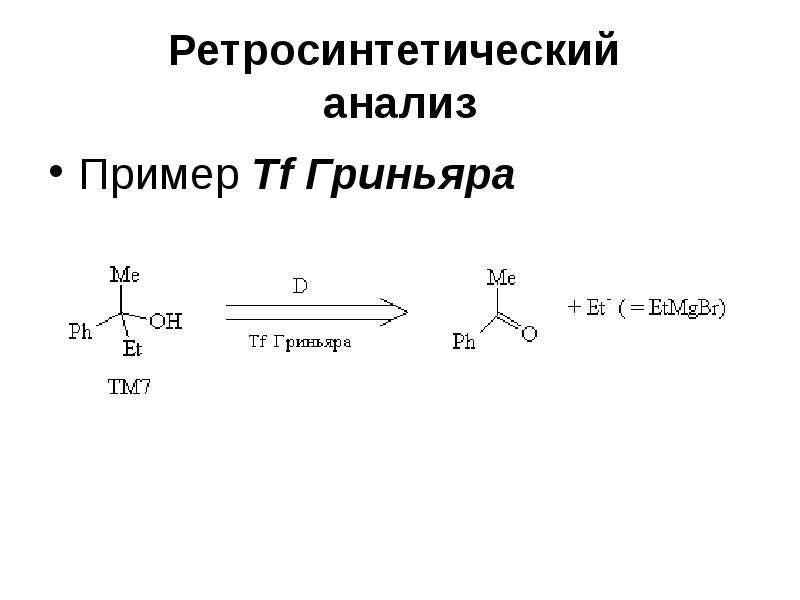
Основные этапы ретросинтетического анализа
При выполнении ретросинтеза рекомендуется придерживаться следующего алгоритма:
- Внимательно изучите структуру целевой молекулы
- Определите ключевые функциональные группы и структурные фрагменты
- Подумайте, какими реакциями можно получить эти группы/фрагменты
- Мысленно «разрежьте» молекулу по ключевым связям
- Выявите возможные синтоны и их синтетические эквиваленты
- Предложите вероятные исходные соединения
- Проанализируйте несколько альтернативных путей синтеза
- Выберите оптимальную стратегию синтеза
Последовательно отвечая на эти вопросы, вы сможете эффективно спланировать синтез даже очень сложных органических молекул.
Ключевые вопросы при выполнении ретросинтеза
При ретросинтетическом анализе крайне важно задавать себе правильные вопросы. Вот некоторые из них:
- Какие функциональные группы присутствуют в целевой молекуле?
- Какими реакциями можно получить эти функциональные группы?
- Какие связи в молекуле наиболее логично разорвать?
- Какие синтоны можно выделить в структуре молекулы?
- Какие реагенты могут быть синтетическими эквивалентами этих синтонов?
- Какие исходные вещества потребуются для синтеза?
- В какой последовательности лучше проводить реакции?
Отвечая на эти вопросы, вы сможете системно подойти к решению задачи и не упустить важные детали.
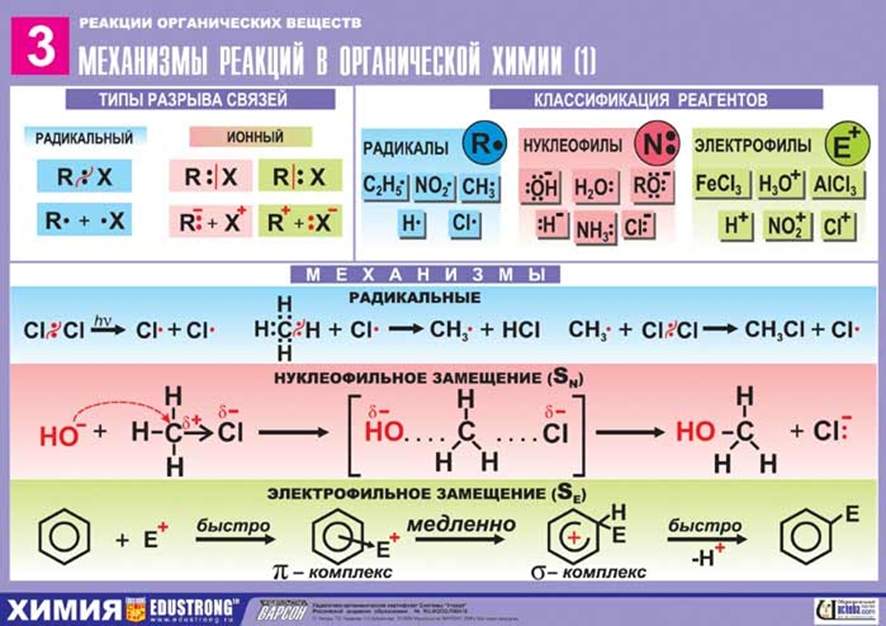
Как выявить ключевые структурные фрагменты в молекуле
Умение выделять ключевые фрагменты в структуре целевой молекулы — важнейший навык при ретросинтезе. Вот на что следует обращать внимание:
- Карбонильные группы (альдегиды, кетоны, карбоновые кислоты)
- Двойные и тройные связи
- Ароматические циклы
- Гетероциклы
- Стереоцентры
- Галогены и другие заместители
Анализ этих структурных элементов поможет определить ключевые трансформации, необходимые для синтеза целевой молекулы.
Выбор оптимальной стратегии синтеза
При планировании синтеза важно рассмотреть несколько альтернативных путей и выбрать оптимальный. Критерии выбора:
- Доступность и стоимость исходных реагентов
- Количество стадий синтеза
- Суммарный выход продукта
- Селективность ключевых стадий
- Возможность побочных реакций
- Простота выделения и очистки продуктов
Тщательный анализ этих факторов позволит выбрать наиболее эффективный путь синтеза целевой молекулы.
Типичные ошибки при выполнении ретросинтеза
При ретросинтетическом анализе важно избегать распространенных ошибок:
- Недостаточный анализ структуры целевой молекулы
- Пропуск важных функциональных групп
- Неверный выбор разрываемых связей
- Игнорирование стереохимических аспектов
- Использование неподходящих реагентов
- Неправильная последовательность стадий
Внимательность и системный подход помогут избежать этих ошибок и успешно решить задачу.
Применение ретросинтеза для решения сложных синтетических задач
Метод ретросинтеза особенно эффективен при планировании синтеза сложных органических молекул, таких как:
- Природные соединения (алкалоиды, терпены, стероиды)
- Лекарственные препараты
- Макроциклические соединения
- Полициклические системы
- Молекулы со множественными стереоцентрами
Ретросинтетический анализ позволяет разработать эффективные стратегии получения даже самых сложных органических структур.
Анализ наоборот, 6 букв, первая буква С — кроссворды и сканворды
синтез
Слово «синтез» состоит из 6 букв:
— первая буква С
— вторая буква И
— третья буква Н
— четвертая буква Т
— пятая буква Е
— шестая буква З
Посмотреть значние слова «синтез» в словаре.
Альтернативные варианты определений к слову «синтез», всего найдено — 22 варианта:
- «Слияние» по-философски
- Антоним анализ
- Греческое «соединение»
- Движение от частей к целому в познании, вообще соединение, обобщение
- Метод исследования
- Метод исследования внутренних органов непосредственным осмотром их специальными приборами
- Напарник анализа
- Научное сочленение
- Обратное анализу
- Переведите на греческий язык «объединение»
- Получение сложных соединений из простых
- Процесс слияния в физике
- Процесс, обратный анализу
- Реакция, во время которой из двух простых веществ получают химическое соединение
- Сбор элементов в систему
- Слияние (филос)
- Слияние элементов
- Соединение элементов целое
- Способ исследования
- Тезис + антитезис
- Третий этап триады Гегеля
- Что получится, если соединить тезис и антитезис?
Другие вопросы:
- Вскопанная полоса на плантации
- Соседи венгров и хорватов
- Знаменитый русский историк
- Платан с «восточной» пропиской
- В ВМФ лицо младш.
 комсостава
комсостава - Древнегреческая металлическая, реже глиняная чаша для пиров и возлияний богам
- Посещение больного врачом
- Между Невадой и Вашингтоном
- Скромная должность в науке
- Какое озеро прозвали морем Сахары?
| Вопрос 1 из 20 Процесс действия по значению глагола закрапывать | |
| замусливание | зондирование |
| закрапывание | заквашивание |
Только что искали: ляеамн сейчас пургапр 1 секунда назад к л а п р ь о 1 секунда назад щербаковское 1 секунда назад п р и х с а т и 1 секунда назад р о е т р е н 1 секунда назад недожорова 1 секунда назад унонсиа 1 секунда назад размолачивавший 1 секунда назад антидатируйся 1 секунда назад капюшон 2 секунды назад нестройность в игре на музыкальных инструментах 2 секунды назад подталкивающеюся 2 секунды назад абвгдеёжзйикрлмнопрстуфхцчшщ 2 секунды назад эпиграф 2 секунды назад
Эксперимент в Великобритании может преодолеть препятствие для термоядерного синтеза
- Пол Ринкон
- Редактор отдела науки, Би-би-си
Подпишитесь на нашу рассылку ”Контекст”: она поможет вам разобраться в событиях.
Автор фото, UKAEA
Подпись к фото,Новый дизайн охлаждения термоядерных реакторов обещает сделать их более доступными
Эксперты считают, что первые результаты эксперимента в Великобритании могут помочь устранить препятствия на пути к коммерческой энергетике, основанной на ядерном синтезе.
Исследователи полагают, что нашли способ удалить избыточное тепло, выделяемое в ходе реакций синтеза.
Избыточный нагрев материалов реактора может их попросту расплавить, что сильно ограничивает время его работы.
- Атомная энергетика: быть или не быть?
Новая система отвода тепла, чем-то напоминающая выхлопную систему автомобиля, позволит снизить температуру в десять раз.
Испытания проводились в рамках эксперимента по модернизации ядерного синтеза Mast (Mega Amp Spherical Tokamak) в Калэме в графстве Оксфордшир. Устройство стоимостью 55 млн фунтов было введено в эксплуатацию в октябре прошлого года после сборки, продолжавшейся семь лет.
Ядерный синтез — это попытка воспроизвести процессы, идущие в глубине Солнца и других звезд, на Земле
Неуловимый синтез
Главная задача сегодня — это получить на выходе реакции синтеза больше энергии, чем затрачивается на ее поддержание. Добиться этого пока не удается.
Ядерная энергия сегодня получается в процессе деления ядер тяжелых элементов, например урана или плутония, на более легкие. В процессе деления появляются новые, более легкие элементы и выделяются нейтроны, которые, как и осколки деления, обладают значительной кинетической энергией. В результате их столкновений с осколками и друг другом выделяется значительное количества тепла, которое мы и используем.
Реакция ядерного синтеза, наоборот, соединяет ядра легких элементов, например водорода, в одно более тяжелое. При этом выделяется огромное количество энергии, которую физики во всем мире пока безуспешно пытаются поймать и заставить работать.
Один из распространенных методов термоядерного синтеза — это реактор типа «токамак», в котором для управления заряженным газом — или плазмой — внутри контейнера, формой напоминающего пончик, используются мощные магнитные поля.
Автор фото, John Lawrence
Подпись к фото,Так токамак выглядит изнутри
Установка термоядерного синтеза в настоящее время строится на юге Франции в рамках международного проекта под названием Iter. Профессор Иэн Чапман, исполнительный директор Управления по атомной энергии Соединенного Королевства (UKAEA), сказал, что он будет иметь решающее значение для демонстрации возможности внедрения термоядерной энергии в сеть.
Однако профессор указывает, что размер и стоимость Iter означают, что «если каждый раз, когда вы хотите построить термоядерный реактор, вы должны собирать такую сумму денег, — проникновение [термоядерной энергии] на рынок будет определяться экономикой, а не технологиями».
«Горячее Солнца»
Модернизация Mast — это одна из попыток сконструировать своего рода шаблон для более компактных и дешевых термоядерных реакторов. В нем используется инновационная конструкция — сферический токамак, — позволяющая втиснуть ядерное топливо в пространство высотой 4,4 метра и шириной 4 метра. Для сравнения, защитный сосуд, который Iter будет использовать для управления реакциями термоядерного синтеза, имеет высоту 11,4 м и ширину 19,4 м.
В нем используется инновационная конструкция — сферический токамак, — позволяющая втиснуть ядерное топливо в пространство высотой 4,4 метра и шириной 4 метра. Для сравнения, защитный сосуд, который Iter будет использовать для управления реакциями термоядерного синтеза, имеет высоту 11,4 м и ширину 19,4 м.
У столь скромного размера камеры Mast есть и обратная сторона: «Вы создаете что-то более горячее, чем Солнце … в меньшем объеме. Вывести оттуда тепло — большая проблема», — говорит профессор Чапман.
- Ручное солнце. Когда термоядерные реакторы станут реальностью
Пропустить Подкаст и продолжить чтение.
Подкаст
Что это было?
Мы быстро, просто и понятно объясняем, что случилось, почему это важно и что будет дальше.
эпизоды
Конец истории Подкаст
Внутри токамака плазма достигает температуры 100 миллионов градусов. Без системы охлаждения, способной справиться с такими температурами, материалы в конструкции пришлось бы регулярно заменять, что сказалось бы на времени работы электростанции.
Без системы охлаждения, способной справиться с такими температурами, материалы в конструкции пришлось бы регулярно заменять, что сказалось бы на времени работы электростанции.
Новая выхлопная система Super-X, испытываемая в Калхэме, позволит компонентам будущих коммерческих токамаков прослужить намного дольше. Это должно значительно увеличить доступность электростанций, улучшить их экономическую жизнеспособность и снизить стоимость термоядерного электричества.
Испытания на Mast показали, как минимум, десятикратное снижение нагрева материалов с помощью системы Super-X.
Исследователи заявили, что эти результаты кардинально изменили перспективы создания термоядерных электростанций, которые могли бы обеспечивать доступную и эффективную электроэнергию. Термоядерный синтез может стать чистым и практически безграничным источником энергии, что особенно важно в условиях изменения климата.
- 10 лет ядерной катастрофе на «Фукусиме-1».
 Что происходит сейчас и каковы последствия?
Что происходит сейчас и каковы последствия?
Доктор Эндрю Кирк, ведущий научный сотрудник проекта модернизации Mast, сказал, что результаты эксперимента стали «моментом, к которому наша команда шла почти 10 лет».
«Мы разработали программу модернизации Mast, чтобы решить проблему выхлопа компактных термоядерных реакторов, и есть признаки того, что нам это удалось, — говорит Кирк. — Super-X снижает нагрев выхлопной системы от температуры паяльной лампы до температуры автомобильного двигателя. Это означает, что ее, возможно, придется менять только один раз за все время службы силовой установки».
Успех выхлопной системы для Mast поможет реализации планов по созданию прототипа термоядерной электростанции под названием Step в Великобритании. Ожидается, что она войдет в строй где-то в 2040-х годах.
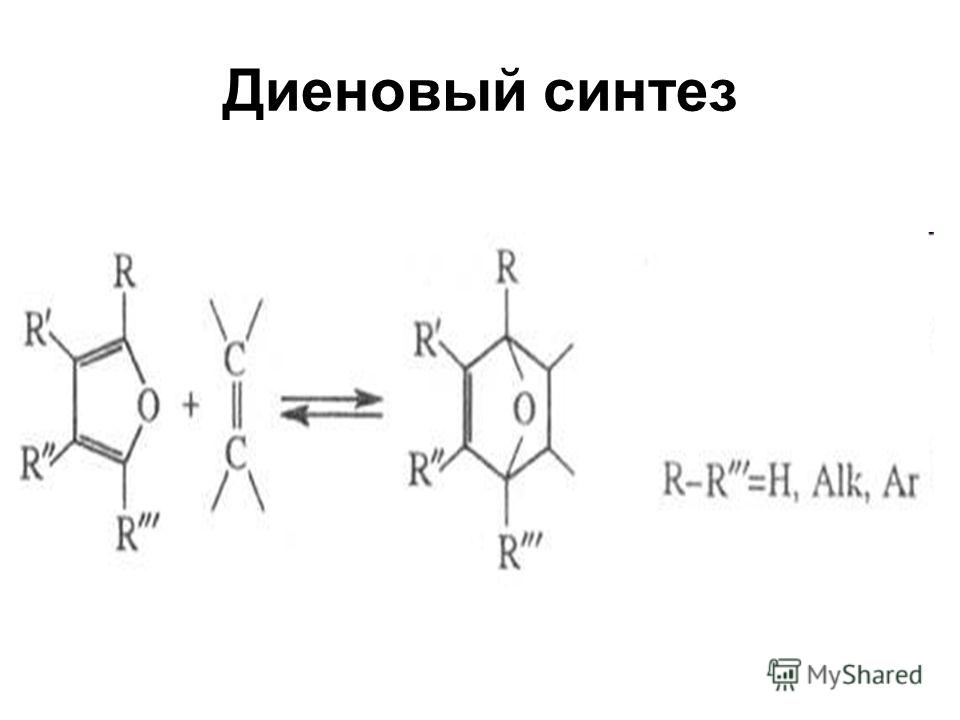
Ретросинтез Учебное пособие по органической химии
В органической химии синтез и ретросинтез идут рука об руку.
Хотя четкого разграничения нет, мне нравится думать о синтезе как о передовом мышлении, а о ретросинтезе как о обратном .
Синтез — это тема, которая обычно вводится в органическую химию 1 сразу после изучения алкиновых реакций. Вы будете использовать его снова и снова по мере накопления реакций, которым вы научились.
Вот почему так важно просмотреть прошлые темы , прежде чем переходить к следующей главе. При изучении новых тем вас могут попросить выполнить ретросинтез, который включает в себя извлечение пяти различных реакций из пяти разных глав.
Давайте вернемся…
Ретро = Назад
Синтез = Процесс объединения более простых реакций для образования химического соединения/молекулы.
В вашем курсе органической химии это представлено в виде сложной молекулы, которую вам затем предлагается синтезировать из заданной исходной молекулы или набора условий реакции.
-> Вам могут дать определенный реагент и попросить синтезировать продукт.
Например:
«Синтез транс-3,4-дибромгексана из этина».
-> Вас могут попросить синтезировать продукт при наборе расплывчатых или специфических условий реакции.
Например:
«Синтезировать 2-бутанон с использованием любых неорганических реагентов. Используйте двухуглеродные алкилгалогениды в качестве единственного источника углерода».
Встречали ли вы похожие вопросы в домашних заданиях, викторинах или практических экзаменах?
Что вы думаете?
Многие студенты будут смотреть на процесс и паниковать;
И в упомянутой панике начали рисовать все и вся, что приходит на ум, без четкого процесса или представления о том, куда они направляются.
Мне нравится системный подход к решению проблем.
Мне нравится планировать свои действия и точно знать, что я должен делать.
И, что более важно, я верю, что этот процесс поможет мне снова и снова получать правильные результаты.
Как можно быстрее!
Чем систематичнее ваш подход, тем больше вероятность того, что вы получите все компоненты реакции. Поэтому меньше шансов, что вы что-то пропустите.
Это ключ. Получите все компоненты и сведите к минимуму количество потерянных баллов на экзамене.
Прежде чем углубляться в сами проблемы, вам нужно знать, куда вы идете.
Вы должны убедиться, что ваши действия в конечном итоге окупятся, и вы получите желаемый продукт.
- Что такое же?
- Что изменилось?
- Как добиться этой разницы?
Что такое же?
Прежде чем добавлять в молекулу новые группы, нужно посмотреть, с чем уже можно работать.
Мы будем использовать анализ, описанный в учебнике по синтезу , при анализе того, что присутствует в реагенте.
СЧИТАЙТЕ УГЛЕРОДА!!!
(так много очков теряется из-за отсутствия подсчета.)
Сколько атомов углерода присутствует в реагент и продукт ?
Это поможет вам идентифицировать реакции удлинения цепи или расщепления.
Найдите любые
неуглеродных атомов и функциональных групп .Что еще на молекуле в реагенте и продукте?
Ищите
местоположение реактивности на молекуле.
Реакционная способность молекулы относится к расположению реакционноспособных атомов или функциональных групп.
Например, 2-хлорпропан имеет реакционную способность по второму углероду. Cl — хорошая уходящая группа. Это позволяет провести ряд реакций:
- Удаление для создания пи-связи (E1 или E2)
- Замена для получения другой функциональной группы в виде входящего нуклеофила (SN1 или SN2)
- И многое другое…
Это ваша подсказка относительно того, ГДЕ начать реакцию.
Сравните каждую из этих функций с конечным продуктом.
Внимательно отмечайте все, что заменяет , потому что наша цель при проведении ретросинтеза будет именно такой: выяснить, КАК выполнять эти преобразования, что подводит меня к вопросу 2.
Чем отличается?
- Если число атомов углерода изменится, на сколько?
- Сколько атомов углерода было добавлено или удалено?
- Если функциональные группы или реактивность изменились , что было заменено и чем?
- Сколько новый Добавлено групп?
После того, как мы определили, что одинаково, а что отличается, мы задаем самый важный вопрос:
КАК я могу осуществить эту трансформацию?
Этот вопрос состоит из двух частей.
1) Для коротких задач на синтез ответ прост.
Какая ОДНА реакция превратит исходную молекулу x в конечный продукт y ?
Например, 2-йодопропан в пропилен.
Что такое же?
И реагент, и продукт имеют три атома углерода.
Чем отличается?
Реагент содержит галоген у углерода №2.
Продукт имеет пи-связь между бывшим углеродом 2 и углеродом 3.
Как я могу осуществить это преобразование?
Удалите галоген, используя сильное основание для реакции E2 или даже слабое основание и нагревание для реакции E1. Оба будут предоставлять один и тот же продукт.
Подсказка: если вы сомневаетесь, выберите E2 вместо E1. Это быстрее, точнее и имеет меньшую конкуренцию (E1 против SN1), при правильных условиях. Вы также можете контролировать продукт, выбирая более (Зайцев) или менее замещенную (Big Bulky Base) пи-связь.
2) Но ваш профессор вряд ли даст вам такую простую одношаговую трансформацию для ретросинтеза.

Давайте попробуем.
Например, вас попросили преобразовать 2-хлорбутан в 1-бутанол.
Все еще относительно простое преобразование, но мы больше не рассматриваем простую одностадийную реакцию.
Применяется тот же набор вопросов, которые по-прежнему будут направлять вас к продукту.
Что такое же?
В реагенте и продукте всего четыре атома углерода.
У нас есть одна функциональная группа в реагенте и продукте.
Чем отличается?
Реагент содержит галоген; продукт содержит спирт.
Реакционная способность молекулы сместилась с углерода №2 на углерод №1.
Какие реакции я знаю, чтобы осуществить это преобразование?
Внезапно ответ не так ясен, но все же не невозможен.
В предыдущем примере мы смогли быстро ответить на этот вопрос.
ОДНА единственная реакция превратила нашу исходную молекулу в желаемый продукт.
Здесь не так много!
Здесь проявляется истинная сила ретросинтетического анализа.
Давайте разберемся.
У нас есть хлор в исходной молекуле и спирт в продукте.
Хотя мы ДЕЙСТВИТЕЛЬНО знаем о реакции превращения Cl в OH (SN2), это произойдет на том же самом углероде. Нам нужен ОН на другом углероде.
Итак, давайте сделаем еще один шаг или, лучше сказать, сделаем шаг назад .
Ретросинтез — это устаревшее мышление, поэтому давайте начнем с продукта.
Если продукт представляет собой спирт на первичном углероде, какая известная мне реакция даст мне спирт на первичном углероде?
Первичный и вторичный указывает мне на антимарковниковский спирт, который говорит мне, что мне нужно провести реакцию присоединения алкена в антимарковниковских условиях.
Если сделать еще один шаг назад, мне нужен алкен.
Пока не беспокойтесь о реагентах. Гораздо проще продумать молекул, сначала , а затем вернуться и заполнить недостающие реагенты, как описано в руководстве по синтезу.
Теперь мы относимся к алкену как к нашему новому продукту и снова задаем тот же вопрос.
Сравнение реагента с алкеном,
Знаю ли я реакцию, которая либо осуществит это превращение, либо приблизит меня к этому?
Абсолютно да, простая реакция исключения, как мы видели выше.
Однако на этот раз мы не можем просто использовать сильное основание, потому что пи-связь будет благоприятствовать более замещенному продукту Зайцева 2-бутену.
Вместо этого нам нужна реакция отщепления, которая заставит пи-связь образоваться на менее замещенном первичном и вторичном углероде.
Какой реагент выполнит это «антизайцевское» или элиминирование Хоффмана?
Нам нужно «тройное B» или большое громоздкое основание
Трет-бутоксид
Но давайте не будем сейчас беспокоиться о трет-бутоксиде, вместо этого давайте просто признаем тот факт, что мы МОЖЕМ взаимодействовать с 2-хлорбутаном с образованием 1-бутена и нарисуем это. трансформация.
После того, как все промежуточные продукты будут перенесены из продукта в реагент, быстро проследите последовательность от реагента к продукту, чтобы убедиться, что она выглядит правильно и имеет смысл.
Теперь спросите себя:
Какой реагент будет выполнять каждое преобразование?
Задавайте себе этот вопрос по очереди, когда будете заполнять условия реакции и завершать последовательность ретросинтеза.
Мы начинаем со вторичного галогена и формируем менее замещенную пи-связь.
Для этого требуется сильное основание трет-бутоксид, как мы уже намекали выше.
В то время как некоторые профессора примут это как есть, другим потребуется полный набор условий.
Давайте используем трет-бутоксид калия, растворенный в его собственном конъюгированном трет-бутаноле спирта, и нагреваем, чтобы помочь провести эту реакцию. Напомним, что реакции E2 предпочитают тепло. Теперь, когда у нас есть асимметричный алкен, нам нужна реакция присоединения алкена, которая позволит спирту присоединиться к первичному углероду или антимарковниковскому положению. Сразу приходит на ум
Окисление гидроборированием.
Добавим Bh4, THF в NaOH и h3O2.
И вот оно, пошаговое преобразование с использованием реагентов.
Синтез + ретросинтетический анализ.
Начните с в обратном порядке думая всякий раз, когда можете.
Вы знаете выражение «задним числом 20/20?»
Вот на что мы рассчитываем.
Глядя на свой продукт и держа в уме только свой реагент, вы можете задать очень, очень важный вопрос:
Как выглядела эта молекула всего за ОДИН шаг до того, чтобы я мог образовать функциональную группу x?
Эта форма ретросинтетического анализа поможет вам быстро идентифицировать одно промежуточное соединение за раз, вплоть до исходной молекулы.
Давайте попробуем что-нибудь посложнее.
Допустим, вас попросили начать с бензола для синтеза 2-нитробензойной кислоты.
Что такое же?
Реагент и продукт имеют бензольное кольцо.
Чем отличается?
Продукт представляет собой дизамещенный бензол. Заместители имеют орто-соотношение.
Мы добавили карбоновую кислоту и нитрогруппу.
Какие реакции я знаю для осуществления этих превращений?
Учитывая, что у нас происходит более одной реакции, всегда обращайте внимание на то, как реакции влияют друг на друга.
Мы можем добавить карбоновую кислоту посредством алкилирования Фриделя-Крафтса с последующим окислением.
Мы можем добавить нитрогруппу через EAS Nitration.
НО, вот с чем вы должны быть осторожны:
Группы орто друг к другу.
Как NO2, так и карбоновая кислота являются деактивирующими группами EAS с метанаправляющими эффектами.
Давайте все обдумаем, прежде чем реагировать.
Если карбоновая кислота получена в результате алкилирования FC, алкильная группа до окисления является орто/пара-директором.
Это хорошо.
Но как нам гарантировать, что мы получим положение орто , а не пара ?
Нужна еще одна реакция, которой нет в продукте.
Нам нужна блокирующая группа в пара-позиции, чтобы гарантировать, что орто-группа является единственной доступной группой.
Все эти мысли должны быстро пробежать у вас в голове. Пока нет необходимости записывать реакции, хотя я люблю помечать молекулы как «заметку для себя»
Теперь, когда мы знаем, куда идем, ретросинтез завершен, и мы можем взять эту реакцию из реагента. к продукту напрямую.
Начнем с алкилирования Фриделя-Крафтса. Размер вашей углеродной цепи не имеет значения, так как окисление боковой цепи отрезает лишние атомы углерода.
Возьмем этилхлорид в FeCl3, что даст нам этилбензол:
Теперь у нас есть орто-парадиректор, поэтому давайте добавим блокирующую группу .
Сульфирование EAS добавит объемистый SO3H в пара-положении.
При блокировке пара мы можем провести другую реакцию, имея в виду следующее:
- Этил по-прежнему является орто/пара директором, но пара заблокирована!
- Сера является частично положительной и метанаправляющей группой.

ОБЕ группы направляются к углероду №2 рядом с этильной группой, что нам и нужно.
Далее проводим нитрование ЭАС, заставляя нитрогруппу орто к этилу и мета к сульфату.
Разбавленная кислота затем удалит блокирующую группу из пара-положения, оставив вам метагруппу нитро к этильной группе.
Здесь многие студенты теряют баллы.
Они так взволнованы мыслью обо всем этом, что забывают, что это не желаемый продукт.
ВСЕГДА возвращайтесь к первому вопросу, чтобы ничего не забыть.
Что мы забыли?
Этил не является нашей целью.
Нам нужна карбоновая кислота.
Введите перманганат калия с окислительной способностью боковой цепи, превращая бензильную позицию в карбоновую кислоту для нашего конечного продукта.
После этого выполните всю последовательность, чтобы убедиться, что все ваши реагенты и промежуточные продукты работают вместе и имеют смысл, и мы закончили.
Эти же мысли можно применить к любой задаче ретросинтеза от двух до 100 и более шагов. Хорошо, возможно, я преувеличиваю, надеюсь, ваш профессор ограничит ваши проблемы ретросинтеза тремя-семью шагами.
Хорошо, возможно, я преувеличиваю, надеюсь, ваш профессор ограничит ваши проблемы ретросинтеза тремя-семью шагами.
Теперь, когда у вас есть основы подхода к ретросинтезу, вам понадобится прочная основа. Я рекомендую вернуться к просмотру всех ключевых реакций, рассмотренных в вашем семестре, чтобы они были свежими и готовыми к использованию по мере необходимости.
Используйте My Syllabus Companion , чтобы быстро найти учебные пособия, видеоролики и шпаргалки по типичным реакциям органической химии.
Я хотел бы услышать от вас
Вы чувствуете себя лучше в ретросинтезе и оставаясь на правильном пути к полной оценке каждой проблемы? Позвольте мне знать в комментариях ниже.
Высокоэффективный обратный (5’→3′) синтез сложных ДНК-микрочипов
. 2018 10 октября; 8 (1): 15099.doi: 10.1038/s41598-018-33311-3.
Катрин Хёльц
1
, Джулия К Хой
2
, Эрика Шауди
1
, Вероника Сомоса
2
, Джори Литард
3
, Марк М. Сомоса
4
Сомоса
4
Принадлежности
- 1 Институт неорганической химии, химический факультет Венского университета, Вена, Австрия.
- 2 Кафедра физиологической химии, Лаборатория биоактивных ароматических соединений Кристиана Доплера, химический факультет Венского университета, Вена, Австрия.
- 3 Институт неорганической химии, химический факультет Венского университета, Вена, Австрия. [email protected].
- 4 Институт неорганической химии, химический факультет Венского университета, Вена, Австрия. [email protected].
- PMID: 30305718
- PMCID: PMC6180089
-
DOI:
10.
 1038/с41598-018-33311-3
1038/с41598-018-33311-3
Бесплатная статья ЧВК
Катрин Хёльц и др. Научный представитель .
Бесплатная статья ЧВК
. 2018 Октябрь 10;8(1):15099.
doi: 10.1038/s41598-018-33311-3.
Авторы
Катрин Хёльц 1 , Джулия К Хой 2 , Эрика Шауди 1 , Вероника Сомоса 2 , Джори Литард 3 , Марк М. Сомоса 4
Принадлежности
- 1 Институт неорганической химии, химический факультет Венского университета, Вена, Австрия.

- 2 Кафедра физиологической химии, Лаборатория биоактивных ароматических соединений Кристиана Доплера, химический факультет Венского университета, Вена, Австрия.
- 3 Институт неорганической химии, химический факультет Венского университета, Вена, Австрия. [email protected].
- 4 Институт неорганической химии, химический факультет Венского университета, Вена, Австрия. [email protected].
- PMID: 30305718
- PMCID: PMC6180089
-
DOI:
10.
 1038/с41598-018-33311-3
1038/с41598-018-33311-3
Абстрактный
ДНК-микрочипы являются важными аналитическими инструментами в генетике и недавно обнаружили множество новых биотехнологических ролей в приложениях, требующих свободных 3′-концевых гидроксильных групп, особенно в качестве отправной точки для ферментативного удлинения с помощью ДНК- или РНК-полимераз. Здесь мы демонстрируем высокоэффективный обратный синтез сложных массивов ДНК с использованием фотолитографического подхода. Этот метод аналогичен обычному твердофазному синтезу, но в нем используются фосфорамидиты с фотолабильной защитной группой бензоил-2-(2-нитрофенил)-пропоксикарбонила (BzNPPOC) на 3′-гидроксильной группе. Использование BzNPPOC с фотолитической эффективностью, более чем вдвое превышающей фотолитическую эффективность 2-(2-нитрофенил)пропоксикарбонила (NPPOC), ранее использовавшегося для 5’→3′-синтеза, в сочетании с дополнительной оптимизацией реакций сочетания и окисления приводит к приблизительно 3-кратное повышение эффективности обратного синтеза сложных массивов олигонуклеотидов ДНК. Эффективность связывания обратных фосфорамидитов такая же, как и у обычных фосфорамидитов, что приводит к сопоставимым выходам. Микрочипы поверхности ДНК, связанные на 5′-конце и со свободными 3′-гидроксильными концами, могут быть синтезированы быстро и с такой же высокой эффективностью ступенчатого связывания, как и микрочипы с использованием обычного синтеза 3’→5′.
Эффективность связывания обратных фосфорамидитов такая же, как и у обычных фосфорамидитов, что приводит к сопоставимым выходам. Микрочипы поверхности ДНК, связанные на 5′-конце и со свободными 3′-гидроксильными концами, могут быть синтезированы быстро и с такой же высокой эффективностью ступенчатого связывания, как и микрочипы с использованием обычного синтеза 3’→5′.
Заявление о конфликте интересов
Авторы заявляют об отсутствии конкурирующих интересов.
Цифры
Рисунок 1
Химические структуры ДНК фосфорамидитов…
Рисунок 1
Химическая структура фосфорамидитов ДНК с NPPOC и BzNPPOC 3′- или 5′-OH, защищающими…
фигура 1 Химическая структура фосфорамидитов ДНК с защитными группами NPPOC и BzNPPOC 3′- или 5′-OH.
Рисунок 2
Репрезентативный цикл синтеза без масок,…
Рисунок 2
Репрезентативный цикл синтеза в безмасочном светонаправленном синтезе обратных микрочипов с использованием фосфорамидитов 3′-BzNPPOC.…
фигура 2 Репрезентативный цикл синтеза в безмасочном светонаправленном синтезе обратных микрочипов с использованием фосфорамидитов 3′-BzNPPOC. Мощный УФ-светодиод используется для фотодезащиты 3′-ОН в присутствии слабого органического основания. Окончательное химическое снятие защиты удаляет цианоэтильные и основные защитные группы. Необязательный этап блокировки с помощью 5′-DMTr-dT блокирует любые оставшиеся непрореагировавшие 3′-гидроксильные группы. Репрезентативное время шага дано, но зависит от конкретных экспериментальных параметров и целей.
Рисунок 3
Интенсивность флуоресценции на основе гибридизации для 25mer…
Рисунок 3
Интенсивность флуоресценции на основе гибридизации для 25-мерных микрочипов, синтезированных с использованием градиента УФ-света.…
Рисунок 3 Интенсивность флуоресценции на основе гибридизации для 25-мерных микрочипов, синтезированных с использованием градиента УФ-света. Микроматрицы были синтезированы либо с фосфорамидитами NPPOC, либо с BzNPPOC. ( A ) 3’→5′ синтез с мономерами 5′-NPPOC и 5′-BzNPPOC. ( B ) Синтез 5’→3′ с мономерами 3′-NPPOC и 3′-BzNPPOC. На обоих графиках значения облучения для синтезов BzNPPOC умножены на 2,2, а положение исходных данных указано пунктирными линиями. Как для NPPOC, так и для BzNPPOC для 3′-фотолиза требуется на 45% больше света, чем для 5′-фотолиза.
Как для NPPOC, так и для BzNPPOC для 3′-фотолиза требуется на 45% больше света, чем для 5′-фотолиза.
Рисунок 4
Исследование оптимального сцепления…
Рисунок 4
Исследование оптимального времени связывания и снятия защиты для 3′- и 5′-NPPOC и…
Рисунок 4Исследование оптимального времени связывания и снятия защиты для фосфорамидитов, защищенных 3′- и 5′-NPPOC и BzNPPOC. Все точки данных соответствуют синтезу одного и того же олигонуклеотида со смешанными основаниями 25mer. Время соединения составляло 15, 30, 45 или 60 секунд. Снятие защитных групп азотистого основания и фосфата проводили в смеси EDA/EtOH 1:1 (об./об.) в течение 2 часов ( A ) или 12 часов ( B ).
Рисунок 5
Интенсивность флуоресценции от гибридизированного прямого…
Рисунок 5
Интенсивность флуоресценции последовательно синтезированных прямых (3′→5′) и обратных (5′→3′) цепей ДНК…
Рисунок 5 Интенсивность флуоресценции гибридизованных прямых (3’→5′) и обратных (5’→3′) цепей ДНК, синтезированных последовательно на одном и том же субстрате. Цепи были синтезированы с использованием 3′- и 5′-NPPOC фосфорамидитов или мономеров 3′- и 5′-BzNPPOC. Гибридизацию проводили с эквимолярной смесью 5′- и 3′-Cy3-меченых комплементарных олигонуклеотидов. Столбики ошибок — это SEM. Пунктирные линии указывают на ожидаемую ~ 6% тенденцию интенсивности гибридизации для последовательно синтезированных 25-меров олигонуклеотидов.
Цепи были синтезированы с использованием 3′- и 5′-NPPOC фосфорамидитов или мономеров 3′- и 5′-BzNPPOC. Гибридизацию проводили с эквимолярной смесью 5′- и 3′-Cy3-меченых комплементарных олигонуклеотидов. Столбики ошибок — это SEM. Пунктирные линии указывают на ожидаемую ~ 6% тенденцию интенсивности гибридизации для последовательно синтезированных 25-меров олигонуклеотидов.
Рисунок 6
Левый . Графики рассеяния…
Рисунок 6
Левый . Диаграммы рассеяния данных, обработанных RMA, из синтезированных микрочипов экспрессии генов…
Рисунок 6 Слева . Диаграммы рассеяния данных, обработанных RMA, для микрочипов экспрессии генов, синтезированных в направлении 3’→5’ (вверху) и в направлении 5’→3’ (внизу). Отклонения от диагональной линии указывают на дифференциальную экспрессию генов. Право . Подробная информация о сканированных изображениях с разрешением 2,5 мкм из микрочипов экспрессии генов, синтезированных в направлении 3 ‘→ 5 ‘(вверху) и в направлении 5 ‘→ 3’ (внизу).
Отклонения от диагональной линии указывают на дифференциальную экспрессию генов. Право . Подробная информация о сканированных изображениях с разрешением 2,5 мкм из микрочипов экспрессии генов, синтезированных в направлении 3 ‘→ 5 ‘(вверху) и в направлении 5 ‘→ 3’ (внизу).
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
-
Синтез 5′-О-фосфорамидитов с фотолабильной 3′-О-защитной группой.
Бейер М., Хохайзель Д.Д. Бейер М. и соавт. Curr Protoc Nucleic Acid Chem. 2004 Сентябрь; Глава 12: Раздел 12.3. дои: 10.1002/0471142700.nc1203s17. Curr Protoc Nucleic Acid Chem. 2004. PMID: 18428919 Обзор.
-
Экспресс-фотолитографический синтез микрочипов ДНК с оптимизированным химическим составом и высокоэффективными фотолабильными группами.

Сак М., Хёльц К., Холик А.К., Кречи Н., Сомоса В., Стенгеле К.П., Сомоса М.М. Сак М. и др. J Нанобиотехнология. 2016 2 марта; 14:14. doi: 10.1186/s12951-016-0166-0. J Нанобиотехнология. 2016. PMID: 26936369 Бесплатная статья ЧВК.
-
Микрочипы РНК высокой плотности, синтезированные in situ с помощью фотолитографии.
Лиетард Дж., Амер Д., Дамха М.Дж., Сомоса М.М. Лиетард Дж. и соавт. Angew Chem Int Ed Engl. 2018 12 ноября; 57 (46): 15257-15261. doi: 10.1002/anie.201806895. Epub 2018 19 октября. Angew Chem Int Ed Engl. 2018. PMID: 30187993 Бесплатная статья ЧВК.
-
2,2,5,5-тетраметилпирролидин-3-он-1-сульфинильная группа для 5′-гидроксильной защиты дезоксирибонуклеозидных фосфорамидитов в твердофазном препарате ДНК-олигонуклеотидов.

Марчан В., Чешлак Дж., Ливенгуд В., Босаж С.Л. Марчан В. и др. J Am Chem Soc. 2004 г., 11 августа; 126 (31): 9601-10. дои: 10.1021/ja048377i. J Am Chem Soc. 2004. PMID: 15291564
-
Твердофазный синтез олигонуклеотидов миРНК.
Босаж SL. Босаж СЛ. Curr Opin Drug Discov Devel. 2008 март; 11 (2): 203-16. Curr Opin Drug Discov Devel. 2008. PMID: 18283608 Обзор.
Посмотреть все похожие статьи
Цитируется
-
Зависимость от последовательности красителей Cy3 и Cy5 в одноцепочечной ДНК с 3′-концевой меткой.
Кекич Т., Лиетард Дж. Кекич Т. и др. Научный представитель 2022 г., 31 августа; 12 (1): 14803. doi: 10.1038/s41598-022-19069-9.
 Научный представитель 2022.
PMID: 36045146
Бесплатная статья ЧВК.
Научный представитель 2022.
PMID: 36045146
Бесплатная статья ЧВК. -
Зависимое от последовательности тушение флуоресценции флуоресцеина на одноцепочечной и двухцепочечной ДНК.
Лиетард Дж., Амер Д., Сомоса М.М. Лиетард Дж. и соавт. RSC Adv. 2022 16 февраля; 12 (9): 5629-5637. doi: 10.1039/d2ra00534d. Электронная коллекция 2022 10 февраля. RSC Adv. 2022. PMID: 35425544 Бесплатная статья ЧВК.
-
Частота химических и фотохимических ошибок при светонаправленном синтезе сложных библиотек ДНК.
Лиетард Дж., Леже А., Эрлих Ю., Садовски Н., Тимп В., Сомоса М.М. Лиетард Дж. и соавт. Нуклеиновые Кислоты Res. 2021 9 июля; 49 (12): 6687-6701. doi: 10.1093/nar/gkab505. Нуклеиновые Кислоты Res. 2021. PMID: 34157124 Бесплатная статья ЧВК.
-
Предпочтение последовательности и неразборчивость инициатора для синтеза ДНК De Novo с помощью терминальной дезоксинуклеотидилтрансферазы.
Шауди Э., Лиетард Дж., Сомоса М.М. Шауди Э. и др. ACS Synth Biol. 2021 16 июля; 10 (7): 1750-1760. doi: 10.1021/acssynbio.1c00142. Epub 2021 22 июня. ACS Synth Biol. 2021. PMID: 34156829Бесплатная статья ЧВК.
-
Недорогое хранилище данных ДНК с использованием фотолитографического синтеза и расширенной реконструкции информации и исправления ошибок.
Antkowiak PL, Lietard J, Darestani MZ, Somoza MM, Stark WJ, Heckel R, Grass RN. Антковяк П.Л. и др. Нац коммун. 2020 22 октября; 11 (1): 5345. doi: 10.1038/s41467-020-19148-3. Нац коммун. 2020. PMID: 33093494 Бесплатная статья ЧВК.

Просмотреть все статьи «Цитируется по»
использованная литература
-
- Бумгарнер Р. ДНК-микрочипы: типы, приложения и их будущее. Curr Protoc Mol Biol. 2013;101(2):1.1–22.21.11.
-
- Герхольд Д., Рашмор Т., Каски КТ. ДНК-чипы: многообещающие игрушки стали мощными инструментами. Тенденции биохимических наук. 1999;24:168–173. doi: 10.1016/S0968-0004(99)01382-1. — DOI — пабмед
-
-
Ståhl PL, et al.
 Визуализация и анализ экспрессии генов в срезах тканей методом пространственной транскриптомики. Наука. 2016; 353:78–82. doi: 10.1126/science.aaf2403.
—
DOI
—
пабмед
Визуализация и анализ экспрессии генов в срезах тканей методом пространственной транскриптомики. Наука. 2016; 353:78–82. doi: 10.1126/science.aaf2403.
—
DOI
—
пабмед
-
Ståhl PL, et al.
-
- Нувайсир Э.Ф. и соавт. Анализ экспрессии генов с использованием массивов олигонуклеотидов, полученных безмасочной фотолитографией. Геном Res. 2002; 12:1749–1755. doi: 10.1101/gr.362402. — DOI — ЧВК — пабмед
-
-
Чоу С-С, Чен С-Х, Ли Т-Т, Пек К.
-
Чоу С-С, Чен С-Х, Ли Т-Т, Пек К.

 комсостава
комсостава