Какие библиотеки можно подключить к КОМПАС-3D. Как установить и использовать приложения и библиотеки в КОМПАС-3D. Какие возможности дают библиотеки для проектирования в КОМПАС-3D. Как создать собственную библиотеку фрагментов в КОМПАС-3D.
Что такое библиотеки и приложения в КОМПАС-3D
Библиотеки и приложения в КОМПАС-3D — это дополнительные программные модули, расширяющие базовые возможности системы. Они позволяют автоматизировать типовые операции проектирования и черчения, ускорить работу конструктора.
Основные виды библиотек в КОМПАС-3D:
- Прикладные библиотеки — содержат функции для автоматизации конкретных задач проектирования
- Библиотеки фрагментов — наборы готовых 2D элементов чертежей
- Библиотеки 3D-моделей — наборы трехмерных моделей стандартных и типовых деталей
Приложения представляют собой отдельные программы, интегрируемые в интерфейс КОМПАС-3D и расширяющие его функциональность. Они могут содержать как библиотеки элементов, так и инструменты для специализированных расчетов.
Как подключить библиотеку в КОМПАС-3D
Для подключения библиотеки в КОМПАС-3D выполните следующие действия:
- Откройте Менеджер библиотек через меню Сервис — Менеджер библиотек
- В появившемся окне выберите нужную библиотеку из списка
- Нажмите кнопку «Подключить» или дважды щелкните по названию библиотеки
- Библиотека появится в меню «Библиотеки» главного окна КОМПАС-3D
Подключенные библиотеки можно использовать при работе с документами КОМПАС-3D. Для отключения библиотеки используйте кнопку «Отключить» в Менеджере библиотек.
Основные библиотеки КОМПАС-3D
КОМПАС-3D содержит ряд встроенных библиотек для решения типовых задач машиностроительного проектирования:
Машиностроительная библиотека
Содержит функции для проектирования типовых деталей и узлов: валы, зубчатые колеса, пружины, подшипники и др. Позволяет выполнять прочностные расчеты.
Библиотека Стандартные изделия
Включает 3D-модели и параметрические чертежи стандартных крепежных элементов, подшипников, уплотнений и других типовых деталей по ГОСТ и ISO.
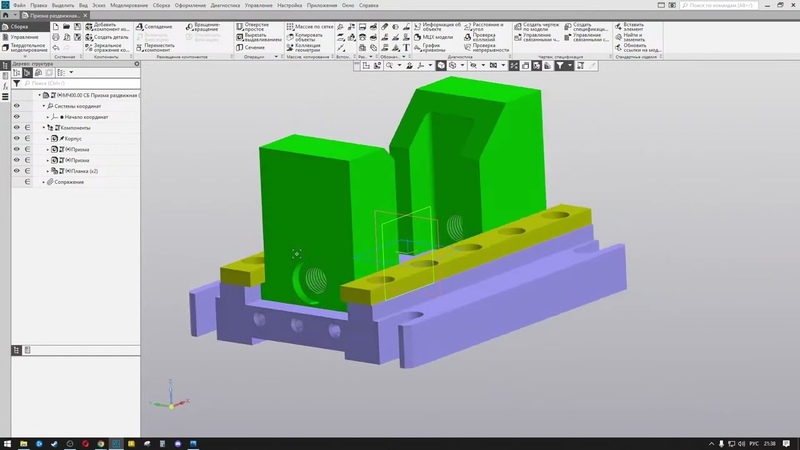
Библиотека электродвигателей
Позволяет подбирать и вставлять в документы 3D-модели электродвигателей различных серий. Содержит информацию о габаритах, массе и других параметрах двигателей.
Создание пользовательских библиотек фрагментов
В КОМПАС-3D можно создавать собственные библиотеки часто используемых фрагментов и 3D-моделей. Для этого:
- Создайте новую библиотеку через Менеджер библиотек
- Добавьте в нее нужные фрагменты или 3D-модели
- Задайте параметры и атрибуты элементов библиотеки
- Сохраните библиотеку в файл .lfr (для 2D) или .l3d (для 3D)
Пользовательские библиотеки позволяют систематизировать наработки и ускорить создание похожих проектов в будущем.
Приложения для расширения возможностей КОМПАС-3D
Дополнительные приложения значительно расширяют базовые возможности КОМПАС-3D. Некоторые популярные приложения:
КОМПАС-Shaft 3D
Автоматизирует проектирование деталей типа тел вращения — валов, осей, втулок. Позволяет рассчитывать геометрические и прочностные характеристики.
КОМПАС-Spring
Инструмент для расчета и проектирования пружин различных типов. Создает 3D-модели и чертежи пружин по результатам расчета.
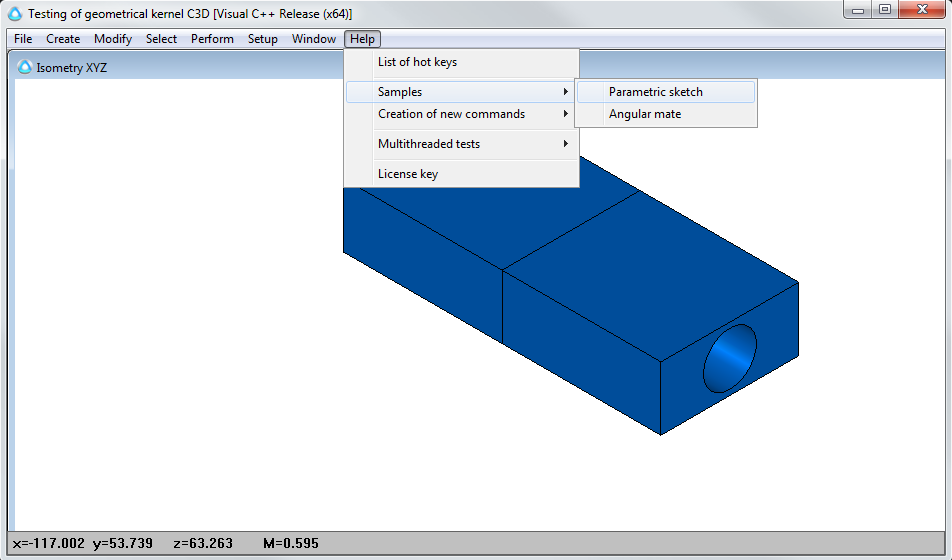
Оборудование: Металлоконструкции
Приложение для проектирования металлических строительных конструкций. Включает библиотеку типовых профилей и узлов.
Преимущества использования библиотек и приложений
Применение дополнительных библиотек и приложений в КОМПАС-3D дает ряд преимуществ:
- Ускорение типовых операций проектирования
- Автоматизация рутинных расчетов
- Использование готовых параметрических моделей
- Соблюдение отраслевых стандартов
- Повышение качества проектной документации
- Сокращение сроков разработки изделий
Грамотное применение библиотек позволяет в разы повысить производительность работы конструктора в КОМПАС-3D.
Как выбрать нужные библиотеки
При выборе библиотек и приложений для КОМПАС-3D следует учитывать:
- Специфику решаемых проектных задач
- Отрасль применения (машиностроение, строительство и т.д.)
- Необходимость специальных расчетов
- Требования по автоматизации типовых операций
- Совместимость с используемой версией КОМПАС-3D
Рекомендуется начать с базовых библиотек, входящих в комплект поставки, а затем при необходимости добавлять специализированные приложения.

Заключение
Библиотеки и приложения существенно расширяют возможности КОМПАС-3D, помогая решать сложные инженерные задачи. Их грамотное использование позволяет в разы повысить эффективность работы конструктора и качество проектирования. При этом важно подбирать библиотеки под конкретные задачи и изучать их функционал для максимально эффективного применения.
АСКОН КОМПАС-3D V20, Библиотеки (обновление лицензий), Библиотека фотореалистики Artisan Rendering
КОМПАС-3D v20 – российская система проектирования, построенная на собственном геометрическом ядре C3D. Новая версия умеет напрямую читать форматы практически всех популярных CAD-систем без необходимости их предварительной конвертации, а также появились инструменты прямого редактирования геометрии, было доработано поверхностное и листовое моделирование, расширены базовые возможности 3D- и 2D-проектирования, проделана большая работа над скоростью и производительностью системы.
Прямое чтение форматов других CAD-систем
КОМПАС-3D научился напрямую открывать модели практически всех популярных CAD-систем без использования дополнительного конвертера. Поддерживаются форматы систем: UGS/NX, CATIA, ProE/Creo, SolidWorks, SolidEdge и Inventor. Новинка доступна в базовой функциональности КОМПАС-3D v20.
Управление наборами инструментальных панелей и другие изменения в интерфейсе
Появилась возможность управлять наборами инструментальных панелей: создавать свой набор, наполнять его необходимыми командами, перемещать, скрывать и удалять. Контекстные панели тоже можно настроить под себя. Их состав зависит от документа, с которым работает пользователь, а также от выбранного объекта: грани, ребра или отрезка на чертеже.
Новинки поверхностного моделирования
Функциональность поверхностного моделирования КОМПАС-3D пополнилась абсолютно новым типом поверхностей – «Поверхностью конического сечения», которая образуется путем перемещения кривой конического сечения по двум направляющим с возможностью изменения параметров этого сечения. В итоге формируется очень гладкая поверхность на всем своем протяжении.
Переработана поверхность по сети кривых. Теперь в качестве границ поверхности можно использовать многосегментные кривые, явно задавать цепочки соединения характерных точек, контролировать направление сопряжения поверхностей, оптимизировать форму поверхности для получения более предсказуемого результата на нечасто заданной, но достаточно искривленной сетке кривых.
Для диагностики гладкости поверхностей создана новая команда «Сетка графиков кривизны». Результат работы команды – графики кривизны для линий пересечения поверхности с плоскостями, расположенными либо параллельно базовой плоскости, либо радиально вокруг указанной точки.
Новинки листового моделирования
Твердотельную или поверхностную модель, в т.ч. модель без истории построения, теперь можно превратить в листовую деталь, а затем получить развертку. При этом задаются различные параметры самого листового тела, углов и сгибов. Доступен автоматический поиск скруглений, определяющих положение сгибов в листовом теле, а полученное листовое тело сохраняет ассоциативную связь с исходной моделью. Новая команда «Отбортовка» строит сгиб в листовой детали вдоль плоского ребра произвольной формы. «Штамповка телом» – еще одна новая команда, создает в листовом теле штамповку по форме другого, заранее созданного в модели тела.
Новая панель управления свойствами изделия и его составных частей
Появилась новая панель управления «Состав изделия», предназначенная для работы со свойствами изделия и его составных частей. «Состав изделия» поможет просматривать и изменять свойства составных частей, управлять их вхождением в спецификацию текущего стиля, добавлять и удалять их.
Новое приложение «Оборудование: Кабельные каналы»
Приложение позволит быстро построить кабельные каналы без предварительно созданной траектории. Настроить стили с указанием профиля канала, поворотов и ветвлений. Автоматически подсчитать крепежные элементы и добавить их в спецификацию. Пользователь сможет добавить свои элементы в состав кабельного канала и задать профиль канала с помощью библиотеки фрагментов.
«Изоляция» металлоконструкций и импорт из IFC
В приложении «Оборудование: Металлоконструкции» появилась группа команд для изолирования каркасных конструкций. Можно изолировать профиль, тело или грань целиком. Новые команды пригодятся при проектировании набора судна.
Вторая крупная новинка приложения – импорт из IFC (Industry Foundation Classes). Новая команда открывает файл формата IFC, содержащий металлоконструкции, для последующего редактирования.
Воспользоваться правом на обновление до версии V20 можно на момент выхода версии V20.
✅ Купите АСКОН КОМПАС-3D V20, Библиотеки (обновление лицензий), Библиотека фотореалистики Artisan Rendering на официальном сайте
✅ Лицензия АСКОН КОМПАС-3D V20, Библиотеки (обновление лицензий), Библиотека фотореалистики Artisan Rendering по выгодной цене
✅ АСКОН КОМПАС-3D V20, Библиотеки (обновление лицензий), Библиотека фотореалистики Artisan Rendering, лицензионное программное обеспечение купите в Москве и других городах России
Предлагаем также:cccp3d.ru | Кодинг библиотек для компаса — Page 3
1 час назад, IgorT сказал:
Чо правильно? Что в сборке получаем разные размеры деталей, а в СП уходит детали одинаковые? Это правильно?
Хорошо, формулирую по-другому. После того, как стандартное изделие добавлено в сборку — его размеры «вручную» меняться не должны. Вот это правильно.
Пример. Конструктор добавил из библиотеки заклепку 3 Х 30.00 ГОСТ 10299-80. Подумал — не, надо диаметр поменьше. Изменил вручную на 2.5. И происходит ОЙ — выясняется, что по ГОСТ-у для диаметра 2.5 максимальная длина стержня заклепки — 20 мм. В лучшем случае КД развернёт нормоконтроль, в худшем снабжение скажет:»Фи на Ваши головы, судари. Сего изделия не существует в природе. Извольте откорректировать свои труды.»
Именно так и должны по-хорошему работать любые библиотеки — хранить точные типоразмеры изделий с их наименованиями. А в СП детали должны меняться только в том случае, если стандартное изделие заменяется полностью, а не его какой-то один размер.
2 часа назад, IgorT сказал:
Вы с компасом работаете?
Вообще-то функционал внешних переменных очень полезный.
Мне с какого-то этапа моей жизни до лампочки, в чём работать — существуют принципы работы, которые не зависят от запускаемого ярлыка на рабочем столе. Насколько система позволяет/непозволяет эти принципы реализовывать — вопрос изучения документации и общения с разработчиками.
6 минут назад, BSV1 сказал:
А связать эти данные для СП с соответствующими переменными модели, чтобы изменения информации для СП происходили автоматом можно?
Опасно. Если значения переменных могут быть произвольными — вполне допустима ситуация, про которую я писал выше.
Как установить библиотеку в компас — MOREREMONTA
При добавлении библиотеки в Менеджернеобходимо щелкнуть левой кнопкой мыши по пункту Библиотеки КОМПАС→Добавить описание→ Библиотеки документов→появится окно Добавить библиотеку(в котором
Для подключения библиотеки к КОМПАС-3D выполните следующие действия.
1. Вызовите команду Сервис — Менеджер библиотек.
На экране появится окно Менеджера библиотек.
2. В списке библиотек (он находится в правой части первой вкладки) выделите имя нужной библиотеки и вызовите команду Подключитьиз контекстного меню.
Для быстрого подключения выбранной библиотеки можно щелкнуть мышью в поле рядом с ее названием.
Выбранная библиотека подключается в установленном для нее режиме: меню, окно, диалог или панель. В поле рядом с названием библиотеки появляется красная «галочка» — признак того, что библиотека подключена.
Названия всех подключенных к системе прикладных библиотек отображаются как команды в меню Библиотека.
С помощью Менеджера(см. рис.5.6) (панель инструментов Стандартная или пункт главного меню Сервис)Вы можете подключать, отключать и запускать библиотеки, выбирать режим их работы (меню, окно, диалог или панель), а также создавать библиотеки фрагментов и библиотеки моделей.
В системе КОМПАС возможна работа с библиотеками трех типов:
1. библиотеки фрагментов *.lfr,
2. библиотеки моделей *.l3d,
3. прикладные библиотеки *.dll или *.rtw.
Можно ли из системы компас импортировать твердотельную модель в препроцессоры других систем ?
Для передачи созданной в КОМПАС-3D модели в другие пакеты с целью дальнейшей ее обработки (для включения в сборку, выполнения прочностных и иных расчетов, формирования управляющих программ для технологического оборудования и т.д.) служат команды экспорта. Трехмерные модели КОМПАС-3D можно сохранить и передать в форматах IGES, SAT и STL. Кроме того, трехмерные модели КОМПАС-3D могут быть напрямую, без использования внешних модулей конвертации, прочитаны пакетом SolidWorks. Это достигается путем использования специального модуля сопряжения с SolidWorks, разработанного специалистами АСКОН.
В качестве примеров использования экспортированных моделей КОМПАС-3D можно привести формирование управляющих программ для станков с ЧПУ на основе файлов формата IGES (система Гемма3D), формирование управляющих программ для стереолитографических машин на основе файлов формата STL, создание сборок на основе файлов формата SAT (системы SolidWorks и SolidEdge).
Наряду с экспортом моделей в КОМПАС-3D существует возможность импорта файлов формата SAT.
Не нашли то, что искали? Воспользуйтесь поиском:
Как добавлять библиотеки элементов (Дополнительно чертежи муфт , гостированных двигателей и тд. ) . И возможна ли установка библиотек формата rtf. на данную версию Компаса?
Дубликаты не найдены
Теперь они наз. «приложения». Отрыть меню «Приложения», далее — конфигуратор, а там уже всё понятно.
Бля, и из Компаса уже какой-то медиаплеер сделали.
Круче намного стал.
Что дружок, сессия пришла? А нечего игры было искать)
Комментарий дня
Мужик по радио слышит что за полярным кругом минус 62, он вспоминает что там работает его знакомый, звонит ему по телефону:
-Привет! Какая у вас температура воздуха?
— ясно, но по радио передовали что минус 62!
Библиотека представляет собой программный модуль, тот, что сделан для того, дабы расширить типовые вероятности программы КОМПАС-3D. Вся библиотека ориентируется на выполнение определенной задачи автоматизированного проектирования, которая формирует конструкторскую документацию.
Вам понадобится
- – компьютер;
- – установленная программа Компас.
Инструкция
1. Подключите библиотеку в Компас двумя методами. 1-й случай применяется, когда на экран не вызвана система управления библиотеками. Запустите программу Компас, перейдите в основное меню, выберите пункт «Сервис», в меню выберите пункт «Администратор библиотек».
2. В левой части окна щелкните в пункте, соответствующей той библиотеке, которую нужно подключить. В правой части окна, дабы подключить библиотеку в «Компас», вызовите контекстное меню на ней, выберите команду «Многофункциональный механизм», дальше «Подключить». Дождитесь происхождения красного флажка, это значит подключение библиотеки произведено удачно.
3. Используйте 2-й метод присоединения библиотеки к программе «Компас». Для этого в основном меню программы выберите пункт «Сервис», дальше «Администратор библиотек». Перейдите в левую часть окна систему управления, щелкните пункт подключаемой библиотеки , скажем «Машиностроение».
4. В правой части окна щелкните двукратно по библиотеке, дождитесь ее подключения, должно открыться ее содержимое. Если все открылось, и на экране отображается состав данной библиотеки , значит подключение закончено.
5. Подключите библиотеку «Фотореалистика» в «Компас». Данная библиотека комфортна для применения в рекламной деятельности, при визуализации выпускаемой продукции. Она содержит существенный выбор реалистичных материалов и текстур, также в нее дозволено добавить пользовательские элементы тени, света, фона, и сцен окружающей атмосферы. Для ее установки запустите архив photoreal.msi, дальше следуйте указаниям мастера установки.
6. Позже этого подключите библиотеку с подмогой администратора в программе «Компас». Вначале добавьте изложение данной библиотеки , потом перейдите в окно выбора вида и выберите файл photoreal.rtw. Путь для подключения библиотек в программу – C:/Program Files/, дальше папка с программой, по умолчанию это папка ASCON, потом KOMPAS-3D V10, а в ней находится папка Libs.
Библиотека – это программный модуль, тот, что сделан для растяжения стандартных вероятностей программы. Вся определенная библиотека надобна для выполнения сурово обозначенных задач механического проектирования либо создания определенной документации. Разглядим методы подключения библиотек на примере программы “Компас 3-D”
Инструкция
1. Используйте один из следующих методов для того, дабы подключить библиотеку к программе “Компас 3-D”. Запустите приложение, зайдите в основное меню и выберите пункт «Сервис». После этого обнаружьте подпункт «Администратор библиотек». В левой части появившегося окна выберите тот пункт, соответствующий наименованию библиотеки , которую вы теперь хоте подключить.
2. В правой части этого же окна вызовите контекстное меню и выберите команду «Многофункциональный механизм». Позже этого нажмите на кнопку «Подключить». Подождите, должно пройти некоторое время. Позже того как наоборот библиотеки появится алый флажок, можете закрывать окно, библиотека подключена. Данный метод подходит, если не вызвана система механического управления библиотеками.
3. Используйте 2-й метод, дабы присоединить библиотеку. Запустите программу. В основном меню выберите пункт «Сервис», после этого «Администратор библиотек». Появится окно. В левой его части выберите волнующую вас библиотеку. В правой части окна двукратно кликните по этой же библиотеке. Должно пройти некоторое время. Позже этого отобразится все содержимое выбранной библиотеки . Если все содержимое открыто и отображается без ошибок, значит, выбранная библиотека подключена удачно.
4. Сделайте следующее, дабы подключить библиотеку «Фотореалистика». Она гораздо расширит базовые вероятности программы, и дозволит применять ее не только как многофункциональный инструмент проектирования, но и как средство создания текстур и материалов рекламного нрава.
Компьютерная графика | Уроки по КОМПАС-3D | Создание пользовательской библиотеки фрагментов с изменяемыми параметрами
По вопросам репетиторства по компьютерной графике (Autocad, Solidworks, Inventor, Компас), вы можете связаться любым удобным для вас способом в разделе Контакты. Подробное описание программ обучения и стоимость, вы можете посмотреть выбрав соответствующий курс. Обучение возможно очно и дистанционно.8.1 Цель
- научиться использовать выражения для задания параметров при создании эскиза модели;
- получить навыки создания пользовательской библиотеки фрагментов с возможностью изменять параметры.
8.2 Содержание
- создать пользовательскую библиотеку фрагмента на примере профиля отверстия;
- создать параметрическую модель детали корпуса с отверстием, вставленным из своей библиотеки фрагментов по варианту, предложенному преподавателем.
8.3 Последовательность и пример выполнения
8.3.1 Создание параметрического фрагмента
Рис. 1.1. Чертеж отверстия
- Создайте эскиз профиля будущего отверстия. Не забудьте проверить включен ли на панели Текущее состояние⇒Параметрический режим .
Рис. 1.2. Эскиз отверстия
- Проставьте размеры. Вызовите панель Настройка⇒Панели⇒Переменные . Панель появится как вкладка дерева построения. Всем размерам программа назначает имена переменных по шаблону V1… Создайте в главном разделе (под строкой имени файла), например, 10 параметров, задайте им имена и значения. Примените к ним статус Внешняя, для чего, выделите имена новых параметров, вызовите контекстное меню по ПКМ и выберите Внешняя. В разделе Переменные размеров (ниже главного), назначьте некоторым переменным размеров значения новых параметров, например, на рис. 1.3 — V2=d
Рис. 1.3. Создание новых параметров
- Сохраните файл фрагмента (*.frw).
- Запустите Редактор библиотек, используя команду главного меню Приложения⇒Утилиты⇒Редактор библиотек КОМПАС-3D. Появится диалоговое окно редактора библиотек.
Рис. 1.4. Редактор библиотек
- Переименуйте библиотеку, например, Библиотека отверстий Cavity. Создайте папку Отверстия 1, нажав на кнопку . Нажмите кнопку Добавить элемент . Выберите файл сохраненного фрагмента. Сохраните библиотеку. Закройте окно редактора.
Рис. 1.5. Создание библиотеки элементов
- Созданную новую библиотеку необходимо добавить в конфигурацию. Вызовите команду Настройка⇒Конфигуратор. На экране появляется диалог Конфигуратор.
Рис. 1.6. Окно Конфигуратора
- В Конфигураторе вызовите команду Состав⇒Добавить библиотеки элементов и в появившемся диалоге укажите созданную библиотеку. Закройте диалог Конфигуратор.
Рис. 1.7. Окно Конфигуратора с подключенной новой библиотекой
- Работа с библиотеками ведется на Панели библиотек. Для ее включения выберите команду Настройка⇒Панели⇒Библиотеки. Из списка выберите созданную библиотеку.
Рис. 1.8. Окно новой библиотеки
- Для вставки библиотечного фрагмента в эскиз, дважды щелкните на имени фрагмента (или перетащите его из окна библиотеки в окно эскиза), на панели свойств можно настроить и задать значения изменяемых параметров.
Рис. 1.9. Вставка библиотечного фрагмента в эскиз
- Результат выреза вращением.
Рис. 1.10. Вырез вращением
8.3.2. Создание таблицы переменных
- Повторите пункты 4-7, задав другое имя библиотеке.
- В окне Переменные вызовите команду Таблица переменных, нажав на кнопку . В окне Таблица переменных нажмите кнопку Читать внешние переменные . Появится строка со значениями внешних переменных, которые мы создавали в п. 2. Вставьте, используя команду Добавить строку ниже еще одну строку. В столбце Комментарии задайте название исполнений, в остальных столбцах измените значения переменных.
Рис. 1.11. Создание таблицы переменных
- Сохраните в файл (*.xls), нажав на кнопку Сохранить в файл .
- Для просмотра созданных исполнений в окне Таблица переменных выделите строку с нужным исполнением и нажмите кнопку Присвоить значения переменным. Вы увидите, как изображение перестраивается согласно новым значениям.
- Создайте файл модели, войдите в режим создания эскиза, вызовите вставку фрагмента, на Панели свойств нажмите кнопку Таблица переменных и выберите исполнение, при необходимости, измените значения переменных в списке.
НОУ ИНТУИТ | Лекция | Использование прикладной библиотеки КОМПАС 3D
Аннотация: Цель лекции: Изучить основные возможности прикладной библиотеки КОМПАС 3D, а также программу расчета пружин.
14.1 Работа с прикладной библиотекой КОМПАС 3D
Изучив способы построения моделей и специальные возможности программы, Мы не рассмотрели еще несколько базовых возможностей программы, которые значительно помогут сэкономить время.
Библиотека КОМПАС 3D содержит трехмерные модели передач, трубопроводов, втулок, осей и множество других элементов.
Чтобы воспользоваться библиотекой создайте документ «Деталь» и перейдите в «Менеджер библиотек» выберите одну из папок («Примеры библиотек», «Расчет и построение», «Оснастка и инструмент», «Металлоконструкции»).
Например перед Вами стоит задача построить 3D модель цилиндрического колеса. Можно это сделать и при помощи стандартных построений, более быстрый способ воспользоваться «Менеджером библиотек».
Рис. 14.1. Переход к прикладной библиотеке
Подтвердив переход выберите из списка «Цилиндрическая шестерня с внешними зубьями».
Рис. 14.2. Работа с библиотекой механических передач
В строке состояния Вы можете выбрать «позиционирование» — т.е. как будет отображаться Ваша модель и рассчитать параметры модели.
Можно провести геометрический расчет модели, выберите в строке состояния «Расчет в модуле КОМПАС – GEARS».
Рис. 14.3. Задание параметров модели
Теперь перед Вами раскроется окно привычной программы КОМПАС – GEARS. Можно приступить к геометрическому расчету.
Заполните поля программы как показано на рис. 14.4.
Рис. 14.4. Задание параметров геометрического расчета
Перейдите на страницу 2 проведите расчет, а затем выберите «закончить расчет».
Рис. 14.5. Завершение геометрического расчета
Остальные расчеты не нужно проводить.
Обучение в компас-3d для начинающих
Создание пользовательских библиотек с помощью КОМПАС-Макро
КОМПАС-Макро это интегрированная в систему КОМПАС-3D среда разработки конструкторских приложений на основе языка программирования Python. Почему за основу выбран именно Python? Во-первых, Python распространяется бесплатно и, как следствие, не налагает никаких ограничений на использование и распространение написанных на нем программ. Во-вторых, сегодня Python один из самых простых и понятных языков программирования, однако при всей своей простоте он мало в чем уступает таким «китам» объектно-ориентированного программирования, как C++ и Object Pascal (Delphi).
По своей сути КОМПАС-Макро является обычной библиотекой, подключаемой к КОМПАС, только с большими возможностями. При создании приложений в КОМПАС-Макро можно пользоваться как функциями КОМПАС-Мастер (о них мы еще расскажем), так и специальными функциями макросреды, облегчающими разработку прикладных библиотек. Среди специальных функций КОМПАС-Макро следует отметить функции простановки угловых, линейных и радиальных размеров, функцию вставки в документ фрагмента, рисования линии-выноски и пр. Синтаксис перечисленных методов значительно проще их аналогов, реализованных в КОМПАС-Мастер (к примеру, вместо вызова одной-единственной функции создания линейного размера в КОМПАС-Макро при работе с API-функциями среды КОМПАС-Мастер приходится объявлять и инициализировать целых три интерфейса).
Если же вы не понаслышке знакомы с основами объектно-ориентированного программирования и у вас есть желание разрабатывать самые мощные библиотеки на базе КОМПАС-3D, то использовать вы можете КОМПАС-Мастер.
Среда разработки прикладных библиотек к КОМПАС-3D
Создание библиотек фрагментов и моделей
Для создания библиотек этого типа вам не потребуется никаких специальных навыков, кроме умения работать в КОМПАС-График или в КОМПАС-3D. С помощью таких библиотек каждый проектировщик может систематизировать свой набор наиболее часто используемых элементов, чтобы облегчить доступ к ним при разработке новых чертежей или моделей.
Создать свою библиотеку фрагментов совсем несложно. Для этого в окне Менеджера библиотек нужно воспользоваться командой контекстного меню Добавить описание > Библиотеки документов. В появившемся диалоговом окне открытия библиотеки следует выбрать тип файла: КОМПАС-Библиотеки фрагментов (*.lfr), если вы создаете хранилище для чертежей или эскизов, или КОМПАС-Библиотеки моделей (*.l3d) для наполнения будущей библиотеки 3D-моделями. В итоге в окне Менеджера библиотек должна появиться ваша библиотека, пока еще пустая. После запуска к ней можно добавлять фрагменты и модели с помощью команд контекстного меню.
Главное преимущество библиотек фрагментов простота их создания и применения. Большим плюсом таких приложений является также то, что при появлении новых версий КОМПАС не нужно подгонять или изменять их структуру под только что выпущенный релиз. Достаточно загрузить старый файл библиотеки в Менеджер библиотек, и можете не сомневаться всё будет работать.
Недостатком подобных библиотек является ограниченность их функциональных возможностей. Автоматизация таких библиотек достигается только за счет параметризации объектов, которыми вы наполняете приложение, а библиотека лишь ускоряет процесс поиска и вставки нужного графического элемента в документ и обеспечивает лучшие условия для их хранения (не в отдельных файлах, раскиданных по жесткому диску, а упорядоченно, в едином файле-библиотеке).
Более широкими возможностями, по сравнению с библиотеками фрагментов, обладают библиотеки шаблонов КОМПАС-3D.
Создание библиотеки моделей
Пример пользовательской библиотеки, содержащей модели шпонок, и ее применение
Пример пользовательской библиотеки шаблонов для создания трехмерной модели гайки
Как изучить маршрут по карте и компасу?
- Возьмите карту местности, куда собираетесь отправиться, расстелите ее на полу или на столе. Карандашом обозначьте все точки, через которые нужно будет пройти: начальный пункт, конечный, привалы для перекусов или даже ночевки, если поход ожидается длинным.
- На карте разместите компас и вращайте ее до тех пор, пока показатели севера не совпадут.
- При помощи линейки нужно обозначить свой маршрут. Его нужно прокладывать так, чтобы точка начала маршрута совпала со средней точкой на циферблате. Градус, который получается в этом случае, нужно вычислить. Это значение записывается в блокноте. Сразу стоит записать и другое значение. Это обратный азимут.
- Весь отрезок пути должен быть зафиксирован на бумаге. Так вы точно будете знать, как двигаться от точки к точке, и ваша прогулка будет продуктивной.
Во время движения нужно ориентироваться по стрелке, назад вы уже будете идти по расчету азимута. Предварительная подготовка к походу обезопасит вас и вашу группу от неожиданных мест. Заблудиться будет невозможно, если двигаться строго по компасу.
Обучение 3D моделированию в Компас-3D
Откроем Компас-3D и сделаем первые шаги к проектированию в твердотельном конструировании. Нажимаем создать Деталь.
Нажимаем правой клавишей мыши на одну из плоскостей (в данном примере плоскость ZX) и выбираем Создать эскиз.
Итак, мы перешли в режим создания Эскиза.
Начнем чертить эскиз. Переходим во вкладку геометрия, зажимаем левой клавишей мыши на Прямоугольник и выбираем Прямоугольник по центру и вершине, для того чтобы было удобно начинать строить фигуру с центра координат.
Строим прямоугольник, начиная с центра и доводя до вершины (размеры произвольные).
Во вкладке Размеры выберем инструмент Линейный размер.
Задавая начальную и конечную точку линии которая будет размерной, вводим значение ширины и высоты прямоугольника (30х50 мм).
Аналогичным образом начертим окружность (вкладка Геометрия) из центра прямоугольника с диаметром 16 мм.
Далее, выберем еще раз Прямоугольник по центру и вершине, но изменим стиль линии на Осевая.
Чертим прямоугольник в центре основного прямоугольника и сразу же образмерим его (40х20). Данный прямоугольник будет служить для удобства построения отверстий расположенных в углах будущей детали.
Теперь, привязываясь к точкам вершин внутреннего прямоугольника, строим 4 окружности.
С помощью инструмента Диаметральный размер во вкладке Размеры, задаем диаметр для одной из окружностей.
Зажимаем клавишу Ctrl, выделяем все 4 окружности и во вкладке Ограничения нажимаем Равенство. Это сделает все размеры отверстий равными, отклоняясь от заданного размера на одной из окружностей.
Выходим из эскиза с помощью кнопки справа в верхнем углу экрана.
Сохраняя эскиз выделенным, нажимаем Элемент выдавливания во вкладке Элементы тела и задаем расстояние 5 мм. Нажимаем ОК.
В конечном итоге получаем твердотельную деталь с толщиной 5 мм.
Для того чтобы сохранить деталь, нажимаем Файл > Сохранить как… Выбираем нужную папку для сохранения и нажимаем Сохранить.
Уроки Компас-3D для начинающих: бесплатные видео для домашнего обучения
Компас-3D — универсальная система трёхмерного проектирования, которая обладает большим набором инструментов для моделирования изделий от разработки идеи в 3Д формате до подготовки полного комплекта документации. В ней можно создать модель изделия, здания, сооружения, и при этом получить развернутые чертежи деталей, техническую документацию соответствующую принятым стандартам. Софт поддерживает импорт-экспорт файлов различных форматов.
ВСЕ КУРСЫ ОНЛАЙН подобрали лучшие бесплатные видео уроки Компас 3D для самостоятельного обучения на дому, которые познакомят с основами работы в программе.
С продуктом вместе работают
Архитектура: АС/АР,
Металлоконструкции: КМ,
Технология: ТХ,
Жизнеобеспечение: ОВ,
Жизнеобеспечение: ВК,
Железобетонные конструкции: КЖ,
Электроснабжение: ЭС
Технология предлагает проектировщику начать работать в привычной среде чертежа (2D, вид в плане). Процесс проектирования протекает в плоскости чертежа с возможностью автоматического получения спецификаций и ведомостей элементов в любой момент времени. В то же время это начало формирования модели. Само название MinD (Model in Drawing, или «модель в чертеже») говорит о том, что виртуальная модель здания уже заложена в чертеж. При работе со строительными элементами, взятыми из приложений, остается один шаг до автоматической генерации трехмерной модели. Полученная объемная модель позволит визуализировать объект проектирования, выполнить необходимые сложные разрезы, вернув их на чертеж, а также представить модель объекта заказчику.
В технологии MinD заложена возможность коллективной работы над проектом всеми участниками, задействованными над процессом. Когда архитектор проработал поэтажные планы или технологи завершили компоновку оборудования, то смежные специалисты могут взять готовые планы для дальнейшей проработки конструктивной части или как подложку для проектирования инженерных систем. Основа коллективной работы — специальная команда, позволяющая использовать базовый чертеж на следующих этапах проекта и при его изменении все участники проекта получают уведомление о новых условиях.
Виды компасов
На сегодняшний день компасы можно классифицировать по нескольким критериям:
По типу устройства:
- механические: компасы с намагниченной металлической стрелкой, указывающей в направлении севера;
- гироскопические: компасы с гироскопом в основании. Это более точные приборы, поскольку их стрелка направляется не на магнитный полюс, а на настоящий, географический. Именно поэтому на воздушных и морских суднах чаще используются гироскопические компасы;
- электронные: оснащены процессором, дисплеем и другими электронными компонентами. В зависимости от модели, могут отображать не только направление, но и другую информацию. Среди электронных компасов также выделяют радио компасы,но с появлением системы навигации GPS их применяют все реже.
По назначению:
- туристические: как правило, это круглая коробка (чаще всего из пластмассы) с магнетизированной стрелкой, вращающейся в центре. Зачастую оснащены и другими дополнительными устройствами, как, например, термометр;
- военные: схожие с туристическими, но в обязательном порядке оснащены линейкой, визирным приспособлением, увеличительной линзой. Такие компасы изготавливаются из металла и обладают большей точностью, чем туристические;
- геологические: приборы оснащены также полулимбом и клинометром;
- астрономические: помогают находить стороны света при помощи звезд и светил. Прибор характеризуется высокой точностью, но едва ли может быть полезен в дневное время;
- компас буссоль: используется в геодезии, а также для наведения артиллерийского орудия при атаках.
1 — механический; 2 — гироскопический; 3 — электронный; 4 — военный; 5 — геологический; 6 — компас буссоль; 7 — астрономический; 8 — туристический.
Как пользоваться компасом
Современные модели компасов позволяют не только узнать направление на север и юг, но и измерять азимут на объект либо определять направление на местности по известному азимуту.
Для того, чтобы определить направления сторон света, нужно расположить компас горизонтально, привести стрелки в рабочее положение (если она была зафиксирована тормозом) и дождаться, когда колебания стрелки успокоятся. Северный конец стрелки укажет на север, южный — на юг. Зная эти стороны света, можно легко определить другие, о чем мы рассказывали в этой статье.
По сути, с точки зрения физики северный магнитный полюс Земли на самом деле является южным магнитным полюсом, ведь именно к нему тянется северная часть стрелки магнитного компаса (противоположные полюса магнитов притягиваются). Та же самая «беда» и с южным магнитным полюсом, который по сути является северным полюсом магнита. Такое «перекручивание» было сделано для удобства, поскольку в противном случае северный географический полюс соответствовал бы южному магнитному, а южный географический — северному магнитному, что не очень удобно с практической точки зрения.
Если с помощью компаса нужно измерить азимут на объект (ориентир), то тут алгоритм действий будет зависеть от того, какой моделью мы пользуемся. Рассмотрим два основных варианта и способы ориентирования с их помощью.
Вариант №1. Измерение азимута с помощью компаса с фиксированной шкалой и подвижной стрелкой:
- Компас располагается в горизонтальной плоскости.
- Целик и мушка визируются на нужный ориентир.
- При фиксированном положении компаса его шкала (лимб) вращается до тех пор, пока северная часть магнитной стрелки не укажет на значение 0°/360° на шкале. Теперь указатель компаса показывает значение на шкале, соответствующее магнитному азимуту на ориентир. О том, как переводить магнитный азимут в истинный, можно почитать в отдельной статье.
Вариант №2. Измерение азимута с помощью компаса со стрелкой, прикрепленной к шкале:
- Компас располагается горизонтально.
- Целик и мушка наводятся на объект, на который измеряется азимут.
- Выжидается время, пока шкала и стрелка повернутся и остановятся. Указатель покажет цифру на шкале, соответствующую измеряемому магнитному азимуту.
Теперь рассмотрим, как определить направление по известному азимуту. Рассматривать также будем для двух моделей.
Вариант №1. Определение направления с помощью компаса с фиксированной шкалой и подвижной стрелкой:
- Компас располагается горизонтально.
- Лимб поворачивают до тех пор, пока указатель не укажет на цифру на шкале, соответствующую заданному азимуту, по которому определяется направление.
- Компас поворачивается в горизонтальной плоскости, пока северная часть магнитной стрелки не укажет на значение 0°/360° на шкале.
- Компас удерживается в таком положении. Теперь мушка и целик укажут искомое направление.
Вариант №2. Определение направления с помощью компаса со стрелкой, прикрепленной к шкале:
- Компас удерживается в горизонтальной плоскости.
- Прибор вращается в горизонтальной плоскости до тех пор, пока указатель не укажет на шкале лимба цифру, соответствующую заданному азимуту.
- Компас неподвижно фиксируется, а через мушки и целик отслеживается искомое направление.
Мы рассмотрели, как работать с компасом на местности, а о том, как производить измерения с помощью компаса по карте и как использовать этот инструмент для хождения по азимутам, можно почитать в отдельной статье.
Кроме работы с компасом стоит также сказать об общих правилах эксплуатации его, которые помогут сохранить работоспособность прибора на более продолжительный срок.
Крепежные соединения
Практический урок демонстрирует создание болта и плиты с отверстием. Будут продемонстрированы два способа. 1. С использованием стандартной библиотеки изделий. 2. Ручная отрисовка болтов и отверстий. Для начала создается эскиз прямоугольника, который выдавливается в одном направлении. Далее заходят в библиотеку, где выбирают элемент отверстие (только если он стандартный), который размещают на плите, предварительно настроив его. Болт также можно найти в библиотеке, подстроив его под диаметр отверстия. Вручную такие элементы делаются с помощью геометрических фигур и базовых операций.
Создание библиотек шаблонов
Библиотека шаблонов это прикладная библиотека, состоящая из базового параметризованного чертежа или трехмерной модели, таблицы переменных, набранной в соответствии с некоторыми правилами в табличном редакторе MS Excel, и схемы документа КОМПАС-3D или рисунка, содержащего имена переменных. Библиотека представляет собой файл с расширением *.tlm, с помощью которого переменным параметризованного фрагмента или детали ставятся в соответствие значения, набранные в Excel-таблице. Для создания библиотек шаблонов предназначено специальное приложение под названием Менеджер шаблонов.
Разработку шаблона следует начинать с создания его прототипа (фрагмента или детали), пользуясь стандартными средствами КОМПАС-График или КОМПАС-3D. Затем необходимо параметризовать вычерченный фрагмент или эскизы модели и назначить внешними все переменные, которые вы планируете вводить (набирать) в таблице Excel. Следующим шагом является создание таблицы значений. Такая таблица формируется в редакторе Excel и включает названия внешних параметризованных переменных, флаги видимости колонок значений в Менеджере шаблонов, конкретные значения или их интервал для каждой переменной и др. Детально с правилами заполнения таблиц к шаблонам вы можете ознакомиться в файле-справке и примерах, поставляемых вместе с библиотекой шаблонов. Формирование еще одной составной части шаблона схемы параметров не вызовет особых затруднений. Схемой может быть любой графический файл системы КОМПАС-3D или файл-рисунок в формате *.bmp, *.gif или *.jpg.
Когда все три рассмотренных выше компонента подготовлены, их нужно собрать в единое приложение. Для этого, пользуясь командой Новая библиотека, следует указать название будущей библиотеки и папку, где она будет размещена. Далее необходимо оформить внутреннюю древовидную структуру библиотеки, то есть разделы и подразделы, в которых будут находиться подготовленные вами шаблоны.
Завершающий этап подготовки библиотеки это наполнение разделов соответствующими шаблонами, для чего следует воспользоваться командой Создать шаблон. После ее вызова появится небольшое окошко, в котором для каждого шаблона нужно ввести имя, указать файл с параметризованным фрагментом или моделью, файл таблицы параметров Excel и заставку (необязательно). По завершении всех этих действий библиотека шаблонов полностью готова к работе. Можно загружать определенный шаблон, вводить значения переменных и вставлять готовую деталь или фрагмент в документ.
Каковы же существенные отличия библиотек шаблонов от библиотек фрагментов? Прежде всего это возможность вставки в документ не всего фрагмента, а отдельных его слоев, а также наличие ряда дискретных значений для переменной, что исключает ввод или выбор пользователем ошибочных значений. Кроме того, переменные шаблонов могут быть различных типов, в том числе логических и строковых, а в размерных надписях фрагмента-заготовки несложно резервировать переменные для текстовых подстановок (они должны выделяться с обеих сторон знаком #). Главным же преимуществом библиотек шаблонов является то, что при использовании шаблона не приходится изменять вручную параметризованные переменные, как это делалось бы при вставке фрагмента или модели из библиотеки фрагментов. При вставке объекта в активный документ Менеджер шаблонов сам позаботится о том, чтобы подставить нужные значения из выбранного пользователем ряда.
Безусловно, на разработку шаблонов уходит больше времени и при этом одних только навыков работы с КОМПАС уже будет недостаточно придется изучить принципы работы Менеджера библиотек. Зато применение шаблонов дает возможность достаточно гибко автоматизировать создание типовых элементов и вместе с тем не запрещает динамично управлять процессом формирования библиотечного элемента.
Создание прикладных библиотек с помощью API
Муфты, сгенерированные с помощью приложения, разработанного
в среде КОМПАС-Мастер
Заключение
Мы закончили рассказ о наборе разнообразных приложений к системе КОМПАС-3D. Главная цель этого обзора показать значение прикладных библиотек для улучшения качества и ускорения проектирования в целом и с использованием КОМПАС-3D в частности. Учитывая, что стандартные библиотеки не всегда могут удовлетворить всех пользователей, в статьях были рассмотрены различные способы создания конструктором собственных приложений от простых утилит до сложных модулей, обладающих мощной функциональностью.
Наверняка искушенные пользователи КОМПАС-3D знают и активно применяют эти возможности. Данный материал поможет систематизировать их знания о системе и ее приложениях. Полезной окажется данная статья и для молодых специалистов конструкторско-технологических отделов, которые зачастую являются экспертами при выборе и внедрении САПР. Надеемся, вышеизложенная информация будет учтена при принятии важных решений и генерации новых идей и в конечном счете будет способствовать повышению качества проектируемой продукции.
Оцените статью:Право на использование АСКОН Обновление Библиотеки элементов электрических схем на КОМПАС-Электрик v18
Основные характеристики
Категория
Организация
Назначение
Проектирование и разработка документации
Версия
КОМПАС-Электрик v18
Платформа
Десктоп
ОС
Windows
Срок использования
Бессрочное
Язык интерфейса
Русский
Форма поставки
Конверт
Объект лицензирования
Пользователь
Количество лицензируемых объектов
1
Входит в единый реестр российских программ для ЭВМ и БД
Да
Совместимость
Версии Windows
10, 8, 7 SP1
Особенности
Основные функции КОМПАС-Электрик
Вставка УГО из библиотеки в схему, его обработка и выполнение контрольных операций
Есть
Построение и редактирование линий электрической связи, электрических шин, групповых линий связи
Есть
Ручная и автоматическая расстановка маркировки проводов
Есть
Автоматическая расстановка УГО на схеме электрической соединений, схеме подключений и схеме общей
Есть
Полуавтоматическое формирование технологической карты раскладки проводов
Есть
Экспорт документов проекта в КОМПАС-График
Есть
Добавление в проект 3D-моделей и текстовых документов системы КОМПАС
Есть
Вставка спецсимволов линий связи (экран, кабель, коаксиальный проводник, скрутка и т. п.)
Есть
Оптимизация трасс прокладки проводов
Есть
Функция централизованной корректировки электрических связей в изделии
Есть
Автоматическое формирование клеммников по ходу работы над проектом
Есть
Специфические виды документов для описания работы ПЛК
Программа работы ПЛК
Есть
Схема подключения модулей ПЛК (входов/выходов)
Есть
Тактовая циклограмма
Есть
Ведомость комплектующих ПЛК
Есть
Таблица распределения памяти ПЛК
Есть
Список ошибок в программе работы
Есть
Журнал учета изменений
Есть
База данных системы содержит комплектующие изделия, применяемые в проектах, а также условные графические обозначения (УГО), используемые при создании схем электрического вида. База данных уже имеет первичное наполнение — около 6000 типоисполнений изделий и около 600 графических обозначений. В любой момент времени в нее можно добавлять новые комплектующие изделия и УГО. База может работать на платформе СУБД Microsoft SQL Server, Microsoft Access, Borland InterBase, Oracle. Также в состав системы входит база данных продукции фирмы Schneider Electric, которая содержит более 1800 комплектующих изделий и их описаний.
Системные требования
Процессор
С поддержкой инструкций SSE2
Видеокарта
С поддержкой OpenGL 2.0
Оперативная память
2 ГБ, рекомендуется 8 ГБ и более
Место на диске
Не менее 2,3 ГБ
Монитор
С разрешением 1920х1080 или более
Старинный компас | Для продажи на compasslibrary.com — Библиотека компаса
Фильтр Filter18th Century19th Century20th Century24th Regiment3rd Border Regiment7.9mm MauserAlexander из ManchesterAluminium compassAnkle PedometerAntique высотомер BarometerAntique CompassAntique opisometerAntique карманного BarometerAntique Scientific InstrumentAntique sundialArtilleryArtillery compassAston & ManderBalloonBalloonistBalmain светящегося paintBarker compassBarker Mk III CompassBarker о патентной Универсальной CompassBarometerBattle из SommeBirminghamBoer warBorder RegimentBosworth в patentBrass Box CompassBrass CompassBrass Карманного BarometerBrass Карманного CompassBritish ArmyBritish EmpireBroad СтрелаБрунтонБрунтон КомпасКомпас пулиКембриджКапитан Ричард ДеннисКапитан У.E. Kelly M.C. Гильза для патрона, компасЧарльз Хайамс, Рождество 1914 г., Рождественское перемирие 1914 г.компас, поворотная головка, настольный компас, Доллон, компас DRP, Эд Коэн, образовательный компас, английский карманный компас, компас для спасения, высотомер для исследователя F. Баркер и сын Ф. Баркер (1932) Ф. Баркер CompassField SketchingFirst Мир WarFrancis BarkerFrancis Баркер M-73Francis Баркер M72French 75мм GunFrench ArmyFrench compassGallipoliGeologyGeorge Адамс Fleet StreetGeorge IVGeorgian CompassGerman armyGerman compassGlow иглы compassGreencard compassGrenadier GuardsGroves & BarkerHallmarked silverHenri ChatelainHenry KaterHitler YouthHoughtons LtdHuet из ParisHuet RangefinderHunter caseHunter обсаженных compassHymans Диапазон Патентный FinderHymans Range FinderImproved Colonial CompassIndiaIndian ArmyJ.Х. Стюард J. Х. Стюард Лтд., Лондон J. Halden & Co. LtdJ. HicksJ. Хикс Хаттон GardenJames Паркс BirminghamJapanese наручного CompassJesse RamsdenLawrence и MayoLeather CaseLewis NightingaleLieut-полковник Фрэнсис Боуэна DSOLiquid Призматического CompassLondonLondon SilverLoyal Северного Lancs Regimentluminous compassM 88M 88 CompassM-71 CompassM-72Й-72 CompassM-73M73 compassM88Machine пистолет CorpsMade в JapanMahogany CompassMahogany карманного compassMajor Гилберта LeghMajor Legh в Патентном CompassMap MeasurerMarching compassMarsch KompassMauserMauser стрелковой 1898MesopotamiaMessines 1917Mica DialMilitaryMilitary compassMilitary запястье compassMilliemesMilsMiniature compassMining compassMk V CompassMK VI compassmother из pearlMother перламутровых compassNATONavigationNavy CompassNCO в compassNickel серебра caseNickel-серебро compassNight MarchingNight походный compassOfficer в compassOmmdurmanOpticiansPantochronometerPebble Lens CompassPedometerPocket BarometerPocket compassPocket rangefinderPocket SundialPocket часы compassPresentation compassPrismatic compassProspecting compassPys эр OpticsPyser SGIRAFRailway compassrangefinderRangefinder instructionsRegistered узор CompassRFCRGS compassRichard Molesworth DennysRossRossignolRotameterRoyal Air ForceRoyal ArtilleryRoyal Летучий CorpsRoyal Ирландский полк compassSamuel Berry SingerSamuel FreemanSamuel SingerSchmalcalder CompassSchmalcalder в patentScientific instrumentsScouting compassService узор PatentSitometerSitometreSolid серебро compassShallow HunterSilvaSilver compassSinger в compassSomme июля 1916South Уэльс BorderersStanley LondonSterling silverStescoStesco CompassSudanSundialSundial compassSurveyingSurveyors compassT.Cooke & SonsТермометрТретий РейхТомас АрмстронгТомас Армстронг и братьяТомас Армстронг МанчестерТомас ДжонсТорговая марка ЛондонПрозрачный карманный компасTroughton & SimmsПатент Вернера Компас для конного рисунка ВернераПатент ВернераКарманный компас ВернераВинтажный компасометрВикторианский компас GregoryW. Патентный клинометр компании Gregory & Co УоткинЗападная ГерманияЗападная ГерманияУильям ШмалькальдерДеревянный компасНаручный компасНаручный шагомерWW1WW1 КомпасWW2 КомпасYork
124 товаров
Сортировать СортировкаЛучшие продажиАлфавитный, A-ZАлфавитный, Z-APЦена, от низкой к высокой Цена, от высокой к низкойДата, от новых к старымДата, от старых к новым
Полевое снаряжение | Compasslibrary.com — Библиотека компаса
Фильтр Filter.303 ammunition.303 Максим машина Gun19th Century20th Century24th Regiment3rd Border RegimentAir MinistryAircrewAluminium compassAntique CompassAntique LevelArtilleryArtillery compassAston & ManderAviationAviation booksBaleenBalmain светящемся paintBandolierBarker compassBarker Mk III CompassBattle из BritainBattle из SommeBoer warBorder RegimentBosworth в patentBrass CompassBritish ArmyBritish EmpireBritish OfficerBroad ArrowBruntonBrunton CompassCambridgeCaptain Richard W. DennysCaptainЭ. Келли M.C. Чарльз ХайамсРождество 1914 г.Рождественское перемирие 1914 г.компасДоллондКомпас DRPЭд КоэнКомпас для спасения F. Баркер (1932) Ф. Компас БаркераПолевое снаряжениеЭскизы поляПервая мировая войнаФрансис БаркерФрансис Баркер M-73Франсис Баркер M72Франсис Баркер M72Французская 75-мм пушкаФранцузская армияГаллиполиГенеральный штабГеологияНемецкий компасКомпас GreencardГранатыГренадерская гвардияHitler YouthHoughtons Ltd. Х. Стюард J. Х. Стюард Лтд., Лондон J.Halden & Co. LtdJ. HicksLee Энфилд RifleLieut-полковник Фрэнсис Боуэн DSOLiquid Призматический CompassLondonLoyal Северный Lancs Regimentluminous compassM 88M 88 CompassM-71 CompassM-72М-72 CompassM-73M73 compassM88Machine GunMachine пистолет CorpsMachine пистолет Обучение 1925Major Гилберта LeghMajor Legh в патент CompassMarching compassMarsch KompassMaxim GunMesopotamiaMessines 1917MilitariaMilitaryMilitary BooksMilitary compassMilitary запястья compassMilliemesMilsMk V CompassMK В.И. compassmother из pearlMother Нот NotesPilot Перл compassMusketryNATONauticalNavalNavigationNCO в compassNight MarchingNotre Дам де LoretteOfficer в compassOmmdurmanOpticiansPhotographyPilot для SpitfirePocket compassPocket rangefinderPrismatic compassPyser OpticsPyser SGIRadarRAFRAF FighterRAF Обработка SquadronrangefinderRangefinder instructionsReconnaissance photographsRegistered модель CompassRFCRichard Molesworth DennysRifleRossignolRoyal Air ForceRoyal ArtilleryRoyal Летучий CorpsRoyal ирландский полк compassSchmalcalder CompassScie Контрольные приборы, служебный образец, компас, Сильва, Патент Зингера, Ситометр, Ситометр, Малое оружие, Сомма, июль 1916 года, граница Южного Уэльса, Спитфайр, командир эскадрильи Р.Л. ФуллерСтэнли ЛондонСуданСверхмариновый СпитфайрСюрвейерский уровеньСюрвейерский компастелескопТретий РейхТомас Армстронг и братьяТоп секретный RAF РуководствоКартранцовая война ОкопыПатентный компас ВернераКомпас для кавалерии ВернераПатент ВернераСтаринный компас компасаВернеровский компасВинтажный компас компасаВернера GregoryWar Office Патентный клинометр УоткинаКитовая костьВторая мировая войнаНаручный компасWW1WW1 КомпасWW2WW2 Компас
48 товаров
Сортировать СортировкаЛучшие продажиАлфавитный, A-ZАлфавитный, Z-APЦена, от низкой к высокой Цена, от высокой к низкойДата, от новых к старымДата, от старых к новым
Как сельские библиотеки повышают навыки чтения · Giving Compass
Давать компас:
• Программа стипендий для сельских библиотек, финансируемая за счет гранта Института музейного и библиотечного обслуживания и фонда «Спасите детей», пытается укрепить сельские библиотеки, чтобы они способствовали развитию навыков чтения в третьем классе.
• Каков уровень грамотности чтения в сельской местности? Как доноры могут помочь распространить информацию об этой проблеме?
• Прочтите о важности умения читать на уровне своего класса и о том, как спонсоры могут помочь.
Двухлетняя стипендия для сельских библиотек, финансируемая за счет гранта Института музейного и библиотечного обслуживания и фонда «Спасите детей», пытается повысить потенциал библиотек и «активировать библиотеки для чтения в третьем классе», по словам Дримы Джентри, исполнительного директора. партнеров по образованию в Berea College.«В сельской местности центром внимания являются библиотека и школа, — сказал Джентри. «Мы действительно сосредоточены на том, как библиотеки могут улучшить результаты для детей».
По всей стране, по крайней мере, шестнадцать штатов и Вашингтон, округ Колумбия, требуют, чтобы школы удерживали большинство учащихся, не умеющих читать, к концу третьего класса. Исследования показывают, что если к третьему классу учащиеся не будут читать на уровне своего класса, они с меньшей вероятностью закончат среднюю школу. Стипендия для сельских библиотек проводится в то время, когда результаты тестов показывают, что многие ученики утратили навыки чтения и из-за пандемии все больше читают ниже уровня своего класса, чем в прошлом году.Педагоги говорят, что в этом году у многих детей нет доступа к книгам в школе из-за протоколов, связанных с пандемией.
Некоторые библиотеки по всей стране пытались вводить новшества во время пандемии, предлагая мобильные библиотеки, время для рассказов на открытом воздухе и рассылку книг детям дома. С запуском новой программы стипендий двадцать два сотрудника сельских библиотек по всей стране получат профессиональное развитие по таким темам, как наука о мозге и ранняя грамотность, а также будут обучены тому, как они могут помочь в повышении грамотности.Стипендиаты получат небольшую стипендию и проектные средства для создания программы обучения грамоте в своей библиотеке. Некоторые примеры: пополнение библиотек книгами, соответствующими культурным традициям, или интерактивные мероприятия, такие как «прогулка с рассказами», включающая литературные элементы через пешеходную тропу.
Прочтите полную статью Джеки Мэдера о том, как сельские библиотеки способствуют развитию навыков чтения, в The Hechinger Report.
Хотите узнать больше о COVID-19? Другие читатели Giving Compass сочли следующие статьи полезными для оказания воздействия, связанного с COVID-19.
Пандемия COVID-19: инструментарий и руководство для доноров
Мы находимся в муках глобальной пандемии. На момент написания этой статьи случаи COVID-19 были обнаружены в 211 странах и территориях, что создает чрезмерную нагрузку на системы здравоохранения в таких разных странах, как США, Италия, Иран, Бразилия и Индия. Самый эффективный, широко применяемый инструмент сдерживания болезни — социальное дистанцирование — остановил экономику, оставив закрытыми предприятия, закрытые школы, миллионы людей без средств к существованию, а людей во всем мире изолированными как от близких, так и от тех, кто обычно оказывал бы поддержку.На этом фоне возникает вопрос как для индивидуальных доноров, так и для институциональных грантодателей: чем я могу помочь? Здесь вы найдете ответ нашей команды на этот вопрос. В течение нескольких недель мы изучали сотни источников информации, включая отчеты учреждений здравоохранения; основные СМИ; счета первого респондента; соответствующие исторические свидетельства прошлых пандемий и бедствий; Сеть грантодателей, некоммерческих организаций и посредников CHIP; и опросы в реальном времени, моделирование и данные ученых и практиков — чтобы дать ответы на этот вопрос.Наши ответы делятся на категории ниже. Эффективное антикризисное реагирование и предоставление грантов Срочные нужды и некоммерческие организации, которым нужно пожертвовать Список некоммерческих организаций, фондов и ресурсов Что дальше: помимо сиюминутных потребностей Прочтите полную статью о руководстве по COVID-19 для доноров в Центре высокоэффективной благотворительности.
Ищете способ принять участие?
Если вы ищете возможности для обучения и общения с другими людьми, интересующимися темой «Дети и молодежь», обратите внимание на эти мероприятия, гала-концерты, конференции и возможности для волонтерства, собранные Giving Compass.
Готовы отдать?
Дети и молодежь — важная тема. Другие участники сочли, что эти благотворительные фонды, благотворительные организации и проекты, объединенные Giving Compass, имеют отношение к людям, страстно увлеченным детьми и молодежью.
КОМПАС для быстрой комбинаторной оптимизации биохимических путей на основе искусственных факторов транскрипции
Общие
Список S.cerevisiae , использованные в этом исследовании, и их генотипы приведены в дополнительных данных 7. Плазмиды были сконструированы с помощью сборки ДНК NEBuilder HiFi (New England Biolabs, Франкфурт-на-Майне, Германия) и клонирования SLiCE 43 . Последовательности плазмид и праймеров приведены в дополнительных данных 14 и дополнительных данных 15. ПЦР-амплификации фрагментов ДНК проводили с использованием высокоточных полимераз: фьюжн-полимеразы (Thermo Fisher Scientific), ДНК-полимеразы Q5 (New England Biolabs) или ДНК-полимеразы PrimeSTAR GXL ( Takara Bio, Saint-Germain-en-Laye, France) в соответствии с рекомендациями производителя.Части амплифицированной ДНК очищали в геле перед дальнейшим использованием, если не указано иное. Более того, фрагменты, амплифицированные с помощью мультиплексной ПЦР, не очищались в геле (дополнительные методы). Все праймеры и олигонуклеотиды были заказаны в Eurofins Genomics (Эберсберг, Германия). Все конструкции подтверждены секвенированием (LGC Genomics, Берлин, Германия).
Штаммы бактерий и дрожжей
Плазмиды трансформировали в клетки E. coli NEB 5α или NEB 10β (New England Biolabs) или в компетентные клетки ElectroSHOX (Bioline, Luckenwalde, Германия).Штаммы выращивали в среде Луриа-Бертани с соответствующим маркером селекции при 28 ° C (триклозан, 14,5 мкг / мл) или 37 ° C (спектиномицин, 50 мкг / мл, ампициллин, 50 мкг / мл, хлорамфеникол, 25 мкг / мл; гентамицин, 50 мкг / мл).
S . Использовали штаммы cerevisiae YPH500 (ATCC: 76626), IMX672 (Euroscarf, # Y40595) и SCIGS22a 30 . Информация о дрожжевых штаммах, созданных в этой работе, представлена в дополнительных данных 7. Генерация компетентных дрожжевых клеток и генетическая трансформация плазмид или линеаризованных фрагментов ДНК проводились с использованием метода LiAc / SS-носитель ДНК / PEG 44 или The Frozen-EZ Набор для трансформации дрожжей II (Zymo Research, Фрайбург, Германия).Все штаммы выращивали при 30 ° C в среде, обогащенной дрожжевым экстрактом, пептон-декстрозой и аденином (YPDA), или в соответствующей синтетической полной (SC) среде, в которой отсутствует одна или несколько аминокислот, чтобы обеспечить возможность отбора трансформированных клеток. Доминантные маркеры отбора использовали в среде YPDA в указанных конечных концентрациях: G418 (200 мкг / мл), гигромицин B (200 мкг / мл), флеомицин (20 мкг / мл), блеомицин (100 мкг / мл) и норзотрицин ( 100 мкг / мл). Проверка трансформации проводилась с помощью ПЦР колоний с последующим секвенированием.Для выделения плазмидной ДНК из клонов положительных дрожжей использовали либо набор Zymoprep Yeast Plasmid Miniprep II (Zymo Research), либо способ выделения высококачественной кольцевой плазмидной ДНК в количествах 27 микрограммов.
Конструирование плазмид pCOM для генерации штамма
pCOM001: Донорные и прямые повторяющиеся последовательности, необходимые для разрушения маркеров ауксотрофной селекции дрожжей, были созданы путем синтеза гена и вставлены в плазмиду pEXA2 с помощью MWG Eurofins для создания плазмид pCOMA и pCOMB.Плазмиды служили матрицами для ПЦР-амплификации фрагментов A (праймеры COMA_for / COMA_rev, на pCOMA) и B (праймеры COMB_for / COMB_rev, на pCOMB). Два фрагмента были индивидуально собраны в плазмиду pCRCT, расщепленную Bsa I (Addgene # 60621), и полученные плазмиды были названы pCOMC (содержащая фрагмент A) и pCOMD (содержащая фрагмент B). Затем амплифицированный с помощью ПЦР фрагмент B (праймеры COMD_for / COMD_rev, на pCOMD) собирали в pCOMC, расщепленную Bsa I. Полученная плазмида была названа pCOM001 и использовалась для разрушения маркерных генов LEU2 , HIS3 , LYS2 и TRP1 .
pCOM002: Для конструирования pCOM002, ПЦР-амплифицированный ген neo (праймеры KAN_for / KAN_rev, на pTAJAK92 45 ), фрагмент, содержащий терминатор CYC1 — структурная РНК — STU4 терминатор (tCYC1_ для tCYC1_ BY4741) и фрагмент SNR52 (праймеры SNR_for / SNR_rev, на pCRCT, Addgene # 60621) собирали в pCOM001, расщепленную Bsa I. Полученная плазмида была названа pCOM002.
pCOM003: ориджин репликации CEN / ARS (CEN_for / CEN_rev, на pGN006 4 ) клонировали в pGN003B 4 , расщепленную Pme I, для конструирования pGN003BM.Затем плазмиду pCOM003 конструировали сборкой Гибсона, амплифицируя транскрипционную единицу Cre-EBD из pDL12 32 , и ее вставляли в pGN003BM 4 , расщепленную Eco RI / Sac II.
pCOM004: кодирующий фрагмент LYS2 (LYSA_for / LYSA_rev, на pYC6Lys-TRP1URA3, Addgene # 11010) и кодирующий фрагмент iCas9 (CASA_for / CASA2_rev, на pCRCT621) были клонированы N Not 60 / Ico , Addgene # , Icoon 60/2006, Addgene # , клонирован в IQT621, был клонирован. I-переваренный pTAJAK-92 45 .
pCOM005: кодирующий фрагмент LYS2 (LYSA_for / LYSA_rev, на pYC6Lys-TRP1URA3, Addgene # 11010) и кодирующий фрагмент iCas9 (CASA_for / CASA_rev, на pCRCT) были клонированы в Icoph с дайджестом Ncoph / Ncoph65 Icoph Icoph65 pCfB3052 (Добавить # 73294).
pCOM006: кодирующий фрагмент LYS2 (LYSB_for / LYSA_rev, в pYC6Lys-TRP1URA3, Addgene # 11010), кодирующий фрагмент iCas9 (CASA_for / CASB_rev, в pCRCT_ 900, Addgene # 60phoding 900, Addgene # 60phoding_for66, Addgene № 60 / HYG_rev в акцепторном векторе H, см. Раздел вектора COMPASS) были клонированы в Sfo I-расщепленную pTAJAK-105 46 .
pCOM007: кодирующий фрагмент LYS2 (LYSA_for / LYSA_rev, на pYC6Lys-TRP1URA3, Addgene # 11010) и кодирующий фрагмент iCas9 (CASA_for / CASA_rev, на pCRCT) были клонированы в Icoph-кодирующий код Ncoph / Icoph Icoph с дайджестом Icoph. pCfB3051 (Добавить # 73293).
pCOM008: Кодирующий фрагмент LYS2 (LYSA_for / LYSA_rev, на pYC6Lys-TRP1URA3, Addgene # 11010) был клонирован в Nco I / Sph I-переваренный pCfB303295 (Addgene # 7).
pCOM009: Для конструирования pCOM009 фрагменты C (праймеры COMC1_for и COMC1_rev, на отожженных одноцепочечных олигонуклеотидах COMC2_for / COMC2_rev) и D (праймеры COMD1_for / COMD2_rev, на отожженных одноцепочечных олигонуклеотидах COMD2_rev, на отожженных одноцепочечных олигонуклеотидах COMD2_rev, на отожженном одноцепочечном олигонуклеотиде COMD2_rev) былиЗатем фрагменты C и D, расщепленные Bsa, I, вставляли в плазмиду pCRCT, расщепленную Bsa I (Addgene # 60621). Полученная плазмида была названа pCOMCD. Затем фрагмент E (праймеры COME1_for / COME1_rev, на отожженных одноцепочечных олигонуклеотидах COME2_for / COME2_rev) амплифицировали с помощью ПЦР с последующим расщеплением с Bsa I и клонированием в pCOMCD, расщепленную Bsa I. Полученная плазмида была названа pCOM009 и использовалась для разрушения генов ble , nat1 , blp R , neo и hph .
Конструирование штаммов дрожжей
Штамм Gen 0.1: S . cerevisiae штамм SCIGS22a 30,47 был использован в этой работе для создания штамма Gen 0.1. Штамм SCIGS22a имеет фон CEN.PK с дополнительными модификациями в геноме для сверхаккумуляции FPP 30,47 и является ауксотрофным для URA3 . COMPASS использует схему положительного отбора, которая включает пять генов ауксотрофных маркеров. Кодирующие последовательности маркера находятся внутри векторных скелетов, а соответствующие им промоторы являются частью сборочных фрагментов, используемых в реакции TAR.Промотор управляет экспрессией соответствующего ауксотрофного маркера только в успешно собранных конструкциях. Следовательно, SCIGS22a должен быть ауксотрофным для HIS3 , LEU2 , TRP1 и LYS2 в дополнение к URA3 . Следовательно, мы использовали систему Homology-Integrated CRISPR-Cas (HI-CRISPR) и ее принципы проектирования для одноэтапного нарушения множественного ауксотрофного гена 33 . HI-CRISPR использует плазмиду pCRCT (Addgene, # 60621), высококопийную плазмиду, несущую iCas9, вариант Cas9 дикого типа (WT), который увеличивает эффективность разрушения гена, транскодируемую РНК (tracrRNA) и гомологичный интегрированная кассета crRNA.Он основан на вставке дцДНК длиной 100 п.н., мутагенизирующей донор гомологичной рекомбинации, между двумя прямыми повторами в случае каждого гена-мишени. В pCRCT можно ввести несколько доноров и соответствующие направляющие последовательности. Для каждого нарушения гена с помощью поисков BLAST против S была выбрана gRNA, нацеленная на уникальную последовательность длиной 20 пар оснований. cerevisiae S288c геном (код таксономии NCBI: 559292), чтобы минимизировать нецелевые эффекты. На следующем этапе плазмида pCOM001 для четырехкратного разрушения ауксотрофного гена (см. Выше и дополнительный рис.9а) был преобразован в S . cerevisiae клеток SCIGS22a. Следовательно, leu2.a (519 п.н. ниже стартового кодона LEU2 ), his3.a (265 п.н. ниже стартового кодона HIS3 ), lys2.a (799 п.н. старт-кодона LYS2 ) и trp1.a (245 п.н. ниже стартового кодона TRP1 ) были нацелены на достижение мутаций со сдвигом рамки считывания. Трансформированные клетки инокулировали в жидкую культуру SC-Ura в течение ночи.Через 4 дня 200 мкл разведенной в 10 4 -кратной культуры клеток высевали на планшеты SC-Ura. Через 2 дня было случайным образом отобрано всего 50 колоний, и каждая отдельная колония была нанесена штрихами на четыре различных селективных чашки (т.е. SC-Leu, SC-His, SC-Lys и SC-Trp). Еще через 2 дня клетки колонии, которые не росли ни на одном из четырех селективных планшетов, наносили штрихами на неселективную агаризованную среду YPDA для удаления плазмиды pCOM001. После четырех раундов повторного нанесения отдельных колоний на новые чашки YPDA мы выделили колонию, которая также не могла расти на среде SC-Ura.Новый штамм получил название Gen 0.1.
Штамм IMX672.1: для достижения мутации со сдвигом рамки lys2.a в штамме IMX672 (полученном из штамма CEN.PK) в этот штамм трансформировали плазмиду pCOM001 и проводили отбор, как описано для Gen 0.1 выше. Тридцать колоний случайным образом наносили штрихами на чашки SC-Lys и YPDA. Колония, которая не росла на чашке SC-Lys, несет мутацию сдвига рамки lys2.a . Чтобы удалить pCOM001, соответствующую колонию повторно штриховали несколько раундов на планшетах YPDA и SC-Ura, что дало колонию, которая не могла расти на SC-Ura.Соответствующий штамм был назван IMX672.1.
Штамм MXFde 0.2: S . cerevisiae штамм TSINO93 (репортерный штамм на основе FdeR) 31 имеет фон CEN.PK с Pro TDh4 — FdeR-URA3 и Pro CYC1-FdeO -GFP -LoxP-HphMX-LoxP и является ауксотрофным для LEU2 и TRP1 . COMPASS использует схему положительного отбора, которая включает ауксотрофные и доминантные маркерные гены.Следовательно, TSINO93 должен быть ауксотрофным для HIS3 , URA3 и LYS2 , в дополнение к LEU2 и TRP1 , а доминантный маркер HphMX необходимо удалить из штамма. Мы использовали метод HI-CRISPR для одноэтапного разрушения нескольких генов 33 . С этой целью фрагмент, кодирующий гРНК, нацелен на последовательность 133 п.н. ниже стартового кодона URA3 (отожженные одноцепочечные олигонуклеотиды URA3.A_for / URA3.A, дополнительный рисунок 9b, c) и плазмида pCOM002 (см. Выше и дополнительный рисунок 9c) котрансформировали в штамм TSINO93 для достижения мутации со сдвигом рамки считывания. Двести микролитров разведенной в 10 4 раз культуры клеток высевали на планшет YPDA с G418. Через 2 дня было случайным образом отобрано всего 50 колоний, и каждая отдельная колония была нанесена штрихами на три различных селективных чашки (т.е. SC-His, SC-Lys и SC-Ura). После нескольких циклов повторного пересева отдельных колоний на новые чашки YPDA мы выделили колонию, которая также не могла расти на среде YPDA с норсеотрицином.Еще через два дня клетки колонии, которые не росли ни на одном из трех селективных планшетов, наносили штрихами на неселективную агаризованную среду YPDA для удаления плазмиды pCOM002. Новый штамм получил название MXFde 0.1. Для создания штамма MXFde 0.2 мы использовали β-эстрадиол (EST) -индуцированную Cre-рекомбиназу 48 для удаления HphMX CDS, фланкированных сайтами loxPsym . Плазмида pCOM003 была сконструирована, как описано, и трансформирована в клетки MXFde 0.1. Культуру клеток EST-Cre высевали на среду SC-Trp.Через 3 дня отдельные колонии инокулировали в жидкой среде SC-Trp и выращивали в темноте в течение 6 часов при 30 ° C и 230 об / мин, затем индуцировали 2 мкМ β-эстрадиола (Sigma-Aldrich, Мюнхен, Германия) и выращивали для другого. 24 ч. Двести микролитров разведенной в 10 4 -кратной культуры клеточной культуры высевали на планшеты YPDA, содержащие 200 мкг / мл гигромицина B. После нескольких циклов повторного нанесения отдельных колоний на новые планшеты YPDA мы выделили колонию, которая также не была способен расти на среде YPDA с гигромицином B.Положительную колонию проверяли с помощью ПЦР на удаление HphMX CDS. Еще через два дня клетки колонии, которая не росла на селективных планшетах, наносили штрихами на неселективную агаризованную среду YPDA для удаления плазмиды pCOM003. Новый штамм получил название MXFde 0.2.
Конструирование плазмид COMPASS
Все этапы клонирования выполняются с использованием методов на основе перекрытия. С этой целью в праймеры, используемые для ПЦР-амплификации соединяемых фрагментов ДНК, включают области, гомологичные соседним фрагментам.
Вектор входа X: pGN003B 4 расщепляли с помощью Pme I и повторно лигировали с получением pCOMPASS01. Затем pL0A_0_1 32 был разрезан с помощью Asc I / Fse I и использован в реакции сборки с использованием ПЦР-амплифицированного Pro TEF1 — LacI — Ter ADh2 (праймеры LAC_for / LAC_rev на pCOMPASS01) для создания pCOMPASS02. Not I / Pac I-расщепленную pCOMPASS02 использовали в реакции сборки с использованием ПЦР-амплифицированного Pro TRP1 (праймеры PTRP_for / PTRP_rev на геномной ДНК BY4741).Таким образом, сайты Bam HI и Sal I были представлены ниже по течению от Pro TRP1 , а сайт Pac I был представлен выше по течению от Pro TRP1 . Полученная плазмида была названа pCOMPASS03. Плазмиду pCOMPASS03 расщепляли Sbf I, обрабатывали ДНК-полимеразой Т4 для удаления 3′-выступающего конца и повторно лигировали. Полученная плазмида была названа pCOMPASS04. Bam HI / Sal I-переваренный pCOMPASS04 использовали в реакции сборки с отожженными одноцепочечными олигонуклеотидами CYCM_for / CYCM_rev, вводя MCS и X0 , последние 30 п.н. из Pro , последние 30 п.н. между Pro TRP1 и E . coli ori . Полученная плазмида была названа Entry vector X.
Акцепторные векторы A – D: для конструирования первого набора (набор 1) акцепторных векторов, содержащих маркеры ауксотрофной селекции, использовали Bam HI / Not I-переваренную pCOMPASS04 в Реакция сборки с использованием ПЦР-амплифицированных частей ДНК следующим образом: (i) pL0A_0_1 32 был разрезан с помощью Not I. Двустороннее клонирование Гибсоном Pro KanaR (праймеры PKANA_for / PKANA_rev, на pCR4-topo, Invitrogen, Карлсруэ, Германия), Amp R (праймеры AMP_for / AMP_rev, на pGN005B 4 ) и Ter KanaR (праймеры TKANA_for / TKANA_rev, на pCR4-topo, Invitrogen).Полученная плазмида была названа pCOMPASS05. HIS3 и Ter HIS3 (праймеры HISTERA_for / HISTERA_rev, на pGN005B 4 ), Pro HIS3 (праймер PHIS_for / PHIS_rev , на pGN005B) R и Ter KanaR (праймеры AMPTER_for / AMPTER_rev, на pCOMPASS05) для получения акцепторного вектора A. (ii) LEU2 и Ter LEU2 (праймеры LEUTER_rev, LEUTER_rev / LEUTER_rev на pGAD424, TAKARA Bio, GenBank # U07647), Pro LEU2 (праймер PLEU_for / PLEU_rev, на pGAD424, TAKARA Bio, GenBank # U07647), Cm R Ter CmR (праймеры CMRTER_for / CMRTER_rev, на pLD_3_4 32 ) для получения акцепторного вектора B.(iii) TRP1 и Ter TRP1 (праймер TRPTERC_for / TRPTERC_rev, на pGN003B 4 ), Pro TRP1 (праймеры PTRP_for / PTRPGN0067, на pGN003B , на pTRP_rev ) TCS R и Ter TCSR (праймеры TCSRTER_for / TSCRTER_rev, на pF2, Addgene # 42520) для получения акцепторного вектора C. (iv) LYS2 и Ter LYS2 LYS2 (праймеры LYSTERA_for / LYSTERA_rev, на pYC6Lys-TRP1URA3, Addgene # 11010), Pro LYS2 (праймеры PLYS_for / PLYS_ter, на pYC6Lys-11010, pYC6Lys-11010, pYC6Lys-110101URA и Ter GenR (праймеры GENTER_for / GENTER_rev, на pDEST321) для получения акцепторного вектора D.
Вектор назначения I: pCOMPASS03 был обработан с помощью Pac I и Cla I для удаления Pro URA3 — URA3 — Ter URA3 из нижнего (справа) потока E . coli ori . Затем вектор размером ~ 5 т.п.н. использовали в реакции сборки с использованием ПЦР-амплифицированного фрагмента (праймеры MURA_for / MURA_rev, на pCOMPASS03). Полученная плазмида была названа pCOMPASS06. Для конструирования pCOMPASS07, Not I / Pac I-расщепленную pCOMPASS06 использовали в реакции сборки с использованием ПЦР-амплифицированного Pro URA3 (праймеры URATERI_for / URATERI_rev, на pCOMPASS03 амплифицированный ) и PCRRA-900 — Ter URA3 (грунтовка PURAI_for / PURAI_rev, на pCOMPASS04).Следовательно, сайт Not I был введен между Pro URA3 и URA3 CDS, а сайты Bam HI и Pac I были вставлены ниже по течению от сайта X0 . Для конструирования pCOMPASS08, Bam HI / Pac I-гидролизованный pCOMPASS07 использовали в реакции сборки с использованием Spect R -Ter SpectR (праймеры SPECTERI_for / SPECTTERI_rev, на pCOMPASS07 / GW / TOPO, набор для клонирования TOPO, TAKARA).Таким образом, семь нуклеотидов были удалены перед SpectR R , и сайт Pac I был вставлен ниже Ter SpectR . Кроме того, pCOMPASS04, расщепленный Bam HI / Sal I, использовали в реакции двусторонней сборки с использованием ПЦР-амплифицированных частей ДНК следующим образом: (i) LYS2 и Ter LYS2 (праймеры LYSTERI_for / LYSTERI_rev, на pYC6Lys-TRP1URA3, Addgene # 11010) и отожженных одноцепочечных олигонуклеотидов LYSX0_for / LYSX0_rev с получением pCOMPASS09.Таким образом, последовательность X1 , сайт Asc I и Y4 были введены между сайтом LYS2 CDS и сайтом Pa cI. (ii) TRP1 и Ter TRP1 (праймер TRPTERI_for / TRPTERI_rev, на pGN003B 4 ) и отожженные одноцепочечные олигонуклеотиды TRPX0_for / TRPX0_re11. Таким образом, последовательность X1 , Sfi I и PI-Psp I сайтов и Y3 были введены между LYS2 CDS и Pa cI сайтом.(iii) LEU2 и Ter LEU2 (праймеры LEUTERI_for / LEUTERI_rev, на pGAD424, TAKARA Bio, GenBank # U07647) и отожженные одноцепочечные олигонуклеотиды в COMP0_rev12 до LEUX0_rev / LE. Таким образом, между LEU2 CDS и Pa cI были введены последовательности X1 , Fse I и I- Sce I и Y2 . (iv) HIS3 и Ter HIS3 (праймеры HISTERI_for / HISTERI_rev, на pGN005B 4 ) и отожженные одноцепочечные олигонуклеотиды HISX0_for / HISX0_rev, вводящие COMPASS13 HR.Таким образом, между HIS3 CDS и Pa cI были введены последовательности X1 , Sbf I и I-Ceu I и Y1 .
Далее, для конструирования pCOMPASS13.1, Pac I-переваренный pCOMPASS08 был использован в реакции сборки с ПЦР-амплифицированным фрагментом Ter HIS3 — HIS3 — X1 — I-Ceu I– Y1 (праймеры HIS_for / HIS_rev, на COMPASS13).Для конструирования pCOMPASS14, Fse I / Pac I-переваренный pCOMPASS13 использовали в реакции сборки с ПЦР-амплифицированным фрагментом Ter LEU2 — LEU2 — X1 — Fse II- Sce I– Y2 (праймеры LEU_for / LEU_rev, на pCOMPASS11). Для конструирования pCOMPASS15 использовали расщепленный Asc I / Pac I COMPASS13.1 в реакции сборки с использованием ПЦР-амплифицированного фрагмента Ter TRP1 — TRP1 – X1-SfiI – PI-PspI — Y3 (праймеры TRP_for / TRP_rev, на pCOMPASS10).Для конструирования вектора назначения I, pCOMPASS14, расщепленный Pac I, был использован в реакции сборки с ПЦР-амплифицированным фрагментом Ter TRP1 — TRP1 — X1 — Sfi I- PI-Psp I– Y3 — Ter LYS2 — LYS2 — X1 — Asc I– Y4 (праймеры TRPI_for / LYSI_rev, на pCOMPASS15). Для конструирования вектора-адресата I.1 отожженный одноцепочечный олигонуклеотид LYP_for / LYP_rev был переварен с помощью Pac I и лигирован в вектор-получатель, расщепленный Pac I.Посредством этого в плазмиду был введен фрагмент из 45 п.н. LHR — Pme I- Aat II-45 п.н. R_HR , который позволяет встраивать целевой вектор I.1, расщепленный с помощью Pme I или . Aat II в сайт LYP1.x 33 генома дрожжей.
Акцепторные векторы E – H: для конструирования второго набора (Набор 2) акцепторных векторов, содержащих доминантные маркеры резистентности, Bam HI / Not I-расщепленный pCOMPASS04 использовали в трехсторонней реакции сборки с использованием ПЦР- амплифицированные части ДНК следующим образом: (i) Nat1 и Ter FBA1 (праймеры NATRER_for / NATRER_rev, на pAG36, Addgene # 35126), Pro FBA1 (праймеры PFBA_rev, на PFAB_ pAG36, Addgene # 35126) и Amp R и Ter AmpR (праймеры AMPTERE_for / AMPTERE_rev, на pCOMPASS05), чтобы получить pCOMPASS16.Затем pCOMPASS16 был переварен с помощью Pci I и Nde I для удаления 264 п.н. из кодирующей последовательности URA3 . Оставшийся фрагмент размером ~ 6 т.п.н. использовали в реакции сборки с использованием отожженных одноцепочечных олигонуклеотидов DURA_for / DURA_rev. Полученная плазмида была названа акцепторным вектором E. (ii) Ble и Ter ble (праймеры BLERTER_for / BLERTER_rev, на pCEV-G1-Ph, Addgene # 46814), Pro PGK1 (праймер PGKF_for / PGKF_rev, на pCEV-G1-Ph , Addgene # 46814) и Cm R и Ter CmR (CMRTERF_for / CMRTERF_rev, на pLD_3674 900_3) результат pCOMPASS17.Затем pCOMPASS17 был переварен с помощью Pci I и Nde I для удаления 273 п.н. из кодирующей последовательности URA3 . Оставшийся фрагмент размером ~ 6 т.п.н. использовали в реакции сборки с использованием отожженных одноцепочечных олигонуклеотидов DURA_for / DURA_rev. Полученная плазмида была названа акцепторным вектором F. (iii) Neo и Ter neo (праймеры KANARTER_for / KANARTER_rev, на pCEV-G2-Km, Addgene # 46815), Pro TDh4 (праймеры TDHG_for / TDHG_rev, на pCEV-G2-Km, Addgene # 46815), TCS R и Ter TCSR (праймеры, на TCSRGTER_for / TSCRGTER_revgene на pF2 425, Add чтобы получить pCOMPASS17.Затем pCOMPASS18 был переварен с помощью Pci I и Nde I для удаления 273 п.н. из кодирующей последовательности URA3 . Оставшийся фрагмент размером ~ 6 т.п.н. использовали в реакции сборки с использованием отожженных одноцепочечных олигонуклеотидов DURA_for / DURA_rev. Полученная плазмида была названа акцепторным вектором G. (iv) Hph и Ter hph (праймеры HPHRTER_for / HPHRTER_rev, на pHIS3p: mRuby2-Tub1 + 3’UTR :: HPH, Addgene # 50633), Pro TEF1 (праймеры PTEFH_rev / PTEFH_rev, pHIS3p: mRuby2-Tub1 + 3’UTR :: HPH, Addgene # 50633), Gen R и Ter GenR 9027 (праймеры GENTERH_for / GENTERH_rev, TAKARA Bio), чтобы получить pCOMPASS19.Затем pCOMPASS19 был переварен с помощью AcI I и Cla I для удаления 974 п.н., включая Pro URA3 и первые 749 п.н. из URA3 CDS. Оставшийся фрагмент размером ~ 5,5 т.п.н. использовали в реакции сборки с использованием отожженных одноцепочечных олигонуклеотидов DDURA_for / DDURA_rev. Полученная плазмида была названа Акцепторный вектор H.
Целевой вектор II был сконструирован следующим образом: (i) Not I / I-Ceu I-расщепленная pCOMPASS12 была использована в реакции сборки с PCR-амплифицированным nat1 и Ter nat1 (праймеры NATRERII_for / NATRERII_rev, на pAG36, Addgene # 35126), чтобы получить pCOMPASS20.Таким образом, последовательность X1 , Sbf I и I — Ceu I сайты и последовательность Y1 были введены между nat1 CDS и Pa cI сайтом. (ii) Fse I / Not I-переваренный pCOMPASS11 использовали в реакции сборки с ПЦР-амплифицированными ble и Ter ble (праймеры BLERTERII_for / BLERTERII_rev, на pCEV-G1-Ph , Addgene # 46814), чтобы получить pCOMPASS21.Таким образом, последовательность X1 , Fse I и сайты I- Sce I и Y2 были введены между сайтом ble CDS и сайтом Pa cI. (iii) PI-Psp I / Not I-переваренный pCOMPASS10 использовали в реакции сборки с ПЦР-амплифицированными neo и Ter neo (праймеры KANARTERII_for / KANARTERII_rev, на pCEV-G2- Km, Addgene # 46815), чтобы получить pCOMPASS22. Таким образом, последовательность X1 , сайты Sfi I и PI-Psp I и Y3 были введены между сайтом neo CDS и сайтом Pa cI.(iv) Asc I / Not I-переваренный pCOMPASS09 использовали в реакции сборки с ПЦР-амплифицированными hph и Ter hph (праймеры HPHRTERII_for / HPHRTERII_rev, на pHIS3p: mRuby2-Tub 3′UTR :: HPH, Addgene # 50633), чтобы получить pCOMPASS23. Таким образом, между узлами Hph CDS и Pa cI были введены сайты X1 , Asc, I и Y4 .
Затем pCOMPASS06 был обработан с использованием Not I и Pac I для удаления Pro Trp1 .Оставшийся фрагмент размером ~ 5,2 т.п.н. использовали в реакции сборки с ПЦР-амплифицированными Spect R и Ter SpectR (праймеры SPECTII_for / SPECTII_rev, на pCOMPASS08) с получением pCOMPASS24. Pac I-переваренный pCOMPASS24 был использован в реакции сборки с ПЦР-амплифицированным фрагментом nat1 — Ter nat1 — X1 — Sbf I- I-Ceu I– Y1 (праймеры NATII_for / NATII_rev, по COMPASS21).Полученная плазмида была названа pCOMPASS25. Для конструирования pCOMPASS26, Fse I / Pac I-переваренный pCOMPASS25 использовали в реакции сборки с ПЦР-амплифицированным фрагментом Ble — Ter ble — X1 — Fse II- Sce I– Y2 (праймеры BLEII_for / BLEII_rev, на COMPASS22). Для конструирования pCOMPASS27, Fse I / Pac I-переваренный pCOMPASS22 использовали в реакции сборки с ПЦР-амплифицированным фрагментом hph — Ter hph — X1 — Asc I– Y3 (праймеры HPHRII_for / HPHII_rev, pCOMPASS26).Для конструирования pCOMPASS28 был использован pCOMPASS27, расщепленный Pac I в реакции сборки с ПЦР-амплифицированным фрагментом Hph — Ter hph — Asc I– Y3 — neo — Ter neo — X1 — Sfi I- PI-Psp I– Y4 (HPHRRII_for / HKANARII_rev, на pCOMPASS27). Not I-расщепленную pCOMPASS28 использовали в реакции сборки с отожженными одноцепочечными олигонуклеотидами RE_for / RE_rev.Благодаря этому, между последовательностью X0 и Spect R CDS были введены сайты Bam HI и Xho I. Полученная плазмида была названа pCOMPASS29. Не I-переваренный pCOMPASS29 был использован в реакции сборки с ПЦР-амплифицированным Pro TEF1 — blp R — Ter TEF1 (BLPR_for / BLPR_rev, on pAG31 , Addgene # 35124).Благодаря этому сайт Not I был введен между кодирующим фрагментом blp R и последовательностью X0 . Полученная плазмида была названа pCOMPASS30. Наконец, олигонуклеотиды ADE2A_for и ADE2A_rev были отожжены, и полученный двухцепочечный олигонуклеотид был расщеплен Pac I и лигирован в pCOMPASS30, расщепленный Pac I. Полученная плазмида была названа вектором назначения II. Посредством этого 45 п.н. LHR — Pme I- Pci I-45-п.н. RHR были введены в плазмиду, чтобы обеспечить интеграцию вектора назначения II после переваривания с Pme I или Pci. I, в ADE2.сайт генома дрожжей 33 .
Построение библиотеки ATF / BS
Мы выбрали три JUB1-, два ANAC102-, два ATAF1-, один RAV1- и один производный от GRF7 ATF. Кодирующие последовательности ATF получали с помощью ПЦР с использованием соответствующих плазмид экспрессии 4 в качестве матриц и соответствующих прямых (ATF-for) и обратных (ATF-rev) праймеров (см. Дополнительные методы). Соответствующие BS ( JUB1 2 × , JUB1 4 × , ANAC102 4 × , ATAF1 2 × , RAV1 4 × и GRF7 4 × ) слиты до минимума дрожжей CYC1 промотор получали с помощью ПЦР с использованием соответствующих репортерных плазмид 4 в качестве матриц и соответствующих прямых (BS-for) и обратных (BS-rev) праймеров (дополнительные методы).Оба фрагмента вставляли в вектор входа X, предварительно расщепленный с помощью Fse I / Asc I. Конструкции, содержащие ATF NLS-GAL4AD-RAV1 и NLS-GAL4AD-GRF7 (оба в комбинации с четырьмя копиями их BS перед минимальной CYC1 промотор) 4 клонировали в вектор входа X стандартным клонированием на основе перекрытия. Остальные комбинации ATF / BS были собраны с использованием комбинаторного подхода (см. Результаты). Для JUB1 три плазмиды экспрессии, содержащие NLS-JUB1-GAL4AD, NLS-DBD , JUB1, -GAL4AD и NLS-JUB1-EDLLAD-EDLLAD, были смешаны в молярном соотношении 1: 1: 1, и две репортерные плазмиды содержали две и две репортерные плазмиды. четыре копии JUB1 BS, соответственно, были смешаны в молярном соотношении 1: 1.Клонирование на основе перекрытия приводит к различным комбинациям между тремя ATF и двумя BS в векторе входа, включая три требуемые комбинации. Для ATAF1 фрагменты ДНК, кодирующие два ATF, полученных из ATAF1, смешивали в молярном соотношении 1: 1 и собирали путем клонирования на основе перекрытия с фрагментом промотора, содержащим две копии BS ATAF1. Для ANAC102 фрагменты ДНК, кодирующие два ATF, полученные из ANAC102, были смешаны в молярном соотношении 1: 1 и собраны путем клонирования на основе перекрытия с фрагментом промотора, содержащим четыре копии BS ANAC102.Таким образом, были сгенерированы девять различных производных X векторов входа, содержащих различные модули регулятора ATF / BS. Желаемые конструкции были идентифицированы с помощью ПЦР колоний с последующим секвенированием (ATF: праймеры EXSEQ-for и EXSEQ-rev; BS-Pro CYC1_mini и Pro TDh4 : PROSEQ-for и PROSEQ-rev ). Последовательности праймеров приведены в дополнительных данных 15.
Сборка генов пути
β-каротин и β-ионон: промоторы E . coli гены маркеров селекции, терминаторы дрожжей, соответствующие части CDS генов биосинтеза β-каротина ( BTS1 или GGPPSbc , оптимизированные по кодонам McrtI и McrtYB ) и β-ионона ( RiCCD1 ) были амплифицированы из разных источников геномной ДНК или плазмид. Вектор входа X был расщеплен с помощью Fse I и Asc I и трех фрагментов, включая CDS интересующего гена, терминатор дрожжей и промотор E .Был вставлен маркер селекции coli . Праймеры, используемые для амплификации, включали выступы с сайтами распознавания редких RE, совместимых с подходящим акцепторным вектором для следующих этапов клонирования. Все части были проверены секвенированием.
Нарингенин: Промоутеры E . coli маркерные гены селекции, соответствующие части CDS пути биосинтеза NG ( AtC4H: L5: AtATR2 , PhCHI , HaCHS , At4CL-2 и AtPAL-2 ), слитые с терминаторы были амплифицированы из разных источников плазмид и смешаны в эквимолярном соотношении.Акцепторные векторы обрабатывали Fse I и Asc I (акцепторный вектор E – H) или Xho I и Bam HI (целевой вектор II) и смешивали в эквимолярном соотношении. Комбинированные фрагменты, содержащие CDS, промоторы E . coli, маркерные гены селекции и расщепленные плазмиды смешивали в одной пробирке в соотношении, рекомендованном производителем для проведения реакции NEBuilder HiFi. Мы высевали трансформированные клетки на четыре различных агаровых среды LB, содержащих спектиномицин, ампициллин, хлорамфеникол или триклозан в качестве маркеров отбора для трансформированных плазмид.Таким образом, AtC4H :: L5 :: AtATR2 , PhCHI , HaCHS , At4CL-2 и AtPAL-2 были собраны в векторе назначения II, векторе приемника E – H, соответственно. Все части, их функции и источники приведены в дополнительных данных 5.
Комбинаторная экспрессия каждого отдельного гена путей
β-каротин и β-ионон: девять амплифицированных с помощью ПЦР фрагментов ATF / BS (праймеры X0_for и Z0_rev, ПЦР выполненные с векторами входа-девять ATF / BS) были смешаны (см. Дополнительные методы).Кодирующие последовательности McrtI , BTS1 , McrtYB и RiCCD1 и их последующие терминаторы и промоторы E . Гены маркеров селекции coli амплифицировали с помощью ПЦР из векторов Entry с использованием соответствующих пар праймеров (дополнительные методы). Четыре вектора были переварены : Целевой вектор I ( Sal I / Eco RI) и акцепторный вектор A – C ( Fse I / Asc I) и смешаны в эквимолярном соотношении.Объединенные фрагменты ATF / BS, фрагменты, содержащие CDS, и расщепленные плазмиды были смешаны в одной пробирке в соотношении, рекомендованном производителем для проведения реакции NEBuilder HiFi. Мы высевали трансформированные клетки на четыре различных агаризованной среды LB, содержащей спектиномицин, ампициллин, хлорамфеникол или триклозан в качестве маркеров отбора для трансформированных плазмид. Клетки, несущие успешно собранные конструкции, способны расти и образовывать колонии на соответствующей селективной среде.Следовательно, McrtI , BTS1 , McrtYB и RiCDD1 были собраны в целевом векторе I и акцепторном векторах A – C, соответственно. Кроме того, кодирующая последовательность GGPPSbc и ее нижний терминатор и промоторы селекционного маркера Amp R амплифицировали с помощью ПЦР из вектора входа X с использованием соответствующих пар праймеров и смешивали в эквимолярных количествах. Объединенные фрагменты ATF / BS, фрагмент, содержащий GGPPSbc CDS, и расщепленный Fse I / Asc I акцепторный вектор A были смешаны в одной пробирке в соотношении, рекомендованном производителем для выполнения NEBuilder HiFi. реакция.Мы высевали трансформированные клетки на агаровую среду LB, содержащую ампициллин, что позволяло клеткам, несущим успешно собранные конструкции, расти. Конститутивный дрожжевой промотор TDh4 32 использовали в качестве положительного контроля во всех экспериментах. ПЦР-амплифицированный Pro TDh4 (TDH_for / TDH_rev, on на геномной ДНК BY4741) клонировали в Fse I / Asc I-переваренный вектор входа X (дополнительные данные 6).
Комбинаторная экспрессия генов нарингенинового пути
Смешивали девять амплифицированных с помощью ПЦР фрагментов ATF / BS (см. Дополнительные методы).Кодирующие последовательности AtC4H: L5: AtATR2 , PhCHI , HaCHS , At4CL-2 и AtPAL-2 и их последующие терминаторы и промоторы E . Гены маркеров селекции coli амплифицировали с помощью ПЦР из целевого вектора II и акцепторного вектора E – H соответственно (дополнительные методы). Пять переваренных векторов, вектор назначения II ( Xho I / Bam HI) и акцепторные векторы E – H ( Fse I / Asc I), фрагменты ATF / BS и фрагменты, содержащие CDS биосинтеза нарингенина смешивали в одной пробирке в соотношении, рекомендованном производителем для проведения реакции NEBuilder HiFi.Мы высевали трансформированные клетки на пять различных агаровых сред LB, содержащих спектиномицин, ампициллин, хлорамфеникол, триклозан или гентамицин. Клетки с успешно собранными конструкциями способны расти на соответствующей селективной среде. Таким образом, AtC4H: L5: AtATR2 , PhCHI , HaCHS , At4CL-2 и AtPAL-2 были собраны в целевом векторе II и акцепторном векторах E – H, соответственно (дополнительные данные 5).
Комбинаторное клонирование генов пути
Равные количества девяти целевых векторов I – McrtI были смешаны и переварены с I — Ceu I / Sbf I.Равные количества девяти акцепторных векторов A-BTS1 были смешаны и использованы в качестве матрицы для амплификации фрагментов, содержащих промотор ауксотрофного маркера HIS3 , индуцируемый IPTG промотор, фрагменты ATF / BS, BTS1 CDS, TDh4 терминатор, промотор и CDS маркера селекции ампициллина с использованием соответствующих прямых (X0_for) и обратных (Z2_rev) праймеров. Следовательно, фрагменты, амплифицированные с помощью ПЦР, содержат девять различных модулей, различающихся по своим единицам ATF / BS (см. Дополнительные методы).Используя TAR, амплифицированные с помощью ПЦР фрагменты вставляли в девять векторов-адресатов I-McrtI для создания библиотеки из 9 2 = 81 векторов-адресатов I-McrtI-BTS1. Клетки дрожжей с успешными конструкциями растут на среде SC-Ura / -His. Плазмидную библиотеку выделяли из дрожжевых клеток, трансформировали в E . coli и выращивают на чашках с агаром LB, содержащем ампициллин, где будут расти только клетки, несущие правильные сборки. На следующем этапе библиотека плазмид была расщеплена с помощью Fse I / I — Sce I.Равные количества девяти акцепторных векторов B-McrtYB были смешаны и использованы в качестве матрицы для реакции ПЦР для амплификации фрагментов, содержащих промотор ауксотрофного маркера LEU2 , индуцируемый IPTG промотор, фрагменты ATF / BS, MctYB. CDS, дрожжевой синтетический терминатор 3, промотор и CDS маркера селекции хлорамфеникола с использованием соответствующих прямых (X0_for) и обратных (Z3_rev) праймеров. Таким образом, фрагменты, амплифицированные с помощью ПЦР, содержат девять различных модулей, различающихся по своим единицам ATF / BS.Используя TAR, ПЦР-амплифицированные модули McrtYB были вставлены в библиотеку линеаризованных векторов-адресатов I-McrtI-BTS1 для создания новой библиотеки из 9 3 = 729 векторов-адресатов I-McrtI-BTS1-McrtYB. Клетки дрожжей с успешными конструкциями растут на среде SC-Ura / -His / -Leu. Библиотека вектора назначения I, содержащая все три гена, приводит к продукции β-каротина в индуцирующих средах. Плазмидную библиотеку выделяли из дрожжевых клеток и трансформировали в E . coli , которую отбирали на агаровой среде LB, содержащей хлорамфеникол.Восстановленная библиотека впоследствии была использована для интеграции генов пути, включая регуляторные модули ATF / BS, в геном дрожжей (см. Ниже).
Плазмиды, продуцирующие наибольшее количество β-каротина в каждом фоновом штамме, IMX672.1 и Gen 0.1, впоследствии были использованы для производства β-ионона. Плазмиды расщепляли PI — Psp I. Равные количества девяти акцепторных векторов C — RiCCD1 смешивали и использовали в качестве матрицы для амплификации фрагментов, содержащих промотор ауксотрофного маркера TRP1 , IPTG- индуцибельный промотор, регуляторные единицы ATF / BS, RiCCD1 CDS, дрожжевой терминатор TEF1 , а также промотор и CDS маркера селекции триклозана с использованием соответствующих прямых (X0_for) и обратных (Z4_rev) праймеров.Таким образом, амплифицированные с помощью ПЦР фрагменты содержат девять различных модулей, различающихся своими регуляторными модулями ATF / BS. Используя TAR, амплифицированные с помощью ПЦР фрагменты вставляли в целевой вектор I-McrtI-BTS1-McrtYB. Дрожжевые клетки с правильно собранными конструкциями растут на среде SC-Ura / -His / -Leu / -Trp. Библиотека вектора-получателя I, содержащая все четыре гена, приводит к продукции β-ионона. Плазмидную библиотеку выделяли из дрожжевых клеток, трансформировали в E . coli и выращивали на агаровой среде LB, содержащей триклозан.Плазмиды pCAROTENE-PTDh4 и pIONONE-PTDh4 (см. Следующую главу) содержат CDS β-каротина и β-ионона под контролем промотора TDh4 , собранного в целевом векторе I.
Положительный контроль на β-каротин и β-ионон production
Целевой вектор I был расщеплен с помощью Eco RI / Sal I и использован в реакции двусторонней сборки с использованием ПЦР-амплифицированной последовательности Pro TDh4 (PROTDHMCRTI_for / PROTDHMCRTI_rev, на pCP11 32 ) и McrtI CDS слились с Ter FBA1 (MCRTIPOS_for / MCRTIPOS_rev, в векторе входа X-McrtI) для генерации pMCRTI_PTDh4. PciI / Cla I-переваренный pCP11 32 использовали в реакции сборки с использованием ПЦР-амплифицированной кодирующей последовательности HIS3 (PCPHIS_for / PCPHIS_rev, на pGN005B 4 ) для создания pCOMPASS32. Затем, pCOMPASS32, расщепленный Not I, использовали в реакции сборки с использованием BTS1 CDS (BTSPOS_for / BTSPOS_rev, в векторе входа X-BTS1) для генерации pBTS1_PTDh4. Pci I / Cla I-переваренный pCP11 32 использовали в реакции сборки с использованием ПЦР-амплифицированной кодирующей последовательности LEU2 (PCPLEU_for / PCPLEU_rev, на pGAD424, TAKARA Bio, GenBank # U07647) для создания pCOMPASS33.Затем pCOMPASS33, расщепленный Not I, использовали в реакции сборки с использованием McrtYB CDS (MCRTYBPOS_for / MCRTYBPOS_rev, в векторе входа X-McrtYB) для генерации pMCRTYB_PTDh4. Акцепторный вектор C был расщеплен с помощью Fse I / Asc I и использован в реакции двусторонней сборки с использованием ПЦР-амплифицированной последовательности Pro TDh4 (PROTDHRICCD_for / PROTDHRICCD_rev, на pCP11 32 ) и RiCCD1 CDS- Ter TEF2 — PI-Psp I- Pro TCSR (RICCDPOS_for / RICCDPOS_rev, в векторе входа X-RiCCD1) для создания pRIC4CD1_PTDh. I-Ceu I-переваренный pMCRTI_PTDh4 был использован в реакции сборки с использованием ПЦР-амплифицированного Pro TDh4 — BTS1 — Ter TDh4 (PTDh4_BTS1_for / PT1_revD) и кодирующая последовательность AmpR (AMPR_for / Y1_rev, на pGN003B 4 ). Полученная плазмида была названа pCOMPASS34. Затем, Fse I / I-Sce I-переваренный pCOMPASS33 был использован в реакции сборки с использованием ПЦР-амплифицированного Pro TDh4 — McrtYB (PTDh4_MCRTYB_for / PTDh4_MCRTYMCDh4) и на p-ptdh4_MCRTYMC_rev. Ter SYN3 -CmR – Ter CmR (CMR_for / Y2_rev, на pLD_3_4 32 ).Полученная плазмида была названа pCAROTENE-PTDh4. Затем PI-Psp I-переваренный pCOMPASS34 использовали в реакции сборки с использованием ПЦР-амплифицированного Pro TDh4 — RiCCD1 — Ter TEF2 -TCSR – Ter TCSR (PTDh4_RICCD1_for / Y3_rev, на pRICCD1_PTDh4.). Полученная плазмида была названа pIONONE-PTDh4.
Интеграция векторов-адресатов в геном дрожжей
Штаммы IMX672.1 или Gen 0.1 были трансформированы библиотекой Bam HI- или Not I-линеаризованных векторов назначения I, что привело к интеграции кассеты в дрожжевые локусы LYS2 или URA3 , соответственно, что привело к интеграции Гены β-каротинового или β-иононного пути.
Мультилокусная интеграция генов пути
Для одновременной интеграции генов, необходимых для β-каротина ( McrtI , BTS1 и McrtYB ) или β-ионона ( McrtI , BTS1 , McrtYB , и RiCCD1 ), штаммы Gen 0.1 и IMX672.1 котрансформировали с помощью 1 мкг плазмид sgRNA pTAJAK-92 45 и pCOM005 (для интеграции McrtI , McrtYB и BTS1 , а также в X-3, XI-3 , и локус XII-5 , соответственно) или pCOM006 (для интеграции модуля, содержащего RiCCD1 , в локус ura3-52 ), плюс 1 мкг каждого донорского фрагмента: McrtI (праймеры DES1-X3_for и DES1- X3_ rev в целевом векторе I-McrtI), BTS1 (праймеры ACCEPTA-XII5_for и ACCEPTA-XII5_rev в акцепторном векторе A-BTS1), McrtYB (праймеры ACCEPB-XI3_for и ACCEPTB-XI3_rev в векторе Acceptor) и RiCCD1 (праймеры ACCEPTC-ura_for и ACCEPTC-ura_rev на акцепторном векторе C-RiCCD1).Для отбора штаммов, продуцирующих β-каротин, клетки инокулировали в 1 мл жидкой культуральной среды в течение 3 дней с последующим посевом 1 мл 10 2 -разведенных клеток на среду, выбранную для присутствия плазмид sgRNA и Cas9 pTAJAK- 92 45 и pCOM005, которые несут гены маркеров селекции G418 и LYS2, соответственно. Колонии смывали с планшета, а затем клетки высевали на селективную среду (SC-Leu / -Ura / -His) для скрининга колоний, продуцирующих β-каротин, с интегрированными маркерами отбора.Для отбора штаммов β-иононного пути клетки высевали на SC-Lys для отбора на наличие плазмиды pCOM006. Колонии смывали и высевали на селективную среду для скрининга колоний, продуцирующих β-ионон, с интегрированными маркерами селекции. Когда появлялись колонии, планшеты для трансформации реплицировали на планшеты для неселективной индукции. Мультиплексная ПЦР выполнялась на отдельных колониях; праймеры амплифицировали регуляторные единицы ATF / BS перед каждой CDS.
Мультилокусная интеграция генов пути в штамме MXFde 0.2
Штамм MXFde 0.2 был котрансформирован с pCOM006 и 1 мкг донора RiCCD1 (праймеры ACCEPTC-ura_for и ACCEPTC-ura_rev на акцепторном векторе C-RiCCD1) для интеграции модуля, содержащего RiCCD1 ra3, в модуль ura2. сайт. Для отбора для успешной интеграции клетки высевали на SC-Lys / -Trp, так как маркер LYS2 кодируется на плазмиде, а маркер отбора TRP1 присутствует на интегрированном доноре. Когда появлялись колонии, планшеты для трансформации реплицировали на планшеты для неселективной индукции.Затем для интеграции пяти генов, необходимых для продукции нарингенина, библиотека красителей, продуцирующих β-ионон, была котрансформирована 1 мкг плазмиды sgRNA pCOM004 (для интеграции PhCHI и HaCHS в X-3 и XI-2. Локус соответственно), pCOM007 (для интеграции AtC4H :: L5 :: AtATR2 в XII-2 ), pCOM008 (для интеграции At4CL-2 и AtPAL-2 в X-2 и XI-5 локуса соответственно), плюс 1 мкг каждого донорского фрагмента: PhCHI (праймеры ACCPTE-X3_for и ACCPTE-X3_rev на акцепторном векторе E-CHI), HaCHS (праймеры ACCPTF-XI2_for и ACCPTF-XI2_rev на акцепторном векторе F-CHS), AtC4H :: AtATR2 (праймеры DESII-XII2_for и DESII-XII2_rev в целевом векторе II-C4H :: ATR2), At4CL-2 (праймеры ACCPTG-X2_for и ACCEPTG-X2_rev на Acceptor вектор G-4CL-2) и AtPAL-2 (праймеры ACCEPTH-XI5_for и ACCEPTH-XI5_rev на Акцепторный вектор H-PAL2).Клетки инокулировали в 1 мл жидкой культуральной среды в течение 3 дней с последующим посевом 1 мл 10 2 -разведенных клеток на среду, выбранную по присутствию плазмид sgRNA, которая кодирует маркер селекции LYS2 . Когда появлялись колонии, планшеты для трансформации реплицировали на планшеты для селекции (YPDA с пятью доминантными маркерами отбора) для (i) удаления эписомальных плазмид и (ii) скрининга на предмет успешно интегрированных генов в геном. Для одновременной интеграции трех CDS (в дополнение к RiCCD1), необходимых для продукции β-ионона в дрожжах, библиотеку штаммов нарингенина совместно трансформировали 1 мкг плазмиды pCOM005 с тройной sgRNA (для интеграции McrtI , McrtYB , и BTS1 или GGPPSbc в локусы X-4, XI-3 и XII-5 , соответственно), плюс 1 мкг донора McrtI , McrtYB и BTS1 фрагменты: McrtI (праймеры DES1-X4_for и DES1-X4_rev в целевом векторе I-McrtI), McrtYB (праймеры ACCEPB-XI3_for и ACCEPTB-XI3_rev в акцепторном векторе B-McrtYB) и BTSC1 (праймеры ACCEP1 ). XII5_for и ACCEPTA-XII5_rev на акцепторном векторе A-BTS1).Кроме того, мы использовали донор GGPPSbc (праймеры ACCEPTA-XII5_for и ACCEPTA-XII5_rev на акцепторном векторе A-GGPPSbc) в дополнение к донору BTS1 . Клетки инокулировали в 1 мл жидкой культуральной среды в течение 3 дней с последующим посевом 1 мл 10 2 -разведенных клеток на среду, выбранную для присутствия плазмид sgRNA. Впоследствии, когда появлялись колонии, культуры планшетов для трансформации реплицировали на планшеты для неселективной индукции. Когда появлялись колонии, их соскребали с планшетов и использовали для создания культур в жидкой среде, тем самым создавая библиотеку изолятов (называемых нарионами), продуцирующих β-ионон и нарингенин на разных уровнях.
Извлечение плазмид из дрожжей
Собранные конструкции, кодирующие пути β-каротина и β-ионона, были выделены из дрожжей с использованием протокола выделения высококачественной кольцевой плазмидной ДНК в количествах микрограммов 27 . Вкратце, дрожжевые клетки, несущие плазмиды, выращивали в 10 мл селективной среды в течение ночи при 30 ° C, затем инокулировали в 400 мл селективной среды и снова выращивали в течение ночи при 30 ° C. При OD 600 1,5 клетки собирали центрифугированием и ресуспендировали в 100 мл дистиллированной воды, переносили в две 50-мл пробирки Falcon и собирали центрифугированием.Клетки лизировали с использованием раствора SPE (1 M сорбит, 0,01 M фосфат натрия, 0,01 M Na 2 EDTA, pH 7,5), зимолиаза 20T (10 мг / мл -1 в 25% (мас. / Об.) Глицерине), β -меркаптоэтанол, буфер для лизиса (0,05 M трис-HCl, 0,02 M EDTA, 1% SDS, pH 12,8) и фенол: хлороформ: изоамиловый спирт. ДНК осаждали с использованием ацетата натрия и изопропанола, а плазмидную ДНК экстрагировали с использованием набора Qiagen Large-Construct (Qiagen). Выделенные плазмиды трансформировали в клетки E. coli и высевали на планшеты LB с соответствующими клетками E .Маркеры селекции coli .
Интеграция девяти модулей ATF / BS-yEGFP в локус
XII-5Девять акцепторных векторов A-ATF / BS-BTS1 (дополнительный рисунок 11 и дополнительные данные 6) расщепляли с помощью I, — Ceu I, чтобы удалить фрагмент BTS1-Ter TDh4 . I, — Ceu, I-переваренный фрагмент yEGFP-Ter CYC1 (праймеры YEGFP_for и YEGFP_rev на pGN005B 4 ) собирали в каждом из девяти линеаризованных остовов для создания девяти акцепторных векторов (A- yEGFP1 – A-yEGFP9).Девять акцепторных векторов идентифицировали с помощью ПЦР с использованием праймеров YEGFP2-for и YEGFP2-rev с последующим секвенированием. Более того, фрагменты, содержащие TDh4 промотор –yEGFP – TDh4 терминатор (праймеры PTDH_for и TTDHX_rev на плазмиде pCP11 32 ) и промоторы Amp R генов маркеров селекции (AMPR_ Afor / Z1_rev, на акцепторном векторе) -yEGFP1) были клонированы в расщепленный Asc I / Fse I акцепторный вектор A. Полученная плазмида была названа акцепторным вектором A-yEGFP0.
Затем по 1 мкг каждого донорного фрагмента yEGFP (праймеры ACCEPTA-XII5_for и ACCEPTA-XII5_rev на десяти акцепторных векторах A-yEGFP0 – A-yEGFP9) вместе с McrtI (праймеры DES1-X3_for и DES1-X rev, на целевом векторе I-McrtI) и McrtYB (праймеры ACCEPB-XI3_for и ACCEPTB-XI3_rev, на акцепторном векторе B-McrtYB) доноров и 1 мкг плазмид тройной sgRNA pTAJAK-92 45 и pCOM005 (для интеграции McrtI , McrtYB , yEGFP в сайты X-3 (, XI-3 и XII-5 соответственно) трансформировали в штамм дрожжей IMX672.1. Клетки высевали на среду для отбора плазмид sgRNA. Колонии смывали с планшетов, а затем клетки помещали на селективную среду (SC-Leu / -Ura / -His) для скрининга успешной интеграции доноров с интегрированными маркерами селекции. Впоследствии, когда появлялись колонии, планшеты для трансформации реплицировали на планшеты для неселективной индукции YPDA. ПЦР проводили на отдельных колониях; праймеры были разработаны для амплификации регуляторных единиц ATF / BS перед каждой CDS.
Конструирование штаммов AGREEN, BRED и AB-GREEN-RED
Акцепторный вектор A-NLS-JUB1-EDLLAD-EDLLAD-4 × -BTS1 и акцепторный вектор B-NLS-JUB1-EDLLAD-EDLLAD-4 × -McrtYB (Дополнительный рисунок 11 и Дополнительные данные 6) были обработаны с помощью I — Ceu I и I-Sce I, чтобы удалить BTS1-Ter TDh4 и McrtYB-Ter SYN3 фрагмент соответственно. I, — Ceu, I-расщепленный фрагмент AcGFP1-Ter TEF2 (праймеры ACGFP1_for и ACGFP1_rev, на плазмиде pGREEN) и I-Sce I-расщепленный DsRED-Ter 2 DsRED-Ter 2 Фрагмент (праймеры DSRED_for и DSRED_rev, на плазмиде pRED) вставляли в линеаризованный акцепторный вектор A и B для создания плазмид AVA-GREEN и AVB-RED соответственно.AVA-GREEN и AVB-RED были идентифицированы с помощью ПЦР с использованием праймеров ACGFP2-for и ACGFP2-rev и DSRED1-for и DSRED1-rev, соответственно, с последующим секвенированием. Затем доноры AcGFP1 (праймеры ACCEPTAGFP-XII5_for и ACCEPTA-XII5_rev, на AVA-GREEN) и DsRED (праймеры ACCEPB-XI3_for и ACCEPTB-XI3_rev, амплифицированы на AVB-RED). Один мкг sgRNA плазмиды pCOM005 (для интеграции доноров AcGFP1 и DsRED в локус XII-5 и XI-3 соответственно) вместе с (i) AcGFP1 , (ii) DsRED или (iii) Доноры AcGFP1 и DsRED трансформировали в штамм дрожжей IMX672.1. Клетки высевали на среду для отбора плазмиды sgRNA, которая несет маркерный ген LYS2 . Затем смытые колонии высевали на селективную среду (SC-Leu / -His). Когда появлялись колонии, планшеты для трансформации реплицировали на планшеты для неселективной индукции YPDA. ПЦР выполняли на отдельных колониях с использованием праймеров, амплифицирующих регуляторные единицы ATF / BS перед каждой CDS.
Создание штаммов для измерения скорости роста
Для создания конструкций, подходящих для экспрессии зеленого флуоресцентного белка (GFP) и красного флуоресцентного белка (RFP), мы вставили фрагмент ДНК, содержащий ген LYS2 (праймеры LYS_for / LYS_rev; на pYC6Lys -TRP1URA3; Addgene # 11010), дрожжевой промотор TEF2 (праймеры PTEF2_for / PTEF2_rev; геномная ДНК BY4741), AcGFP1 ( Aequorea coerulescens GFP, праймеры ACGFP_for / ACGFP_rev; DGFP_for / ACGFP_rev1; плазмида 54DFP1-AcGFP_rev); ( Discosoma sp .Запрос предложений, праймеры DSRED_for / DSRED_rev; плазмида MSCV-CMV-DsRed-IRES-d24EGFP; Addgene # 41944) и терминатор TEF2 (праймеры TTEF2_for / TTEF2_rev; геномная ДНК BY4741) в расщепленную плазмиду Xba I / Pst I pL1D_hc 32 . Полученные плазмиды, названные pGREEN и pRED, были расщеплены с помощью Xho I. Расщепленный pGREEN был затем интегрирован в сайт lys2.a штаммов Gen 0.1 и IMX672.1, тогда как расщепленный pRED был интегрирован в lys2.сайт штаммов Gen 0.1, IMX672.1, PCB, CB1, MXintpDI 1 и RC1. Штаммы-репортеры флуоресцентного белка были названы Green-Gen 0.1, Green-IMX672.1 и Red-Gen 0.1, Red-IMX672.1, Red-PCB, Red-CB1, Red-MXintpDI 1 и Red-RC1 соответственно ( Дополнительные данные 7). Одну колонию штаммов, меченных AcGFP1 и DsRED, предварительно инокулировали в 4 мл неиндуцирующей среды SC с соответствующими маркерами селекции дрожжей в течение 18 ч при 30 ° C во роторном шейкере при 230 об / мин. Субкультуры выращивали в неиндуцирующей (2% (мас. / Об.) Глюкозе) или индуцирующей (2% (мас. / Об.) Галактозе, 20 мкМ IPTG) среде YPDA.Эксперименты по конкуренции роста в отдельных сосудах готовили путем смешивания (i) клеток, меченных DsRED, когда ATF не экспрессируется (неиндуцирующая среда), и соответствующих клеток, меченных AcGFP1; (ii) DsRED-меченные клетки, когда ATF экспрессируется (индуцирующая среда), и соответствующие AcGFP1-меченные клетки. Мы инокулировали сокультуры в соотношении 8: 2 (клетки, меченные DsRED: клетки, меченные AcGFP1) при OD 600 ~ 0,1 в 4 мл среды YPDA. Клетки выращивали в течение 48 ч на роторном шейкере при 30 ° C и 230 об / мин.В моменты времени 6, 24 и 48 часов отбирали образцы для измерения OD 600 и анализа проточной цитометрией для определения соотношения DsRED-положительных и AcGFP1-положительных клеток. В каждый момент времени клетки разводили в 100 раз свежей жидкой средой для роста до следующего момента времени. Мы подсчитывали клетки, меченные DsRED и AcGFP1.
Индукционные эксперименты
Штаммы дрожжей, несущие гены пути, высевали на неиндуцирующую среду SC (2% (мас. / Об.) Глюкозы) с соответствующими маркерами отбора.Клетки выращивали при 30 ° C в течение 3-4 дней. Планшеты соскребали для сбора клеток, которые затем высевали на планшеты со средой для индукции SC, содержащей 20 мМ изопропил-β-D-тиогалактопиранозид (IPTG), 2% (мас. / Об.) Галактозы, 1% (мас. / Об.) Рафинозы и подходящие маркеры селекции (индуцирующая и селективная среда) для эписомальной экспрессии и индукция планшетов со средой YPDA (20 мМ IPTG, 2% (мас. / об.) галактозы) в случае экспрессии на основе интеграции генома. Клетки выращивали при 30 ° C в течение 3-4 дней. Эпизомальные плазмиды выделяли из собранных колоний, трансформировали в E . coli и собранные части были секвенированы. В случае кассет, интегрированных в геном, проводили ПЦР колоний с последующим секвенированием. Для анализа продукта (β-каротин или β-ионон) методом ВЭЖХ были выбраны три независимые колонии либо из интегрированных, либо из эписомальных конструкций, введенных в фоны Gen 0.1 или IMX672. С этой целью колонии отбирали на основе интенсивного оранжевого цвета, указывающего на высокий уровень β-каротина, или светло-оранжевого цвета, указывающего на накопление β-ионона.Положительные контроли экспрессировали гены пути под контролем конститутивного промотора дрожжей TDh4 .
Высокоэффективная жидкостная хроматография
Отдельные колонии дрожжевых штаммов высевали в 4 мл неиндуцирующей среды SC с соответствующим селективным маркером (предварительная культура) и выращивали в течение 18–24 ч при 30 ° C на роторном шейкере при 230 об / мин. . Затем прекультуры использовали для инокуляции субкультур (50 мл), индуцирующей среду SC (20 мМ IPTG, 2% галактозы, 1% (мас. / Об.) Рафинозы) с соответствующим маркером селекции.Все культуры в колбах инокулировали из прекультур, выращенных на той же среде, до исходной OD 600 0,1. Клетки выращивали в колбе на 500 мл при 30 ° C в течение 3 дней на роторном шейкере при 230 об / мин до насыщения, а затем собирали для анализа метаболитов с помощью ВЭЖХ. Экстракцию каротиноидов проводили из клеточных гранул в соответствии с методом экстракции ацетоном 16 со следующими некоторыми изменениями. Осадок клеток один раз промывали деионизированной водой. Стеклянные шарики (диаметр 400–600 мкм; Sigma Chemical Co.) и 500 мкл ацетона добавляли к осадку клеток в 2,0-мл микроцентрифужной пробирке ( Eppendorf ) и встряхивали для измельчения клеток с последующей инкубацией в течение 20 минут при 30 ° C. После разрушения смесь гранул-клеток центрифугировали в настольной микроцентрифуге при 16,300 × g в течение 5 минут при 4 ° C, и супернатант ацетона собирали в стандартные 2,0-мл микроцентрифужные пробирки (Eppendorf). Эту процедуру экстракции повторяли до тех пор, пока осадок клеток не стал белым.Для образцов β-каротина объединенные ацетоновые экстракты переносили в стеклянный флакон и сушили с использованием пылесоса speed-vac . Чтобы предотвратить разложение каротиноидов под действием света, стеклянные флаконы держали внутри черных 1,5-мл микроцентрифужных пробирок (Eppendorf). Для определения β-ионона половину объединенного ацетонового экстракта сушили для количественного определения β-каротина, как описано выше. Другая половина находилась внутри фармакостекла и использовалась для измерения β-ионона.Все операции проводились при зеленом неярком свете, чтобы избежать разложения каротиноидов. Образцы хранили при -80 ° C до дальнейшего использования. Экстракты получали из клеток, выращенных в трех независимых экспериментах, и анализы ВЭЖХ выполнялись AppliChrom (Ораниенбург, Германия). Перед измерением сухие образцы растворяли в ацетоне. Каротиноиды разделяли с помощью ВЭЖХ с использованием фазовой RP-HPLC колонки AppliChrom OTU DiViDo (250 × 4,6 мм) с пористыми частицами 5 мкм (85/10/5, ацетон / метанол / изопропанол, об. / Об. / Об.) В качестве подвижной фазы. , с 1.Поток 0 мл / мин. Профили элюирования регистрировали с помощью детекторов Shimadzu 450 нм (D2) и Kontron 300 нм (D2).
Количественное определение β-каротина на основе поглощения
Используя метод, описанный Lian et al. 21 , штаммы, продуцирующие β-каротин, предварительно культивировали в среде SC с соответствующими маркерами селекции в течение приблизительно 2 дней, инокулировали в 5 мл обоих штаммов, индуцируя (2% (мас. / Об.) Галактозу, 20 мкМ IPTG, 1% ( (мас. / об.) рафинозы) и неиндуцирующей (2% (мас. / об.) глюкозы) среды SC с исходной OD 600 , равной 0.1 в 15-миллилитровые культуральные пробирки и культивировали (30 ° C, 250 об / мин) еще 5 дней. Клетки дрожжей в стационарной фазе собирали центрифугированием при 13000 × g в течение 1 мин, а осадки клеток ресуспендировали в 1 мл 3 н. HCl, кипятили в течение 5 мин и охлаждали на ледяной бане в течение 5 мин. Лизированные клетки промывали ddH 2 O и ресуспендировали в 400 мкл ацетона для экстракции β-каротина. Остатки клеток удаляли центрифугированием. Стадия экстракции повторялась до тех пор, пока осадок клеток не становился белым.Супернатант, содержащий β-каротин, анализировали на его оптическую плотность при 454 нм. Продукция β-каротина была приведена к плотности клеток.
Проточно-цитометрический анализ клеток, продуцирующих нарингенин
Для количественной оценки выхода флуоресценции yEGFP в отсутствие ATF растительного происхождения отдельные колонии репортерных штаммов на основе FdeR инокулировали в 500 мкл неиндуцирующей среды SC с соответствующими маркерами селекции в 48-луночном поле. планшеты с глубокими лунками. Планшеты инкубировали в течение 24 ч при 30 ° C и 230 об / мин на роторном шейкере.Предварительные культуры использовали для инокуляции субкультур в 500 мкл индуцирующей среды YPDA до OD 600 ~ 0,1. Клетки выращивали в течение 16 ч на роторном шейкере при 30 ° C и 230 об / мин. Продукция белка подавлялась добавлением 500 мкг / мл циклогексимида. После этого выход флуоресценции каждой клетки анализировали с помощью проточного цитометра BD FACSCalibur (BD Biosciences). Значения флуоресценции yEGFP рассчитывали как минимум для 10 000 клеток в каждом образце. Среднее геометрическое значение флуоресценции yEGFP на клетку рассчитывали с использованием программного обеспечения Flowing версии 2.5.1 (http://www.uskonaskel.fi/flowingsoftware).
Краткое изложение отчета
Дополнительная информация о дизайне исследования доступна в Резюме отчета по исследованию природы, связанном с этой статьей.
подростков — Золотой компас — Публичная библиотека округа Эри
Подростки — Золотой компас — Публичная библиотека округа Эри — OverDriveПубличная библиотека округа Эри
Подростки
×Вам могут быть доступны другие названия.Войдите, чтобы увидеть полную коллекцию.
ЕГО ТЕМНЫЕ МАТЕРИАЛЫ СКОРО БУДЕТ ОРИГИНАЛЬНОЙ СЕРИИ HBO С ДАФН КИНОМ, РУТОМ УИЛСОНОМ, ДЖЕЙМСОМ МАКАВОЙ И ЛИН-МАНУЭЛ МИРАНДА!Современная классика фэнтези, которую журнал Entertainment Weekly назвал «величайшим романом всех времен», а журнал Newsweek назвал «100 лучших книг всех времен».»Филип Пуллман переносит читателей в мир, где у людей есть друзья-животные и где параллельные вселенные находятся в пределах досягаемости.
Лира устремляется на холодный, дальний север, где правят кланы ведьм и бронированные медведи. украсть — включая ее друга Роджера. Север, где ее грозный дядя Азриэль пытается построить мост в параллельный мир.
Может ли одна маленькая девочка изменить ситуацию в таких великих и ужасных усилиях? Это Lyra : дикарь, интриган, лжец и столь же свирепый и верный чемпион, какого только могли пожелать Роджер или Азриэль.
Но чего Лира не знает, так это того, что помочь одному из них — значит предать другого …
Шедевр повествования и интриги, отмеченный наградами фильм Филипа Пулмана «Золотой компас» — первый в его «Темных материалах». серия, которая продолжается с The Subtle Knife и The Amber Spyglass.
A # 1 New York Times Бестселлер
Обладатель премии Guardian за детскую фантастику
Опубликовано в 40 странах
«Возможно, лучший детский фэнтезийный роман за последние двадцать лет. — The Washington Post
«Действительно грандиозно». — The New York Times
«Пуллман, возможно, гений». — Newsweek
- Детали
Издатель:
Детские книги Random HouseНаграды:
Kindle Book
Дата выпуска: 13 ноября 2001 г.OverDrive Read
ISBN: 9780440418603
Дата выпуска: 13 ноября 2001 г.EPUB ebook
ISBN: 9780440418603
Размер файла: 42979 КБ
Дата выпуска: 13 ноября 2001 г. - Создатели
- Форматы
Разжечь книгу
OverDrive Читать
Электронная книга в формате EPUB - Языки
- Уровни
Уровень ATOS: 7.1
Lexile® Measure: 930
Уровень интереса: 9-12 (UG)
Сложность текста: 4-6 - Отзывы
Загрузка
Доступность может меняться в течение месяца в зависимости от бюджета библиотеки.Вы по-прежнему можете удерживать титул, и он будет автоматически заполнен, как только титул снова станет доступен.
Формат OverDrive Read этой электронной книги имеет профессиональное повествование, которое воспроизводится, пока вы читаете в браузере. Узнайте больше здесь.
Закрывать
Вы достигли максимального количества наименований, которые в настоящее время можете рекомендовать для покупки.
Ok
Время сеанса истекло. Пожалуйста, войдите в систему еще раз, чтобы вы могли продолжать заимствовать заголовки и получать доступ к страницам «Ссуды», «Список желаний» и «Удержания».
Если проблема не исчезла, выполните следующие действия, чтобы войти в систему.
Добавьте библиотечную карточку в свою учетную запись, чтобы брать книги, размещать удержания и добавлять книги в свой список желаний.
Есть карта? Добавьте его сейчас, чтобы начать заимствовать из коллекции.
Библиотечную карточку, которую вы добавили ранее, нельзя использовать для выполнения этого действия.Пожалуйста, добавьте свою карту еще раз или добавьте другую карту. Если вы получили сообщение об ошибке, обратитесь за помощью в свою библиотеку.
| AAPG Datapages Цифровые публикации через Фонд Американской ассоциации геологов-нефтяников | |
| Коллекция Аарона Копленда Коллекция Аарона Копленда, ок.1900–1990, Библиотека Конгресса, представляет подборку оцифрованных материалов из полной коллекции Аарона Копленда. Материалы включают музыкальные зарисовки, переписку, письма и фотографии. | |
| Коллекция ABI / INFORM ABI / INFORM Коллекция указателей и рефератов статей, охватывающих все аспекты бизнеса во всем мире. Полная статья представлена во многих заголовках. Коллекция объединяет ресурсы, представленные в ABI / INFORM Global (бизнес-информация по всему миру), ABI / INFORM Trade & Industry и ABI / INFORM Dateline (локальная и региональная бизнес-информация).Ранее известный как ABI / INFORM Complete. | |
| ABI / INFORM Dateline Бизнес, экономика: местные и региональные деловые издания. Освещение местных и региональных деловых новостей о крупных корпорациях, частных компаниях, местных стартапах, профили руководителей, новости маркетинга, финансов и отрасли. Содержит новости и аналитику, информацию о местных рынках и многое другое, полученное из основных деловых таблоидов, журналов, ежедневных газет, информационных агентств, а также деловых изданий городов, штатов и регионов. | |
| ABI / INFORM Global Бизнес, финансы, экономика: журналы, профили компаний, Wall Street Journal. Освещение тем бизнес-исследований, деловых и экономических условий, методов управления, теории и практики бизнеса, рекламы, маркетинга, экономики, человеческих ресурсов, финансов, налогообложения, компьютеров. Также содержит бизнес-профили и профили руководителей. | |
| ABI / INFORM Торговля и промышленность Бизнес, экономика: торгово-промышленные периодические и информационные бюллетени.Деловые периодические издания и информационные бюллетени с коммерческой или отраслевой направленностью. Освещение отраслевых новостей, информации о продуктах и конкурентах, а также маркетинговых тенденций. Содержит публикации по основным отраслям экономики, включая финансы, страхование, транспорт и строительство. | |
| Academic OneFile Gale Academic OneFile предоставляет учащимся доступ к информации, которую они ищут, с помощью инструментов, которые позволяют быстро и легко находить информацию.Это главное периодическое издание содержит миллионы статей из научных журналов и других авторитетных источников с обширным освещением в ключевых предметных областях, таких как биология, химия, уголовное правосудие, экономика, экология, история, маркетинг, политология и психология. Включает полнотекстовое освещение New York Times с 1995 года. | |
| Academic Search Premier Academic Search Premier — это многопрофильная полнотекстовая база данных, содержащая полные тексты почти 4500 журналов, включая более 3600 названий, прошедших рецензирование. | |
| Академическое видео онлайн AVON — это платформа для потокового видео, предоставляющая более 68 000 наименований, охватывающих широкий спектр предметных областей, включая антропологию, бизнес, историю, музыку и многое другое. | |
| Access Medicine Интернет-магазин «Включите Харрисона» и «Фармакология Гудмана и Гилмана».AccessMedicine.com компании McGraw-Hill — это инновационный онлайн-ресурс, который предоставляет студентам, ординаторам, клиницистам и исследователям мгновенные ответы на клинические вопросы из самых надежных источников. Access Medicine, обновляемая ежедневно и постоянно расширяющаяся, предназначена для прямого доступа к информации, необходимой для выполнения оценок, постановки диагноза, принятия решений по ведению пациентов, проведения исследований, медицинского образования или самооценки и проверки советом директоров. | |
| Доступ к мировым новостям Предоставляет полнотекстовую информацию и перспективы более чем 1400 единиц измерения.С. и более 1200 международных источников. Каждый источник имеет свою особую направленность, предлагая различные точки зрения на местные, региональные и мировые проблемы. | |
| AccessScience Статьи и обзоры исследований, охватывающих все основные научные дисциплины и включающих Энциклопедию науки и технологий МакГроу-Хилла и Ежегодник науки и техники МакГроу-Хилла, а также определения из Словаря научных и технических терминов МакГроу-Хилла. | |
| Цифровая библиотека ACM Полнотекстовый доступ к различным журналам и материалам конференций, опубликованным Association for Computing Machinery. Примечание. Подписка на библиотеку Richter не включает полнотекстовый доступ к статьям информационного бюллетеня ACM Proceeding и SIG. | |
| Веб-версии ACS Предоставляет доступ ко всей библиотеке полнотекстовых журналов ACS.Архивы ACS Journal позволяют получить доступ к 120-летним исследованиям в области химии. В онлайн-архивах выполняется поиск по полному тексту всех названий, опубликованных ACS с 1879 года по сегодняшний день, обеспечивая бесшовную интеграцию между архивами и веб-изданиями. ACS позволяет электронную доставку статей в формате PDF с полной интеграцией с исходным документом. | |
| Ad * Доступ Ad * Access представляет изображения и информацию из базы данных для более 7000 рекламных объявлений, напечатанных в США.S. и канадские газеты и журналы, охватывающие пять категорий товаров — красота и гигиена, радио, телевидение, транспорт и пропаганда Второй мировой войны — датированы периодом с 1911 по 1955 год. | |
| Adforum Посмотрите примеры реальной рекламы из всех форм СМИ, включая печать и видео, со всего мира. Большинство из них — лауреаты премий. | |
| Передовые технологии и аэрокосмическая промышленность (ProQuest) База данных Advanced Technologies & Aerospace Database включает в себя известную базу данных Aerospace Database и предоставляет полнотекстовые названия со всего мира, включая научные журналы, отраслевые и отраслевые журналы, журналы, технические отчеты, материалы конференций, правительственные публикации.Также включает материалы из рефератов по компьютерным и информационным системам, рефератов по электронике и коммуникациям и рефератов по твердым телам и сверхпроводимости. | |
| Электронная библиотека AES Содержит все документы Общества инженеров аудио из журналов, съездов и конференций, обеспечивая доступ к более чем 16 000 файлов PDF с возможностью поиска, документирующих прогресс исследований звука с 1953 года до наших дней., Включает препринты AES Publications Convention Своевременные технические документы, воспроизводимые непосредственно из рукописей презентаций, сделанных на недавних конвенциях AES. Антологии Известная серия сборников документов архивного качества, перепечатанная из журнала AES Journal, в том числе: громкоговорители, запись на диск, микрофоны, звукоусиление и спектрометрия с временной задержкой. Сборник статей с престижных международных конференций AES, каждая из которых посвящена определенной теме. Стандарты, проекты и информационные документы AES Утвержденные на международном уровне документы, разработанные под эгидой Комитета по стандартам AES и его рабочих групп.Справочник образовательных программ Исчерпывающий международный справочник по образовательным программам в аудио. | |
| Каталог AFI Каталог AFI — национальная фильмография, документирующая историю американского кино. В настоящее время каталогизация охватывает 1892–1973 годы всесторонне, с дополнительными записями, охватывающими избранные основные фильмы, начиная с 1975 года. | |
| Афро-американские газеты, серия 1 African American Newspapers, Series 1 предоставляет онлайн-доступ примерно к 280 U.Газеты S., рассказывающие о полутора веках жизни афроамериканцев. В этой коллекции представлены документы из более чем 35 штатов, в том числе множество редких и исторически значимых изданий XIX века. | |
| Афроамериканские газеты: XIX век Афро-американские газеты: XIX век содержат сообщения из первых рук о культурной жизни и истории афроамериканцев в Соединенных Штатах. | |
| Центр афроамериканских исследований Оксфордский центр афроамериканских исследований, в котором собрано более 20 000 статей ведущих ученых в этой области, представляет собой обширную коллекцию стипендий, посвященных жизням и событиям, которые сформировали афроамериканскую и африканскую историю и культуру. | |
| Афро-американский оркестр, музыка и записи, 1883-1923 гг. Коллекция афро-американских групп, музыка и записи, 1883–1923 гг. В Библиотеке Конгресса содержит стандартные аранжировки популярных песен, написанных афроамериканцами, а также небольшую подборку исторических звукозаписей с этими и подобными песнями. | |
| Афро-американские ноты Афро-американские ноты — это постоянно растущая цифровая коллекция материалов, отобранных из Сборника нот Библиотеки Джона Хейла Университета Брауна. Произведения в коллекции датируются 1820-ми годами по настоящее время. | |
| АГРИКОЛА Указатель международных журналов, диссертаций, патентов, компьютерного программного обеспечения и технических отчетов Национальной сельскохозяйственной библиотеки по сельскому хозяйству и смежным областям.Эта база данных включает, но не ограничивается ресурсами, доступными в NAL, и содержит более 5 200 000 записей, включая печатные работы, относящиеся к 15 веку. | |
| Сельское хозяйство и экология Междисциплинарная база данных, которая индексирует и обобщает мировую исследовательскую литературу в области сельскохозяйственных наук и наук об окружающей среде, обеспечивая всесторонний охват с 1967 года по настоящее время. Включает известные AGRICOLA, Экологические науки и управление загрязнением (ESPM) и Заявления о воздействии на окружающую среду (EIS) и предоставляет полнотекстовые заголовки со всего мира, включая научные журналы, отраслевые и отраслевые журналы, журналы, технические отчеты, материалы конференций , правительственные публикации и многое другое. | |
| Публикации AIP (AIP Scitation) Ведущие журналы и материалы конференций издательства AIP и обществ-членов AIP. | |
| Александровская улица Alexander Street предоставляет онлайн-платформу для специализированных коллекций первичных источников, веб-сайтов и потокового мультимедиа, предназначенную для обучения и исследований в самых разных областях. В настоящее время доступный контент включает более 900 000 альбомов, 2600 видео и почти 47 000 текстовых документов. | |
| Александр Стрит Видео Alexander Street Video позволяет пользователям выполнять перекрестный поиск по всем видео, опубликованным Alexander Street Press.В настоящее время доступно более 2600 видеороликов в самых разных областях, от мировой истории до кулинарии. | |
| Амвросий Видео Ambrose Video обеспечивает потоковую передачу образовательного контента по различным дисциплинам. В настоящее время Университет Майами имеет доступ к более чем 30 видео из коллекции BBC Shakespeare Play и всей серии «Долгих поисков», в которой обсуждаются основные верования основных мировых религий. | |
| Отпечатки истории Америки Содержит монографии, брошюры, плакаты, правительственные документы и однодневки. Доступно здесь: Гражданская война Broadsides и Ephemera; Ранние американские оттиски, серия I: Эванс, 1639-1800; Ранние американские оттиски, серия II: Шоу-Шумейкер, 1801-1819. | |
| Америка: история и жизнь Америка: история и жизнь рефераты и указатели журналов и диссертаций по истории Соединенных Штатов и Канады. | |
| Коллекция исторических периодических изданий Американского антикварного общества (AAS): серии 1-5 Коллекция исторических периодических изданий Американского антикварного общества (AAS) включает оцифрованные изображения страниц американских журналов и журналов Американского антикварного общества, главной библиотеки, документирующей жизнь людей Америки от колониальной эры до гражданской войны и реконструкции .Эта коллекция существует в виде серии из пяти баз данных, которые включают 6500 наименований, содержащих более 10 миллионов страниц контента, опубликованного в период с 1691 по 1876 год. | |
| Веб-издания Американского химического общества Предоставляет доступ ко всей библиотеке полнотекстовых журналов ACS. Архивы ACS Journal позволяют получить доступ к 120-летним исследованиям в области химии. В онлайн-архивах выполняется поиск по полному тексту всех названий, опубликованных ACS с 1879 года по сегодняшний день, обеспечивая бесшовную интеграцию между архивами и веб-изданиями.ACS позволяет электронную доставку статей в формате PDF с полной интеграцией с исходным документом. | |
| Американская хоровая музыка «Американская хоровая музыка», созданная в результате сотрудничества Библиотеки Конгресса и Ассоциации хоровых директоров, представляет подборку значимых хоровых произведений ведущих американских композиторов с 1860-х по 1922 год, находящихся в открытом доступе. | |
| Американская фантастика 1774-1920 Этот сборник содержит более 17 800 наименований прозы, написанной американцами с колониальных времен до начала двадцатого века, собирая обширный архив содержания в одном месте и единообразном формате, который позволяет исследовать произведения в контексте истории . | |
| Каталог Американского института кино Каталог AFI — национальная фильмография, документирующая историю американского кино. В настоящее время каталогизация охватывает 1892–1973 годы всесторонне, с дополнительными записями, охватывающими избранные основные фильмы, начиная с 1975 года. | |
| Американское рыболовное общество Американское рыболовное общество издает набор журналов для специалистов по водным ресурсам. | |
| Американская история и культура в Интернете: Сабин Американа, 1500-1926 гг. Этот сборник, основанный на знаменитой библиографии Джозефа Сабина, содержит работы об Америке, опубликованные во всем мире с 1500 до начала 1900-х годов. Включены книги, брошюры, сериалы и другие документы, содержащие оригинальные отчеты об исследованиях, торговле, колониализме, рабстве и отмене рабства, западном движении, коренных американцах, военных действиях и многом другом.Эта коллекция, насчитывающая более 6 миллионов страниц из 29 000 работ, является краеугольным камнем в изучении западного полушария. | |
| Переписка американских индейцев: Пресвитерианское историческое общество, собрание писем миссионеров, 1833-1893 гг. Переписка американских индейцев: Пресвитерианское историческое общество, собрание миссионерских писем, 1833–1893 гг., Представляет собой собрание писем в и от Совета по иностранным миссиям пресвитерианской церкви в Соединенных Штатах Америки.В их письмах описываются коренные народы и культуры, племенная фракционность, отношения с правительством США, а также многие проблемы и достижения их работы. | |
| Движение американских индейцев и радикализм коренных американцев Движение американских индейцев и радикализм коренных американцев включает документацию ФБР об эволюции AIM как организации социального протеста, а также ценную документацию по противостоянию с Вундед-Ни в 1973 году.Отчеты информаторов и материалы, собранные отделом экстремистской разведки ФБР, дают представление о мотивах, действиях и лидерстве ДАИ, а также о развитии радикализма коренных американцев. | |
| Публикации Американского института физики (AIP Scitation) Ведущие журналы и материалы конференций издательства AIP и обществ-членов AIP. | |
| Публикации Американского математического общества Полнотекстовый доступ к различным журналам и журналам, издаваемым Американским математическим обществом. | |
| Журналы Американской медицинской ассоциации Предоставляет доступ к полному тексту журналов, опубликованных Американской медицинской ассоциацией. | |
| Американская память: исторические коллекции для Национальной цифровой библиотеки Проект американской памяти Национальной цифровой библиотеки Библиотеки Конгресса оцифровывает уникальные исторические фонды Америки, хранящиеся в Библиотеке Конгресса, включая фотографии, полнотекстовые рукописи и редкие книги, карты, звукозаписи и движущиеся изображения.Для достижения своей цели эта уникальная государственно-частная программа также работает в сотрудничестве с членами Федерации цифровых библиотек и других библиотек и архивов по всей территории Соединенных Штатов. Например, включены цифровые коллекции конкурса цифровых библиотек LC / Ameritech. | |
| Журналы Американского метеорологического общества Содержит полные тексты статей в журналах и бюллетенях, опубликованных Американским метеорологическим обществом. | |
| Серия американских периодических изданий Серия американских периодических изданий включает оцифрованные изображения страниц американских журналов и журналов, опубликованных с колониальных времен до начала двадцатого века, охватывающих два столетия Америки (1741-1900). Названия варьируются от General Magazine Бенджамина Франклина и первого научного журнала Америки Medical Repository; популярные журналы, такие как Vanity Fair и Ladies ‘Home Journal; региональные и нишевые публикации; и новаторские журналы, такие как Dial, Puck и McClure’s. | |
| История американского радио Мировая история радио — это доступный для поиска цифровой репозиторий, содержащий почти шесть миллионов страниц истории AM, FM и телевещания с начала 1900-х годов до наших дней. | |
| Американское рабство: составная автобиография Широко известный как «Повествования о рабах WPA», «Американское рабство: составная автобиография» дает подлинный портрет жизни, культуры и выживания афроамериканцев в периоды рабства, реконструкции и Америки эпохи депрессии.Более 2000 автобиографических рассказов бывших рабов из 17 штатов включены в этот проект федерального писателя (FWP), который проводился под эгидой Управления рабочих проектов (WPA) и спонсировался Библиотекой Конгресса. Коллекция и ее индекс, полностью доступный для поиска по имени, штату, округу и возрасту, дополняются общедоступными дискуссионными форумами, ссылками на виртуальные учебные программы, учебные ресурсы и руководства по учебным программам, а также различные связанные веб-ресурсы. | |
| Исследовательская библиотека Американского общества инженеров-строителей Полнотекстовый доступ к различным журналам, публикуемым Американским обществом инженеров-строителей. | |
| Американский барометр Американский барометр — это исследование демократического общественного мнения и поведения в Северной и Южной Америке. Это попытка LAPOP измерить демократические ценности и поведение в Северной и Южной Америке с использованием национальных вероятностных выборок взрослых избирательного возраста. | |
| Интернет-журналы AMS Содержит полные тексты статей в журналах и бюллетенях, опубликованных Американским метеорологическим обществом. | |
| Публикации AMS Полнотекстовый доступ к различным журналам и журналам, издаваемым Американским математическим обществом. | |
| Издание библиотеки предков Ancestry Library Edition — это крупнейший в мире онлайн-ресурс по семейной истории, который может дать вам мгновенный доступ к сотням лет истории в миллиардах исторических документов и миллионам исторических фотографий со всего мира. | |
| Рефераты по поведению животных Указатели и рефераты важных статей, относящихся к поведению животных, от нейрофизиологии до поведенческой экологии, генетики, прикладной этологии и т. Д. | |
| Annee philologique Этот ценный ресурс содержит указатели книг, книжных обзоров, статей, Festschriften и других коллекций, посвященных древнегреческому и римскому миру со второго тысячелетия до нашей эры примерно до 800 года нашей эры. APh индексирует более 1500 научных журналов, а также сборники эссе и материалы конференций. Обратите внимание, что ресурс охватывает научные публикации во всем мире на многих языках, и в Библиотеке Рихтера есть ссылки только на некоторые из них. Пожалуйста, обратитесь к каталогу UML для местных холдингов. | |
| Годовые обзоры Служба Annual Reviews обеспечивает полнотекстовый доступ с возможностью поиска к обзорным статьям, посвященным биомедицине / наукам о жизни, физическим наукам, социальным наукам и экономике. | |
| Антропология Плюс Охватывает антропологию, археологию и междисциплинарные исследования. Включает антропологический указатель: с 1957 г. по настоящее время и антропологическую литературу: с конца XIX века по настоящее время | |
| AnthroSource Обеспечивает доступ к рецензируемым журналам, информационным бюллетеням и бюллетеням AAA.Новости антропологии предоставляются отдельным членам Американской антропологической ассоциации (AAA) как часть их членства. Онлайн-доступ к Anthropology News ограничен для не членов AAA, в том числе институциональных подписчиков на AnthroSource. Выпуски за последние десять лет доступны бесплатно только отдельным членам AAA. Более старые выпуски доступны в Интернете для учреждений, подписавшихся на AnthroSource. Этот ограниченный доступ был назначен AAA. На веб-сайте AnthroSource этот ограниченный доступ описан как 10-летняя подвижная стена.Следующие названия журналов имеют более раннее содержание, доступное через JSTOR: Американский антрополог, Американский этнолог, Культурная антропология, Этиос, Ежеквартальная медицинская антропология. Текущее содержание этих журналов AAA за последние 7 лет доступно в AnthroSource. Все выпуски с 1996 г. и ранее заархивированы в JSTOR. | |
| Коллекция изображений AP Более 12 миллионов фотографий, относящихся к 1826 году, более 36 000 звуковых фрагментов и более 340 000 профессионально созданных графических изображений.Охват охватывает более 185 лет, ежедневно добавляется более 3500 фотографий. | |
| APA PsycСтатьи Источник полнотекстовых рецензируемых научных и научных статей по психологии. | |
| APA PsycInfo Рефераты статей из научных журналов, глав книг, книг и диссертаций по поведенческим наукам и психическому здоровью.Цитаты и резюме датируются началом 1800-х годов; освещение журнала с 1887 года по настоящее время. От Американской психологической ассоциации. | |
| APA, Чикаго и MLA Ссылка: KnightCite KnightCite — это онлайн-сервис генератора цитат, предоставляемый библиотекой Хекмана при Колледже Кальвина. Эта услуга упрощает зачастую утомительную задачу составления точной библиографии в соответствующем стиле путем форматирования данных об источнике в надежную цитату, устраняя необходимость запоминать мельчайшие детали стиля для нескольких типов источников.Эта услуга предоставляется колледжем бесплатно и доступна для членов как внутри, так и за пределами сообщества Calvin. | |
| Исследовательские журналы Американского физического общества (APS) Полнотекстовый доступ к различным журналам Американского физического общества | |
| APS Онлайн Серия американских периодических изданий включает оцифрованные изображения страниц американских журналов и журналов, опубликованных с колониальных времен до начала двадцатого века, охватывающих два столетия Америки (1741-1900).Названия варьируются от General Magazine Бенджамина Франклина и первого научного журнала Америки Medical Repository; популярные журналы, такие как Vanity Fair и Ladies ‘Home Journal; региональные и нишевые публикации; и новаторские журналы, такие как Dial, Puck и McClure’s. | |
| Справочник по аквакультуре Глобальный сборник знаний по аквакультуре для принятия практических решений в области управления водными ресурсами и аквакультуры. | |
| Рефераты по водным наукам и рыболовству ASFA — это наиболее полная база данных, охватывающая исследования и техническую литературу по водным наукам. Подфайлы включают Environmental RouteNet и Water Resource RouteNet. | |
| Арабо-израильские отношения, 1917-1970: Интернет-серия на Ближнем Востоке 1 Обзор политической истории Ближнего Востока в 20 веке, основанный на первоисточниках из Национального архива Лондона.Первоначальный исходный материал из документов министерства иностранных дел, министерства по делам колоний, военного министерства и кабинета министров от Декларации Бальфура 1917 года до войны «Черный сентябрь 1970-1». Основные политические заявления изложены в их самом полном контексте, второстепенные документы и маргиналы раскрывают работу колониальной администрации и, после создания Государства Израиль в 1948 году, британскую дипломатию по отношению к Израилю и арабским государствам. | |
| Стандарты архитектурной графики Стандарты архитектурной графики предлагает архитекторам, дизайнерам и строительным подрядчикам исчерпывающее руководство по визуальному представлению материалов, продуктов, систем и сборок, необходимых для концептуализации и строительства зданий. | |
| ArchiveGrid Примечание: За помощью обращайтесь в Отдел специальных коллекций, 8-й этаж, Библиотека Отто Г. Рихтера, 305-284-3247 ArchiveGrid — это инструмент для поиска в исторических документах, личных бумагах и семейных историях, хранящихся в архивах по всему миру. | |
| Архивы человеческой сексуальности и идентичности: история и культура ЛГБТК с 1940 года Уникальная коллекция с возможностью поиска, Архивы человеческой сексуальности и идентичности: история и культура ЛГБТК с 1940 года, часть I объединяет примерно 1.5 миллионов страниц первичных источников по социальным, политическим, медицинским и юридическим вопросам, влияющим на ЛГБТ-сообщества по всему миру. Редкий и уникальный контент из микрофильмов, информационных бюллетеней, организационных документов, правительственных документов, рукописей, брошюр и других типов первоисточников проливает свет на движение за права геев, активизм, кризис ВИЧ / СПИДа и многое другое. В Части II рассказывается о развитии, культуре и обществе ЛГБТ-групп во второй половине двадцатого века, дается новый взгляд на разнообразное сообщество с помощью таких материалов, как стенограммы устной истории, дневники и письма, а также периодические издания и рукописи. . | |
| Архив сексуальности и пола Уникальная коллекция с возможностью полного поиска, Архивы человеческой сексуальности и идентичности: история и культура ЛГБТ с 1940 года, часть I объединяет около 1,5 миллиона страниц первичных источников по социальным, политическим, медицинским и юридическим вопросам, влияющим на сообщества ЛГБТК по всему миру. . Редкий и уникальный контент из микрофильмов, информационных бюллетеней, организационных документов, правительственных документов, рукописей, брошюр и других типов первоисточников проливает свет на движение за права геев, активизм, кризис ВИЧ / СПИДа и многое другое.В Части II рассказывается о развитии, культуре и обществе ЛГБТ-групп во второй половине двадцатого века, дается новый взгляд на разнообразное сообщество с помощью таких материалов, как стенограммы устной истории, дневники и письма, а также периодические издания и рукописи. . | |
| Архив пресвитерианской церкви Кубы Интернет Этот сборник предоставляет для исследования записи Iglesia Presbiteriana-Reformada en Cuba (IPRC) и предшествующих пресвитерианских церквей и миссий на Кубе, включая полный выпуск Heraldo Cristiano, церковного информационного бюллетеня за 1919 2010 г., который обеспечивает основу по истории церкви.Также включены периодические издания Juprecu и Su Voz, ранние записи миссии, которые сначала ведутся на английском, а затем на испанском языках, так как общины переняли управление своими церквями и школами от миссионеров. Сюда входят протоколы сессий и записи о членстве / крещении / браке / смерти, а также протоколы мужских, женских и молодежных групп, включая их миссионерскую работу в своих общинах. | |
| Архивы несвязанные Тематические цифровые коллекции исторических документов по широкому кругу вопросов. | |
| ARL Годовое обследование заработной платы Ежегодный обзор заработной платы ARL сообщает о зарплатах более чем 12 000 профессиональных должностей в библиотеках-членах ARL на ежегодной основе. Эти данные используются для определения конкурентоспособности и справедливости заработной платы в разных учреждениях и личных характеристик, а также для того, чтобы не отставать от инфляции. Опрос также отслеживает представительство меньшинств в библиотеках ARL США и предоставляет отдельные данные для библиотек медицинских наук и юридических библиотек. | |
| Комплекты ARL SPEC Опросы SPEC собирают информацию от учреждений-членов ARL о текущих методах и политике исследовательских библиотек. Наборы SPEC Kits объединяют результаты опроса и документацию организаций-членов ARL, чтобы помочь библиотекам решать постоянно меняющиеся проблемы, с которыми сталкиваются библиотеки. Эти руководства помогают библиотекам изучать текущую практику исследовательских библиотек, внедрять новые практики и технологии, управлять изменениями и повышать производительность. | |
| Статистика по | ARL Статистика ARL — это серия ежегодных публикаций, в которых описываются коллекции, расходы, укомплектование персоналом и обслуживание библиотек-членов ARL. Сборник статистики ARL включает ежегодные публикации ARL Statistics, ARL Academic Health Sciences Library Statistics и ARL Academic Law Library Statistics, которые были опубликованы с 2006 года по настоящее время. |
| Art Abstracts (H.У. Уилсон) Art Abstracts содержит цитаты и аннотации к журнальным статьям и другим ресурсам по искусству, истории искусства, архитектуре, фотографии, археологии, городскому планированию, кино и другим смежным темам. Услуга включает ссылки и возможность перекрестного поиска на подписку библиотеки на библиотеку AMICO. | |
| Art Index Retrospective: 1929-1984 (Х.У. Уилсон) Art Index Retrospective — это библиографическая база данных с возможностью поиска, которая содержит цитаты из печатного Art Index, тома 1-32, опубликованного в период с 1929 по 1984 год.Услуга включает ссылки и возможность перекрестного поиска на подписку библиотеки на библиотеку AMICO. | |
| Артемида: литературные источники Платформа перекрестного поиска по всем литературным источникам Gale, которая обеспечивает беспрепятственный исследовательский опыт, который помогает исследователям всех уровней находить отправную точку, выполнять поиск по широкому спектру материалов и моментов времени и открывать новые способы анализа информации.Пользователи смогут искать среди множества первоисточников, критических статей, литературного и культурного анализа и биографий. В «Литературных источниках Гейла» доступны следующие коллекции:
| |
| Artemis: Первоисточники Интегрированная исследовательская среда, которая позволяет пользователям выполнять поиск по всем коллекциям первичных источников Gale. Следующие коллекции в настоящее время доступны в Gale Artemis: Первоисточники:
| |
| ARTFL (Американские и французские исследования сокровищницы французского языка) ARTFL обеспечивает доступ к базам данных, содержащим полные тексты широкого спектра важных книг, текстов, библиографий и других работ, поддерживающих изучение французского языка и литературы.Сайт содержит доступные для поиска базы данных (Основная база данных французских текстов ARTFL, ARTFL: База данных французских женщин-писательниц и ARTFL: База данных Provenal Poetry) и поддерживает множество общедоступных баз данных, включая Dictionnaires d’autrefois, Encyclopédie of Diderot и d’Alembert, и Bibliothèque Bleue de Troyes. | |
| ARTFL Французские словари Справочная страница ARTFL содержит ссылки на Dictionnaires d’autrefois, недавно разработанный французско-английский, англо-французский современный словарь и другие справочные материалы для изучения лингвистики. | |
| Основная база данных французских текстов ARTFL Полный текст из более чем 3500 французских текстов с 12 по 20 века. | |
| ARTFL: База данных французских писательниц Французские женщины-писательницы (FWW) проекта ARTFL — это база данных с возможностью поиска, содержащая более 150 произведений французских женщин-писателей с 16 по 20 век. | |
| ARTFL: База данных провансальской поэзии Эта база данных на французском языке содержит полные тексты провансальской поэзии. Отобранные работы охватывают период с 1130 по 1300. | |
| СтатьяПервая ArticleFirst — это ежедневно обновляемый междисциплинарный указатель и реферативный сервис, охватывающий статьи в академических периодических изданиях. | |
| Индекс цитирования в области искусства и гуманитарных наук Международный охват более чем 1150 ведущих журналов по искусству и гуманитарным наукам, а также выборочное освещение из ведущих научных и социальных журналов. | |
| АРТстор ARTstor состоит из репозитория сотен тысяч цифровых изображений и связанных данных, включая инструменты для активного использования этих изображений и среды ограниченного использования, которая стремится сбалансировать права поставщиков контента с потребностями и интересами пользователей контента.Коллекции ARTstor состоят из взносов музеев, отдельных фотографов, ученых, специальных коллекций библиотек и фотоархивов. Все изображения сопровождаются исчерпывающими метаданными и разрешены для использования в образовательных целях. | |
| Научная библиотека ASCE Полнотекстовый доступ к различным журналам, публикуемым Американским обществом инженеров-строителей. | |
| ASFA: Рефераты по водным наукам и рыболовству ASFA — это наиболее полная база данных, охватывающая исследования и техническую литературу по водным наукам.Подфайлы включают Environmental RouteNet и Water Resource RouteNet. | |
| Коллекция изображений Ассошиэйтед Пресс Более 12 миллионов фотографий, относящихся к 1826 году, более 36 000 звуковых фрагментов и более 340 000 профессионально созданных графических изображений. Охват охватывает более 185 лет, ежедневно добавляется более 3500 фотографий. | |
| Интернет-архив Ассоциации культурного равенства Аудио, видео, фотографии и другие оцифрованные материалы из архива Алана Ломакса Ассоциации культурного равенства. | |
| ASTM Компас ASTM Compass — это сборник ведущих в отрасли стандартов и технической инженерной информации. Библиотека охватывает ряд инженерных дисциплин, включая аэрокосмическую, биомедицинскую, химическую, гражданскую, экологическую, геологическую, охранную, промышленную, материаловедение, механическую, ядерную, нефтяную, почвоведение и солнечную инженерию. | |
| Система астрофизических данных (ADS) Система астрофизических данных (ADS) SAO / NASA — это портал цифровой библиотеки для исследователей в области астрономии и физики.ADS поддерживает три библиографические базы данных, содержащие более 12,6 миллионов записей, охватывающих публикации по астрономии и астрофизике, физике и электронные печатные издания arXiv. Он обеспечивает доступ к (1) рефератам по астрономии, приборам, физике и геофизике; (2) полные тексты журнальных статей и сканированные книги; (3) ссылки на каталоги астрономических данных НАСА. | |
| База данных религии ATLA с ATLASerials База данных религии Атла — важный ресурс для религиозных и богословских исследований, содержащий более 2.8 миллионов библиографических записей, охватывающих такие темы, как библейские исследования, мировые религии, история церкви и религия в социальных вопросах. | |
| Индекс Эйвери по архитектурной периодике (EBSCOHost) The Avery Index to Architectural Periodicals охватывает архитектуру и смежные области, такие как археология, городское планирование, сохранение исторических памятников и дизайн интерьеров. Охват охватывает период с 1930-х годов (с выборочным охватом с 1860-х годов) по настоящее время. | |
| AVON AVON — это платформа для потокового видео, предоставляющая более 68 000 наименований, охватывающих широкий спектр предметных областей, включая антропологию, бизнес, историю, музыку и многое другое. |
Институт цифровых стипендий ARL — Ассоциация исследовательских библиотек
Институт цифровых стипендий ARL (DSI) проводит серию летних семинаров 9, 16, 23 и 30 июля 2021 года для предыдущих участников одного из своих пятидневных институтов, проходивших с 2017 по 2019 год, а также для коллег, подавших заявки на участие в программе. Институт летом 2020 года, закрытый из-за COVID-19.Серия семинаров включает четыре двухчасовых занятия и будет посвящена следующим темам:
Инструменты для развивающейся и устойчивой цифровой стипендии
В последние годы цифровая наука переместилась в сторону устойчивой и горизонтальной инфраструктуры с минимальными вычислительными технологиями. На этом заседании будут рассмотрены 1) вычислительные среды на базе Интернета для обучения программированию и публикации кода и 2) структуры статических веб-сайтов для создания цифровых коллекций и выставок. Участники познакомятся с различными инструментами и методами, образцовыми проектами, а также с потенциальными рабочими процессами и идеями для своих собственных проектов.
Педагогика цифровых стипендий
Сессия «Педагогика цифровых стипендий» будет посвящена процессам разработки целей, формированию инструкций и оценке обучения, а также дополнительным требованиям, ресурсам и соображениям, необходимым для интеграции курса или разработки семинара и учебного пособия. Участники будут совместно изучать примеры учебных программ, семинаров и учебных пособий, чтобы изучить различные педагогические подходы и практики. Эта сессия направлена на ознакомление участников с ключевыми компонентами учебного дизайна цифровых стипендий и педагогических консультаций.
Уход как компас: заземление DS в сообществе (DEIA / SJ)
На этом семинаре будет рассмотрено, как ученые в области цифровых технологий могут сосредоточить сообщество и осторожно подходить к каждому этапу исследовательского процесса, критически изучая происхождение, отображение и управление данными. Мы определяем заботу как отстаивание интересов всех людей и сообществ, на которые оказывает влияние исследовательский процесс или которые явно представлены в нем; признание и уменьшение привилегий, предвзятости и потенциального вреда, присущего исследовательским инструментам и методологиям; и устранение любых молчаний или пробелов в исследовательских материалах.Вместе мы обсудим отстаивание целей проекта, ориентированных на сообщества, инструменты навигации и институциональные ограничения, критическое использование пробелов и замалчиваний данных, новые и / или альтернативные методологии и практики, а также участие в важных беседах с заинтересованными сторонами проекта. Чтобы направить нашу беседу, мы посетим существующие цифровые проекты, чтобы применить концепции ухода в практических ситуациях. Участникам будет предложено поразмышлять о пересечении ухода с их собственными подходами к цифровой науке.
Начало работы с подготовкой и анализом текста: практический обзор инструментов и подходов
Вы заинтересованы в текстовом анализе, но не знаете, с чего начать? Присоединяйтесь к нам для интерактивного введения «без опыта» в основные концепции, процессы и методологические подходы к подготовке и анализу текста. После общего введения в тему участникам будут предложены подготовленные упражнения, демонстрирующие, как можно использовать различные программные пакеты (OpenRefine, Python) для подготовки и выполнения текстового анализа.Тем, у кого нет опыта программирования на Python, будет предоставлена возможность изучить основы с помощью самостоятельных модулей перед сеансом (необязательно). Что наиболее важно, участники покидают сеанс с большей уверенностью, используя различные программные и вычислительные подходы, и лучше понимая, где найти дополнительные учебные ресурсы для дальнейшего обучения.

