Что такое циклические углеводороды. Какие бывают виды циклических углеводородов. Как устроены молекулы циклоалканов. Какими свойствами обладают циклические соединения. Где применяются циклические углеводороды в промышленности.
Циклические углеводороды: общая характеристика и классификация
Циклические углеводороды представляют собой органические соединения, в молекулах которых атомы углерода образуют замкнутые циклы (кольца). Наличие циклической структуры придает этим веществам ряд специфических свойств, отличающих их от ациклических аналогов.
Основные классы циклических углеводородов:
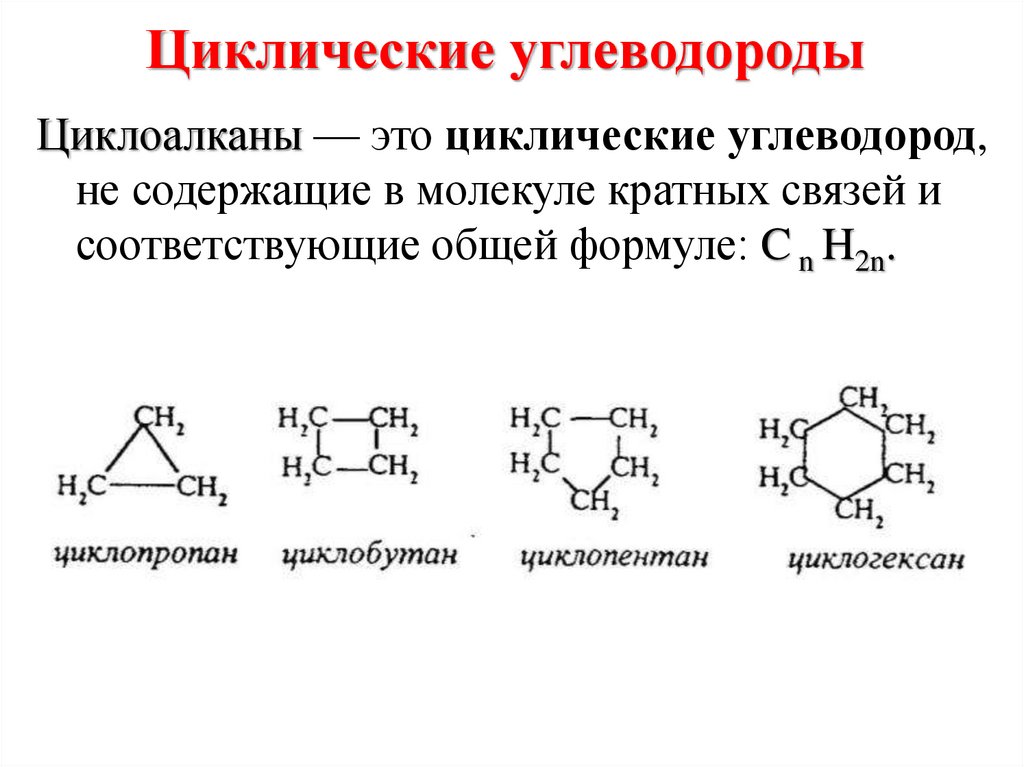
- Циклоалканы (циклопарафины) — насыщенные циклические углеводороды
- Циклоалкены — ненасыщенные циклические углеводороды с одной двойной связью
- Циклоалкадиены — с двумя двойными связями
- Циклоалкины — с одной тройной связью
- Арены (ароматические углеводороды) — с системой сопряженных двойных связей
Циклические углеводороды широко распространены в природе и играют важную роль в живых организмах. Многие из них находят применение в химической промышленности как сырье для синтеза полимеров, лекарств и других веществ.

Строение и изомерия циклоалканов
Циклоалканы имеют общую формулу CnH2n. Простейшим представителем является циклопропан C3H6. Наиболее устойчивы 5-7-членные циклы. Как устроены молекулы циклоалканов?
- Атомы углерода образуют замкнутую цепь (цикл)
- Все связи С-С одинарные
- Валентности атомов углерода насыщены атомами водорода
Для циклоалканов характерны следующие виды изомерии:
- Структурная изомерия — различное расположение заместителей
- Пространственная изомерия
- Цис-транс-изомерия
- Конформационная изомерия (различные конформации молекулы)
Конформации циклогексана — «кресло» и «ванна» — отличаются расположением атомов в пространстве при сохранении химических связей. Конформация «кресло» энергетически более выгодна.
Физические и химические свойства циклоалканов
Физические свойства циклоалканов во многом сходны с алканами нормального строения:
- Бесцветные вещества
- Малорастворимы в воде, хорошо растворяются в органических растворителях
- Температуры кипения и плавления выше, чем у соответствующих алканов
Химические свойства циклоалканов определяются наличием напряжения в цикле. Чем выше напряжение, тем выше реакционная способность. Основные типы реакций:

- Реакции присоединения (характерны для малых циклов)
- Реакции замещения (преобладают для циклогексана и высших циклоалканов)
- Реакции изомеризации
Методы получения и области применения циклоалканов
Основные промышленные и лабораторные способы получения циклоалканов:
- Выделение из нефти
- Циклизация алканов
- Внутримолекулярная дегидратация спиртов
Циклоалканы находят широкое применение в различных отраслях промышленности:
- Сырье для производства полимеров (капрон, найлон)
- Растворители в лакокрасочной промышленности
- Компоненты моторных топлив
- Исходные вещества для синтеза лекарственных препаратов
Ароматические углеводороды (арены)
Арены — циклические углеводороды с системой сопряженных двойных связей. Простейший представитель — бензол C6H6. Чем характеризуются ароматические соединения?
- Наличие замкнутой системы сопряженных π-связей
- Плоское строение молекулы
- Повышенная устойчивость (ароматичность)
- Склонность к реакциям замещения
Бензол и его гомологи широко применяются как растворители и сырье для синтеза красителей, лекарств, пластмасс и других веществ. При этом некоторые арены токсичны, поэтому их использование строго регламентируется.

Биологическая роль циклических углеводородов
Многие природные соединения содержат циклические фрагменты. Какую роль играют циклические углеводороды в живых организмах?
- Входят в состав стероидных гормонов (холестерин, тестостерон)
- Являются компонентами витаминов (A, D)
- Участвуют в построении клеточных мембран
- Служат основой для синтеза биологически активных веществ
Циклические структуры обеспечивают пространственную жесткость молекул и их специфическое взаимодействие с биологическими мишенями. Это определяет важную физиологическую роль циклических соединений.
Экологические аспекты использования циклических углеводородов
Широкое промышленное применение циклических углеводородов связано с определенными экологическими рисками:
- Токсичность многих ароматических соединений
- Низкая скорость биоразложения в окружающей среде
- Накопление в пищевых цепях
- Канцерогенные свойства некоторых аренов
Для снижения негативного воздействия на экосистемы необходимы:
- Строгий контроль за использованием опасных веществ
- Разработка более безопасных аналогов
- Совершенствование методов очистки промышленных выбросов
- Развитие технологий утилизации отходов
Рациональное использование циклических углеводородов позволит сохранить их ценные свойства при минимизации вреда для окружающей среды.

Перспективы исследований циклических углеводородов
Изучение циклических углеводородов остается актуальным направлением современной органической химии. Какие задачи стоят перед учеными в этой области?
- Поиск новых методов селективного синтеза циклических соединений
- Исследование необычных циклических структур (например, циклинов)
- Изучение механизмов реакций с участием циклических молекул
- Компьютерное моделирование свойств сложных циклических систем
- Разработка новых катализаторов для превращений циклических углеводородов
Развитие этих направлений позволит создать новые функциональные материалы и лекарственные препараты на основе циклических углеводородов.
Углеводороды — Что такое Углеводороды?
Соединения углеводородов отличаются друг от друга количеством атомов углерода и водорода, строением углеродного скелета и типом связей между атомами.
Углеводороды (hydrocarbon) – это органические соединения, состоящие из углерода и водорода.
Углеводороды служат фундаментальной основой органической химии: молекулы любых других органических соединений рассматривают как их производные.
Соотношение между углеродом и водородом в углеводородах колеблется в широких пределах (10-90 %).
Соединения углеводородов отличаются друг от друга:
- количеством атомов углерода и водорода,
- строением углеродного скелета,
- типом связей между атомами.
Большинство углеводородов в природе встречаются в сырой нефти.
Кроме того, основными источниками углеводородов являются природный газ, сланцевый газ (низкопроницаемых коллекторов), попутный нефтяной газ (ПНГ), горючие сланцы, уголь, торф.
Классификация углеводородов
Алканы (парафины) – углеводороды общей формулы CnH2n+2, в молекулах которых атомы углерода связаны между собой σ-связью, а остальные их валентности предельно насыщены атомами водорода.
Отсюда другое название алканов – предельные углеводороды.
Первым представителем данного гомологического ряда является метан СН4.
Алкены (олефины) относятся к непредельным углеводородам общей формулы C
nH2n.
В молекуле алкена кроме σ-связей содержится одна π-связь.
Первый представитель гомологического ряда – этилен С2Н4, поэтому алкены называют также «этиленовыми углеводородами».
Диеновые углеводороды содержат в молекуле 2 двойные связи.
Общая формула СnН2n-2.
Первым представителем ряда является бутадиен СН2=СН–СН=СН2.
Алкинами называются углеводороды общей формулы CnH2n-2, молекулы которых содержат тройную связь.
Первый представитель гомологического ряда – ацетилен С2Н2, поэтому алкины называют также «ацетиленовыми углеводородами».
Молекулы циклоалканов содержат циклы разной величины, атомы углерода в которых связаны между собой только σ-связью.
Циклоалкены содержат одну двойную связь и имеют общую формулу СnН2n-2.
Углеводороды, имеющие кратные связи, легко вступают в реакции присоединения по месту разрыва π-связей.
Ароматические углеводороды (арены) – углеводороды общей формулы CnH2n-6.
Первые представители ароматических углеводородов были выделены из природных источников и обладали своеобразным запахом, поэтому и получили название «ароматические».
Важнейшим представителем ароматических углеводородов является бензол С6Н6.
В молекуле бензола 6 атомов углерода, соединяясь σ-связями, образуют правильный шестиугольник.
В результате сопряжения 6 свободных р-электронов образуется единое π-электронное облако над и под плоскостью кольца.
Природные источники углеводородов
Каменный уголь – плотная осадочная порода черного, иногда сepo-черного цвета, дающая на фарфоровой пластинке черную черту.
Каменный уголь представляет собой продукт глубокого разложения остатков растений, погибших миллионы лет назад (древовидных папоротников, хвощей и плаунов, а также первых голосеменных растений).
В органическом веществе угля содержится 75-92 % углерода, 2,5-5,7 % водорода, 1,5-15 % кислорода.
Международное название элемента углерода происходит от лат. carbō («уголь»).
Природный газ – полезное ископаемое, основным компонентом которого является метан СН4 (75-98 %).
В природном газе содержатся также его ближайшие гомологи: этан С2Н6, пропан С3Н8, бутан С4Н10 и следовые количества более тяжелых легкокипящих углеводородов.
Существует следующая закономерность: чем выше относительная молекулярная масса углеводорода, тем меньше его количество в природном газе.
Содержание сероводорода и его органических производных (тиолов) в природном газе в сумме может достигать 5-25 %.
Попутные нефтяные газы (ПНГ) — газы, которые находятся в природе над нефтью или растворены в ней под давлением.
Их состав может быть выражен примерным соотношением компонентов: метан – 31 %, этан – 7,5 %, пропан – 21,5 %,
бутан – 20 %, пентан и гексан (легкокипящие жидкости) – 20 %.
С каждой тонной добытой нефти выделяется около 50 м3 газов, которые вплоть до середины 20 века сжигали в факелах, причиняя двойной ущерб – теряли ценное сырье и загрязняли атмосферу.
Первым предприятием в России, на котором стали использовать ПНГ, стала Сургутская ГРЭС.
6 основных энергоблоков, работающих на ПНГ, были введены в строй в 1985-1988 гг.
В настоящее время ПНГ улавливают и используют как топливо (в том числе и автомобильное) и ценное химическое сырье.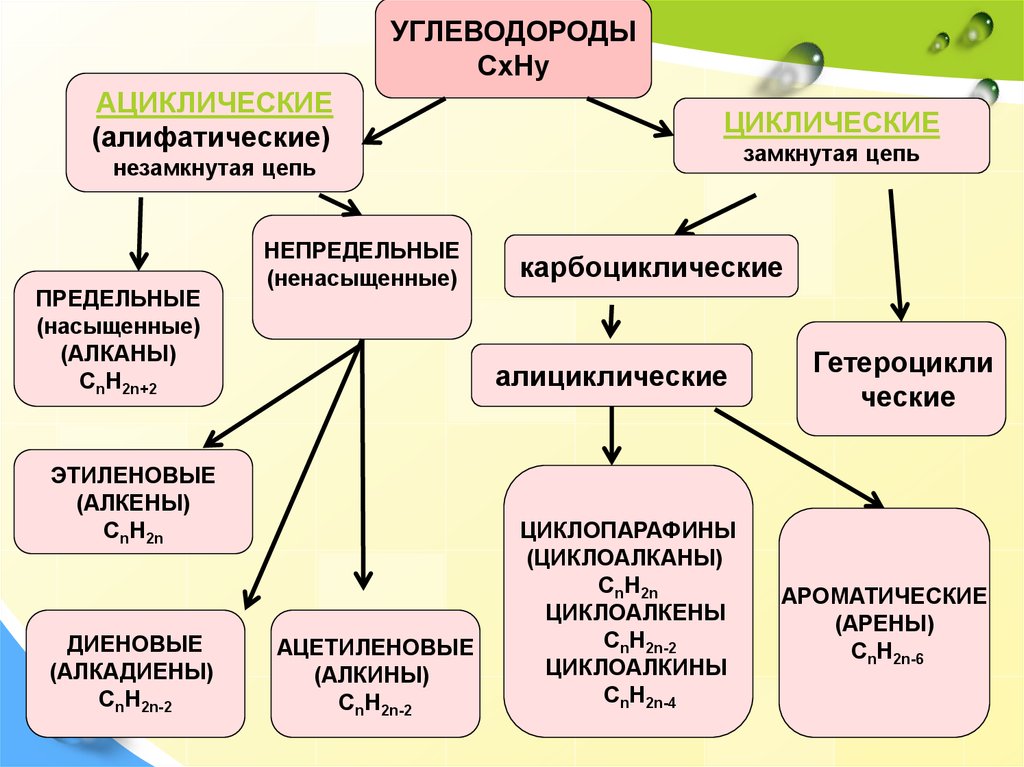
Нефть – смесь углеводородов от светло-бурого до черного цвета с характерным запахом.
Нефть намного легче воды и в ней не растворяется.
В зависимости от происхождения нефть может содержать большое количество алифатических, циклических или ароматических углеводородов.
Так, например, бакинская нефть богата циклоалканами и содержит сравнительно небольшое количество алифатических предельных углеводородов.
Значительно больше алканов в грозненской, ферганской, а также нефти штата Пенсильвания (США).
Пермская нефть содержит ароматические углеводороды.
В небольших количествах в состав нефти могут входить также кислородсодержащие соединения, как, например, альдегиды, кетоны, эфиры и карбоновые кислоты.
Тест Циклические углеводороды: циклоалканы, арены
информационная поддержка студентов
INFO STADIYA — это площадка, на которой студент сможет найти ответ на любой вопрос, а так же получить консультацию, касательно написания студенческих работ. Здесь, вы можете заказать диплом, курсовую, реферат, отчет по практике, документы для приложений, задачи, и многие другие виды ученических заданий. В нашей компании работает большое количество квалифицированных авторов. Ознакомиться ценами на услуги, можно на соответствующей странице.
Здесь, вы можете заказать диплом, курсовую, реферат, отчет по практике, документы для приложений, задачи, и многие другие виды ученических заданий. В нашей компании работает большое количество квалифицированных авторов. Ознакомиться ценами на услуги, можно на соответствующей странице.
ПОСМОТРЕТЬ РАСЦЕНКИ НА УСЛУГИ
Тест по химии по теме «Циклические углеводороды: циклоалканы, арены» призван оценить знания студентов по курсу «Химия». В тесте правильные ответы выделены «+»
Насыщенные алициклические углеводороды называют:
-: циклоалкадиенами;
-: циклоалкенами;
+: циклоалканами;
-: среди ответов нет верного.
Ненасыщенные алициклические углеводороды с одной двойной связью называют:
-: циклоалкадиенами;
+: циклоалкенами;
-: циклоалканами;
-: среди ответов нет верного.
Ненасыщенные алициклические углеводороды с двумя двойными связями называют:
+: циклоалкадиенами;
-: циклоалкенами;
-: циклоалканами;
-: среди ответов нет верного.
Углеводороды бензольного ряда-это:
-: алкены;
-: алкины;
+: арены;
-: среди ответов нет верного.
Атомы углерода в бензоле находятся в состоянии:
-: sp3-гибридизации;
+: sp2- гибридизации;
-: sp- гибридизации;
-: среди ответов нет верного.
Согласно правилу Хюккеля, ароматические молекулы должны иметь:
+: плоский циклический σ -скелет и число обобщенных π -электронов, равное 4n+2;
-: плоский циклический σ -скелет и число обобщенных π -электронов, равное 2n+2;
-: плоский циклический σ -скелет и число обобщенных π -электронов, равное 4n
-: среди ответов нет верного.
Химические свойства ароматических углеводородов определяются в первую очередь наличием в их молекулах:
-: заместителей;
+: сопряженной системы;
-: заместителей и сопряженной системы;
-: среди ответов нет верного.
Арены склонны к реакциям:
-: присоединения;
-: окисления;
+: замещения;
-: среди ответов нет верного.
Для Аренов характерно:
-: они склонны к таким реакциям, в результате которых нарушается ароматичность;
+: реакции электофильного замещения в ароматическом ядре;
-: реакции свободно-радикального замещения в ароматическом ядре;
-: реакции окисления;
Для Аренов характерно:
-: они склонны к таким реакциям, в результате которых нарушается ароматичность;
-: реакции свободно-радикального замещения в ароматическом ядре;
-: реакции окисления;
+: химические свойства определяются в первую очередь наличием в их молекулах сопряженной системы- они склонны к таким реакциям , в результате которых сохраняется ароматичность.
Для ароматических углеводородов, в отличие от алкенов, более характерны реакции …
-: присоединения
+: замещения
-: гидрогалогенирования
-: гидратации
Метки: Тесты по химии
← Предыдущий пост
Следующий пост →
Info Stadiya — информационная поддержка студентов.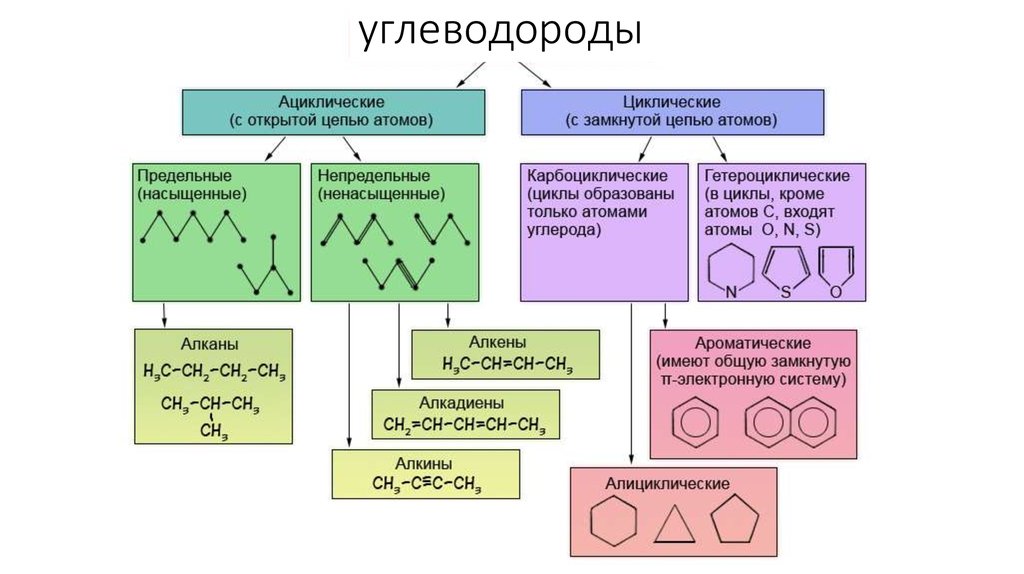 Большая коллекция справочных материалов для студентов всех направлений и специальностей. Наш сайт, поможет тебе сдать экзамены на отлично! Если вы сочли информацию на сайте полезной, обязательно поделитесь ей в социальных сетях или у себя на сайте, таким способом, вы поможете другим получить знания. © 2017
Большая коллекция справочных материалов для студентов всех направлений и специальностей. Наш сайт, поможет тебе сдать экзамены на отлично! Если вы сочли информацию на сайте полезной, обязательно поделитесь ей в социальных сетях или у себя на сайте, таким способом, вы поможете другим получить знания. © 2017
25.6: Циклические углеводороды — Химия LibreTexts
-
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 53998
Хотя циклогексан можно выделить из нефтепродуктов, основным источником этого химического вещества является гидрогенизация бензола. Большая часть произведенного циклогексана используется для производства промежуточных продуктов для производства нейлона. Такие предметы, как нейлоновые воздушные шары, без сомнения, появились на химическом заводе, где газообразный водород и бензол реагировали при высоких температурах с образованием циклогексана. Затем этот циклоалкан подвергается нитрированию, чтобы начать процесс формирования длинных нитей нейлона, из которых можно делать воздушные шары, веревки, одежду и многие другие полезные изделия.
Такие предметы, как нейлоновые воздушные шары, без сомнения, появились на химическом заводе, где газообразный водород и бензол реагировали при высоких температурах с образованием циклогексана. Затем этот циклоалкан подвергается нитрированию, чтобы начать процесс формирования длинных нитей нейлона, из которых можно делать воздушные шары, веревки, одежду и многие другие полезные изделия.
Циклические углеводороды
Циклический углеводород представляет собой углеводород, в котором углеродная цепь соединяется сама с собой в кольцо. Циклоалкан представляет собой циклический углеводород, в котором все углерод-углеродные связи являются одинарными. Как и другие алканы, циклоалканы являются насыщенными соединениями. Циклоалканы имеют общую формулу \(\ce{C_{n}H_{2n}}\). Простейшим циклоалканом является циклопропан с трехуглеродным кольцом.
Рисунок \(\PageIndex{1}\): Циклопропан — простейший циклоалкан. Его сильно напряженная геометрия делает его довольно нестабильным и очень реактивным. 9\text{o}\), молекула сморщена. Сморщивание кольца означает, что каждый второй атом углерода находится выше и ниже плоскости. На рисунке ниже показаны две возможности для сморщенной молекулы циклогексана. Каждая из структур называется конформацией. Конформация слева называется конформацией стула, а правая — конформацией лодки. Рисунок \(\PageIndex{2}\): Конформации кресла (слева) и лодки (справа) для циклогексана.
9\text{o}\), молекула сморщена. Сморщивание кольца означает, что каждый второй атом углерода находится выше и ниже плоскости. На рисунке ниже показаны две возможности для сморщенной молекулы циклогексана. Каждая из структур называется конформацией. Конформация слева называется конформацией стула, а правая — конформацией лодки. Рисунок \(\PageIndex{2}\): Конформации кресла (слева) и лодки (справа) для циклогексана. Хотя обе конформации уменьшают напряжение кольца по сравнению с плоской молекулой, предпочтительнее стул. Это связано с тем, что конформация кресла приводит к меньшему количеству отталкивающих взаимодействий между атомами водорода. Однако между двумя конформациями легко происходит взаимопревращение.
Также существуют более крупные циклоалканы, но они менее распространены. Циклические углеводороды также могут быть ненасыщенными. Циклоалкен представляет собой циклический углеводород по крайней мере с одной двойной углерод-углеродной связью. Циклоалкин представляет собой циклический углеводород с по крайней мере одной тройной углерод-углеродной связью. Ниже показаны упрощенные структурные формулы циклогексена и циклооктина.
Ниже показаны упрощенные структурные формулы циклогексена и циклооктина.
Резюме
- Циклический углеводород – это углеводород, в котором углеродная цепь соединяется сама с собой в кольцо.
- Циклоалкан представляет собой циклический углеводород, в котором все углерод-углеродные связи являются одинарными. (Как и другие алканы, циклоалканы являются насыщенными соединениями.)
- Циклоалкен представляет собой циклический углеводород, содержащий по крайней мере одну углерод-углеродную двойную связь.
- Циклоалкин представляет собой циклический углеводород с по крайней мере одной тройной углерод-углеродной связью.
- Приведены названия и строение типичных циклических углеводородов.
Эта страница под названием 25.6: Циклические углеводороды распространяется под лицензией CK-12 и была создана, изменена и/или курирована Фондом CK-12 с помощью исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
ЛИЦЕНЗИЯ ПОД
- Наверх
-
- Была ли эта статья полезной?
-
- Тип изделия
- Раздел или Страница
- Автор
- Фонд CK-12
- Лицензия
- СК-12
- Программа OER или Publisher
- СК-12
- Показать страницу TOC
- № на стр.
-
- Теги
-
- источник@https://flexbooks.
 ck12.org/cbook/ck-12-chemistry-flexbook-2.0/
ck12.org/cbook/ck-12-chemistry-flexbook-2.0/
- источник@https://flexbooks.
11.6: Циклические углеводороды — Химия LibreTexts
-
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 212527
Хотя циклогексан можно выделить из нефтепродуктов, основным источником этого химического вещества является гидрогенизация бензола. Большая часть произведенного циклогексана используется для производства промежуточных продуктов для производства нейлона. Такие предметы, как нейлоновые воздушные шары, без сомнения, появились на химическом заводе, где газообразный водород и бензол реагировали при высоких температурах с образованием циклогексана. Затем этот циклоалкан подвергается нитрированию, чтобы начать процесс формирования длинных нитей нейлона, из которых можно делать воздушные шары, веревки, одежду и многие другие полезные изделия.
Затем этот циклоалкан подвергается нитрированию, чтобы начать процесс формирования длинных нитей нейлона, из которых можно делать воздушные шары, веревки, одежду и многие другие полезные изделия.
Циклические углеводороды
Циклический углеводород представляет собой углеводород, в котором углеродная цепь соединяется сама с собой в кольцо. Циклоалкан представляет собой циклический углеводород, в котором все углерод-углеродные связи являются одинарными. Как и другие алканы, циклоалканы являются насыщенными соединениями. Циклоалканы имеют общую формулу \(\ce{C_{n}H_{2n}}\). Простейшим циклоалканом является циклопропан с трехуглеродным кольцом.
Рисунок \(\PageIndex{1}\): Циклопропан — простейший циклоалкан. Его сильно напряженная геометрия делает его довольно нестабильным и очень реактивным. 9\text{o}\), молекула сморщена. Сморщивание кольца означает, что каждый второй атом углерода находится выше и ниже плоскости. На рисунке ниже показаны две возможности для сморщенной молекулы циклогексана. Каждая из структур называется конформацией. Конформация слева называется конформацией стула, а правая — конформацией лодки. Рисунок \(\PageIndex{2}\): Конформации кресла (слева) и лодки (справа) для циклогексана.
Каждая из структур называется конформацией. Конформация слева называется конформацией стула, а правая — конформацией лодки. Рисунок \(\PageIndex{2}\): Конформации кресла (слева) и лодки (справа) для циклогексана. Хотя обе конформации уменьшают напряжение кольца по сравнению с плоской молекулой, предпочтительнее стул. Это связано с тем, что конформация кресла приводит к меньшему количеству отталкивающих взаимодействий между атомами водорода. Однако между двумя конформациями легко происходит взаимопревращение.
Также существуют более крупные циклоалканы, но они менее распространены. Циклические углеводороды также могут быть ненасыщенными. Циклоалкен представляет собой циклический углеводород по крайней мере с одной двойной углерод-углеродной связью. Циклоалкин представляет собой циклический углеводород с по крайней мере одной тройной углерод-углеродной связью. Ниже показаны упрощенные структурные формулы циклогексена и циклооктина.
Резюме
- Циклический углеводород – это углеводород, в котором углеродная цепь соединяется сама с собой в кольцо.