Как работают основные типы батарей для электромобилей. Какие преимущества и недостатки у литий-ионных аккумуляторов. Какие перспективные типы топливных элементов существуют для электротранспорта. Как устроены и для чего применяются суперконденсаторы в электромобилях.
Основные типы электрохимических источников тока для электромобилей
Для питания электродвигателей и вспомогательных систем электромобилей и гибридов используются три основных типа электрохимических источников тока:
- Аккумуляторные батареи
- Топливные элементы
- Суперконденсаторы
Каждый из этих источников имеет свои особенности, преимущества и недостатки. Рассмотрим их подробнее.
Аккумуляторные батареи для электромобилей
Аккумуляторные батареи — наиболее распространенный тип источника питания для современных электромобилей. Основные виды аккумуляторов, применяемых в электротранспорте:
- Свинцово-кислотные
- Никель-металлгидридные (Ni-MH)
- Литий-ионные (Li-ion)
Свинцово-кислотные аккумуляторы
Свинцово-кислотные батареи использовались в первых электромобилях. Их преимущества:
- Низкая стоимость
- Отработанная технология производства
- Возможность глубокого разряда
Однако они имеют ряд существенных недостатков для применения в современных электромобилях:
- Низкая удельная энергоемкость (30-40 Вт*ч/кг)
- Большой вес
- Ограниченное количество циклов заряд-разряд
- Длительное время заряда
Из-за этих недостатков свинцово-кислотные батареи сейчас практически не используются в электромобилях.
Никель-металлгидридные аккумуляторы
Ni-MH аккумуляторы получили широкое распространение в гибридных автомобилях. Их характеристики:
- Удельная энергоемкость 60-80 Вт*ч/кг
- Срок службы до 1000 циклов заряд-разряд
- Возможность быстрого заряда
- Устойчивость к перезаряду и глубокому разряду
Недостатки Ni-MH аккумуляторов:
- Высокий саморазряд
- Эффект памяти
- Содержание токсичного кадмия
В настоящее время Ni-MH батареи вытесняются более эффективными литий-ионными.
Литий-ионные аккумуляторы
Литий-ионные батареи сегодня являются основным типом источников питания для электромобилей. Их ключевые преимущества:

- Высокая удельная энергоемкость (100-265 Вт*ч/кг)
- Длительный срок службы (до 2000 циклов)
- Отсутствие эффекта памяти
- Низкий саморазряд
- Возможность быстрого заряда
К недостаткам Li-ion аккумуляторов можно отнести:
- Высокую стоимость
- Деградацию при высоких температурах
- Потенциальную пожароопасность
Несмотря на недостатки, именно литий-ионные батареи сегодня обеспечивают наилучшее сочетание характеристик для электромобилей.
Топливные элементы для электротранспорта
Топливные элементы — перспективный источник энергии для электромобилей. Они преобразуют химическую энергию топлива непосредственно в электрическую. Основные типы топливных элементов для транспорта:
- Щелочные топливные элементы (AFC)
- Топливные элементы с протонообменной мембраной (PEMFC)
- Топливные элементы на основе метанола (DMFC)
Преимущества топливных элементов:
- Высокий КПД (до 60%)
- Экологичность (выделяется только вода)
- Быстрая заправка
- Большой запас хода
Недостатки топливных элементов:
- Высокая стоимость
- Сложность хранения и транспортировки водорода
- Недостаточно развитая инфраструктура
Наиболее перспективными для электротранспорта считаются топливные элементы с протонообменной мембраной (PEMFC). Они обеспечивают высокую удельную мощность при относительно низких рабочих температурах.

Суперконденсаторы в электромобилях
Суперконденсаторы (ультраконденсаторы) — относительно новый тип накопителей энергии. Они занимают промежуточное положение между аккумуляторами и обычными конденсаторами. Основные типы суперконденсаторов:
- Двухслойные конденсаторы
- Псевдоконденсаторы
Ключевые особенности суперконденсаторов:
- Очень высокая удельная мощность (до 10 кВт/кг)
- Практически неограниченное число циклов заряд-разряд
- Быстрый заряд и разряд
- Работа при низких температурах
Недостатки суперконденсаторов:
- Низкая удельная энергоемкость (5-10 Вт*ч/кг)
- Высокий саморазряд
- Высокая стоимость
В электромобилях суперконденсаторы применяются в сочетании с аккумуляторами. Они позволяют эффективно рекуперировать энергию торможения и обеспечивать пиковые нагрузки при разгоне.
Сравнение характеристик источников тока для электромобилей
Рассмотрим основные характеристики различных электрохимических источников тока для электротранспорта:
| Параметр | Li-ion | Ni-MH | PEMFC | Суперконденсатор |
|---|---|---|---|---|
| Удельная энергия, Вт*ч/кг | 100-265 | 60-80 | 500-1000 | 5-10 |
| Удельная мощность, Вт/кг | 250-340 | 200-300 | 100-500 | 1000-10000 |
| КПД, % | 80-90 | 70-80 | 40-60 | 95-98 |
| Число циклов | 500-2000 | 500-1000 | >5000 | >100000 |
Как видно из таблицы, каждый тип источника имеет свои сильные и слабые стороны. Поэтому в современных электромобилях часто применяют гибридные системы питания, сочетающие различные технологии.
Перспективы развития источников тока для электромобилей
Основные направления совершенствования электрохимических источников тока для электротранспорта:
- Повышение удельной энергоемкости литий-ионных аккумуляторов
- Разработка твердотельных литий-ионных батарей
- Создание литий-воздушных и литий-серных аккумуляторов
- Снижение стоимости и повышение эффективности топливных элементов
- Разработка новых материалов для электродов суперконденсаторов
- Создание гибридных накопителей энергии
Ожидается, что в ближайшие годы удельная энергоемкость литий-ионных аккумуляторов возрастет до 300-400 Вт*ч/кг, а их стоимость снизится. Это сделает электромобили еще более привлекательными для потребителей.
Развитие водородных технологий и инфраструктуры заправки может привести к более широкому внедрению топливных элементов в электротранспорте. Это позволит значительно увеличить запас хода и снизить время заправки.
Таким образом, совершенствование электрохимических источников тока играет ключевую роль в развитии электромобильного транспорта. Сочетание различных технологий позволяет создавать все более эффективные и экологичные транспортные средства.

Современные химические источники тока. Гальванические элементы, аккумуляторы, конденсаторы | Библиотека
- 8 октября 2019 г. в 11:39
- 1717
Поделиться
Пожаловаться
Введение
Химические источники тока (ХИТ) являются неотъемлемой и важной частью огромного числа объектов и элементов техники. Они находят широкое применение в автомобильном, напольном (электрокары, электропогрузчики), водном, авиационном, морском и железнодорожном транспорте, входят в состав энергосистем атомных, тепловых и гидроэлектростанций, обеспечивают работу систем связи, телефонных станций и мобильных телефонов, работают совместно с солнечными, ветровыми и приливными генераторами, широко используются в различных приборах, инструментах и оборудовании, в бытовой, медицинской и военной технике. Аккумуляторные батареи можно встретить в космосе в составе космических станций и ракет, в самых глубоких морских впадинах на подводных аппаратах и глубоко под землей. Диапазон емкости аккумуляторов распространяется от 10-9 до 2*104 Ач. Они могут быть размером от 10-9 до 1 м3 . Отдельные аккумуляторы собираются в батареи, создавая системы с мегаваттной мощностью. Если одновременно включить все существующие химические источники тока, то их мощность превысит мощность всех тепловых и гидроэлектростанций.
Диапазон емкости аккумуляторов распространяется от 10-9 до 2*104 Ач. Они могут быть размером от 10-9 до 1 м3 . Отдельные аккумуляторы собираются в батареи, создавая системы с мегаваттной мощностью. Если одновременно включить все существующие химические источники тока, то их мощность превысит мощность всех тепловых и гидроэлектростанций.
Большую роль ХИТ играют в фото- и кинотехнике. Они используются в кино- и видеокамерах, фотоаппаратах, переносных видеомагнитофонах, системах связи, осветительном оборудовании для подводных съемок, различных транспортных средствах, применяемых на съемках,и т.п.
Широкое применение ХИТ в фото- и кинотехнике, а также в системах и оборудовании,обслуживающих процессы кино- и фотосъемок, требует от специалистов умения обоснованно выбирать необходимый источник тока и правильно его эксплуатировать. Для этого нужно иметь представление о работе ХИТ, специфике отдельных электрохимических систем, на базе которых созданы источники. тока. Это позволит максимально эффективно и экономично использовать источники тока.
тока. Это позволит максимально эффективно и экономично использовать источники тока.
Первый химический источник тока был открыт случайно. Итальянский ученый Л. Гальвани, проводя опыты с использованием лягушек, заметил, что одна из них, подвешенная на балконе за медный крючок, при соприкосновении с железным ограждением балкона, начинала дергаться. Было введено понятие «животное» электричество. Позже другой итальянский ученый А. Вольта доказал, что причиной появления электрического тока в опыте с лягушкой является не «животное» электричество, а физико-химические процессы, происходящие при погружении двух различных металлов в электролит. Лягушка оказались лишь чувствительным прибором для обнаружения электричества. В 1800 г. Вольта продемонстрировал первый химический источник тока, собранный путем чередования медных и цинковых кружков, проложенных картоном, смоченным электролитом.
Но был ли это действительно первый ХИТ? В 1936 г. на территории Ирака археолог Кенинг нашел терракотовый сосуд со вставленными в него медным цилиндром и железным стержнем, укрепленным по центру с помощью пробки. Было высказано предположение, что это гальванический элемент, принадлежавший древним шумерам, жившим на планете еще 5000 лет назад. Ученый-археолог предположил, что сосуд заливался каким-либо доступным в те времена электролитом: уксусом, фруктовым соком, морской водой. Найденный сосуд наполнили электролитом и получили электрический ток. Правда, удельная энергия такого гальванического элемента составляла всего 1 Втч/кг. Зачем был нужен шумерам гальванический элемент? Недалеко от найденного сосуда были обнаружены серебряные украшения с тонкой позолотой. Вручную нанести такой тонкий слой золота невозможно. Таким образом, возникла гипотеза о гальваническом нанесении золота с использованием химического источника тока.
Было высказано предположение, что это гальванический элемент, принадлежавший древним шумерам, жившим на планете еще 5000 лет назад. Ученый-археолог предположил, что сосуд заливался каким-либо доступным в те времена электролитом: уксусом, фруктовым соком, морской водой. Найденный сосуд наполнили электролитом и получили электрический ток. Правда, удельная энергия такого гальванического элемента составляла всего 1 Втч/кг. Зачем был нужен шумерам гальванический элемент? Недалеко от найденного сосуда были обнаружены серебряные украшения с тонкой позолотой. Вручную нанести такой тонкий слой золота невозможно. Таким образом, возникла гипотеза о гальваническом нанесении золота с использованием химического источника тока.
Развитие ХИТ шло быстрыми темпами, что определялось большой потребностью в них. Первая свинцово-кислотная батарея была изготовлена Планте в 1859 г., а уже в 1881 r. был испытан первый электромобиль с такой батареей. В 1900 г. Юнгером был изобретен никель-железный аккумулятор, а в 1901 г. Эдисоном — никель-кадмиевый.
Эдисоном — никель-кадмиевый.
…
Скачать Современные источники тока
Смотрите также
Elec.ru в любимой социальной сети Twitter
Актуальные новости, мероприятия, публикации и обзоры в удобном формате.
Подписаться
ХИМИЧЕСКИЕ ИСТОЧНИКИ ТОКА • Большая российская энциклопедия
Авторы: А. М. Скундин, Т. Л. Кулова
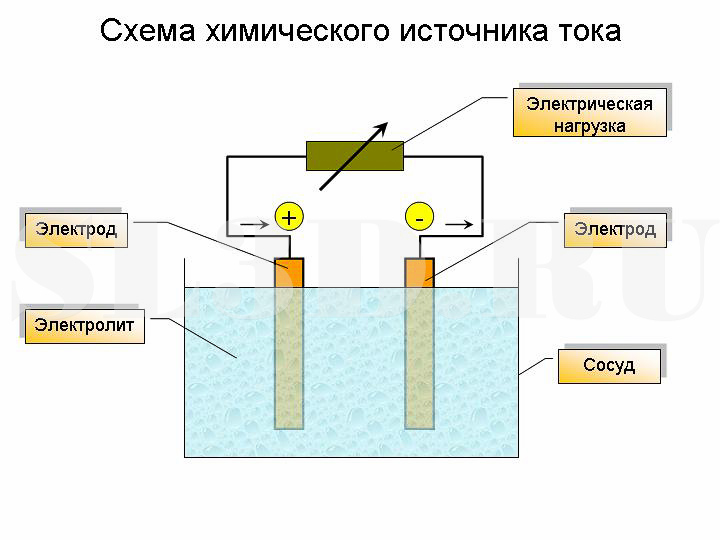
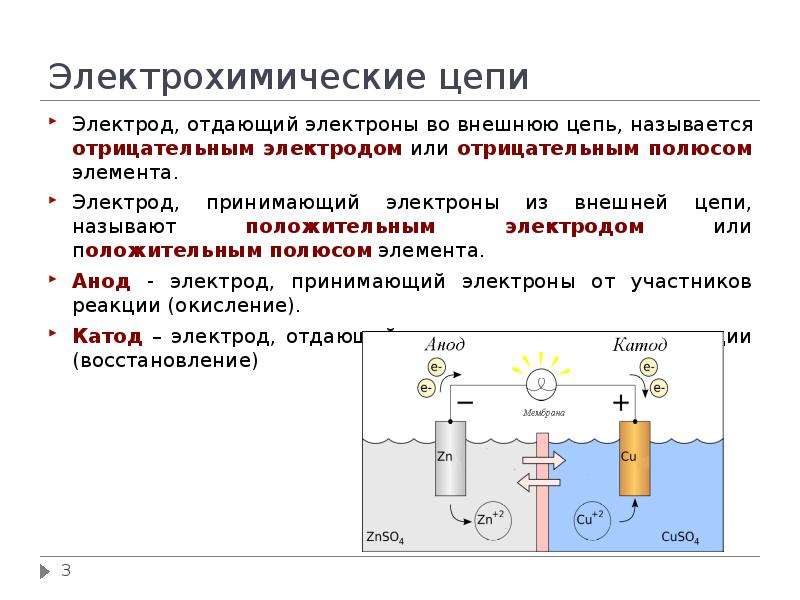
ХИМИ́ЧЕСКИЕ ИСТО́ЧНИКИ ТО́КА, устройства, в которых химич. энергия окислительно-восстановит. реакций преобразуется непосредственно в электрическую. Любой Х. и. т. содержит отрицат. и положит. электроды, изготовленные из электрич. проводников 1-го рода (с электронной проводимостью), которые разделены электролитом – проводником 2-го рода, обладающим ионной проводимостью. Процессы окисления и восстановления в Х. и. т. пространственно разделены: при замыкании внешней цепи на отрицат. электроде протекает окисление восстановителя с выделением электронов во внешнюю цепь, а на положительном – восстановление окислителя с потреблением эквивалентного количества электронов из внешней цепи. Эквивалентное количество ионов переносится при этом через электролит от одного электрода к другому. Совокупность материалов электродов и электролита представляет электрохимич. систему Х. и. т. В условиях разомкнутой цепи ток через Х. и. т. не протекает, а на его электродах устанавливается электродвижущая сила (эдс), которая однозначно определяется электрохимич. системой, т. е. природой токообразующей реакции. Электрод, на котором протекает реакция окисления, называется анодом; электрод, на котором протекает восстановление, – катодом. Значение эдс разл. Х. и. т. колеблется от 0,5 до 4,0 В. Для удобства эксплуатации Х. и. т. часто соединяют в последовательные батареи. Для получения больших токов разряда используют параллельное соединение химич. источников тока.
Эквивалентное количество ионов переносится при этом через электролит от одного электрода к другому. Совокупность материалов электродов и электролита представляет электрохимич. систему Х. и. т. В условиях разомкнутой цепи ток через Х. и. т. не протекает, а на его электродах устанавливается электродвижущая сила (эдс), которая однозначно определяется электрохимич. системой, т. е. природой токообразующей реакции. Электрод, на котором протекает реакция окисления, называется анодом; электрод, на котором протекает восстановление, – катодом. Значение эдс разл. Х. и. т. колеблется от 0,5 до 4,0 В. Для удобства эксплуатации Х. и. т. часто соединяют в последовательные батареи. Для получения больших токов разряда используют параллельное соединение химич. источников тока.
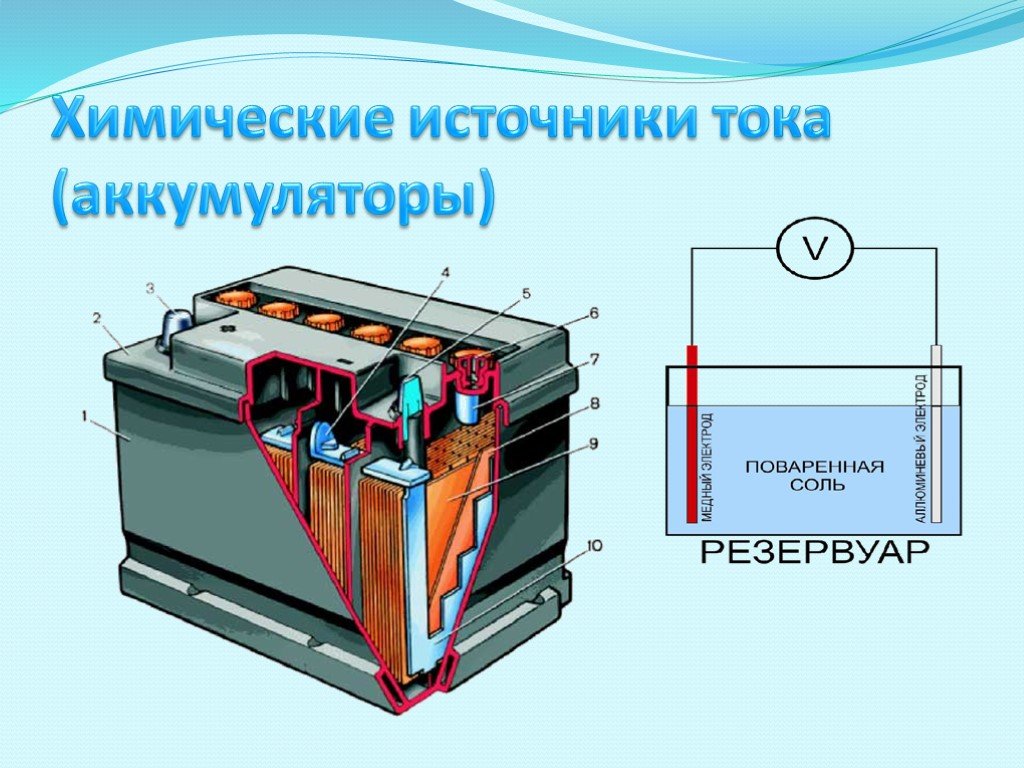
Различают первичные, или одноразовые, Х. и. т. – гальванические элементы, и вторичные, или перезаряжаемые, Х.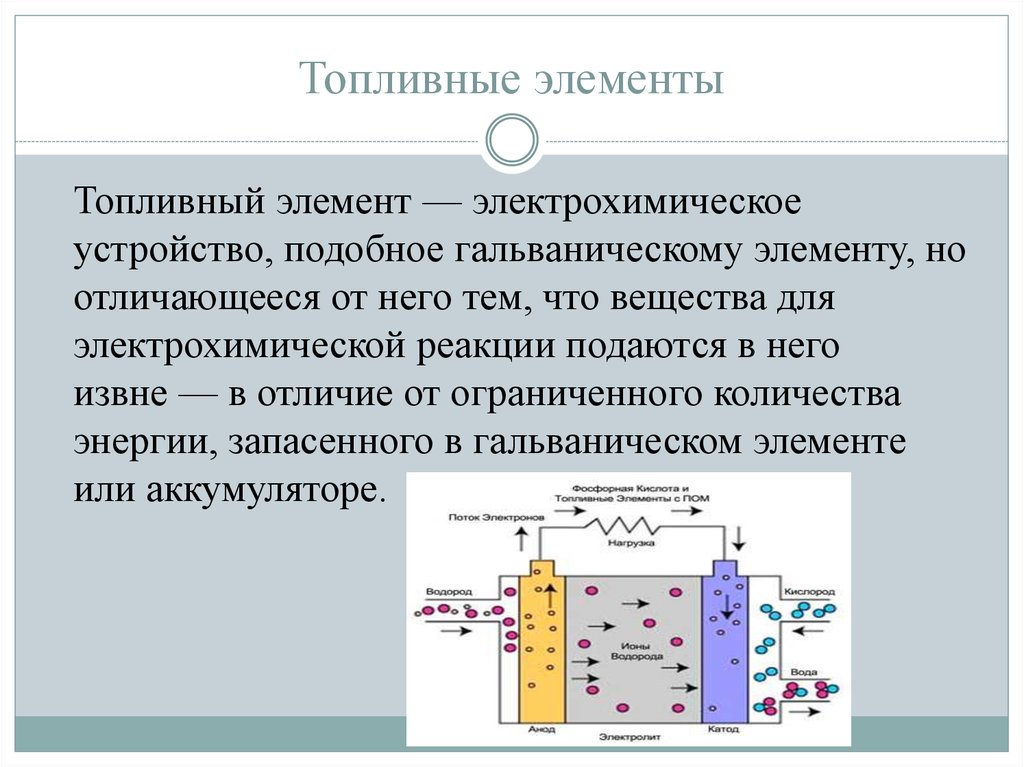 и. т. – аккумуляторы. В тех и других устройствах активные вещества, участвующие в токообразующей реакции, находятся непосредственно в электродах. После окончания разряда, т. е. после исчерпания запаса активных веществ, первичные элементы выходят из строя, а аккумуляторы могут быть вновь переведены в работоспособное состояние путём заряда, т. е. пропусканием тока в направлении, обратном заряду. На электродах при этом протекают те же реакции, что и при разряде, но в обратном направлении. Аккумуляторы могут быть перезаряжены неск. сотен раз. Процесс последовательного заряда и разряда аккумуляторов называют циклированием. Важная разновидность первичных элементов (которую обычно выделяют в отд. самостоят. категорию) – топливные элементы, в которых происходит только процесс токообразования, а активные вещества хранятся отдельно и подаются в элемент по мере необходимости.
и. т. – аккумуляторы. В тех и других устройствах активные вещества, участвующие в токообразующей реакции, находятся непосредственно в электродах. После окончания разряда, т. е. после исчерпания запаса активных веществ, первичные элементы выходят из строя, а аккумуляторы могут быть вновь переведены в работоспособное состояние путём заряда, т. е. пропусканием тока в направлении, обратном заряду. На электродах при этом протекают те же реакции, что и при разряде, но в обратном направлении. Аккумуляторы могут быть перезаряжены неск. сотен раз. Процесс последовательного заряда и разряда аккумуляторов называют циклированием. Важная разновидность первичных элементов (которую обычно выделяют в отд. самостоят. категорию) – топливные элементы, в которых происходит только процесс токообразования, а активные вещества хранятся отдельно и подаются в элемент по мере необходимости. Согласно Фарадея законам, существует прямая пропорциональность между количеством электричества, вырабатываемого Х. и. т., и количеством израсходованных активных веществ. Следовательно, скорость израсходования активных веществ строго пропорциональна току разряда. Т. о., количество электричества, которое может выработать Х. и. т., или его ёмкость, пропорционально количеству заложенных в него активных веществ. Осн. характеристики Х. и. т.: напряжение, максимально допустимый ток разряда, температурный диапазон работоспособности.
Согласно Фарадея законам, существует прямая пропорциональность между количеством электричества, вырабатываемого Х. и. т., и количеством израсходованных активных веществ. Следовательно, скорость израсходования активных веществ строго пропорциональна току разряда. Т. о., количество электричества, которое может выработать Х. и. т., или его ёмкость, пропорционально количеству заложенных в него активных веществ. Осн. характеристики Х. и. т.: напряжение, максимально допустимый ток разряда, температурный диапазон работоспособности.
Первый Х. и. т. создал А. Вольта в 1800, и с этого момента началась эра электричества. Широкое распространение имеют марганцево-цинковые, марганцево-литиевые, фторуглеродно-литиевые первичные элементы, а также свинцовые (кислотные), никель-кадмиевые и никель-металлгидридные (щелочные) и литий-ионные аккумуляторы.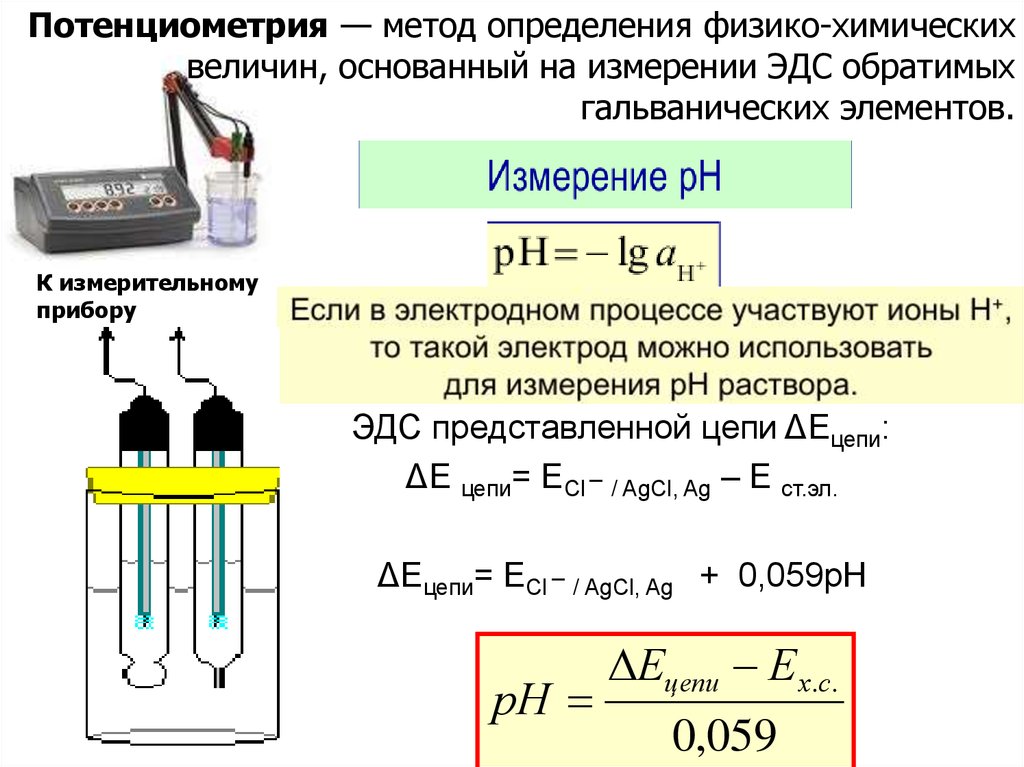 Производятся и находятся в эксплуатации водородно-кислородные (водородно-воздушные) топливные элементы с полимерным электролитом, с расплавленным карбонатным электролитом и с твёрдым оксидным электролитом. В качестве эталонов напряжения используют нормальные элементы, имеющие воспроизводимое с точностью до 1·10–5 В напряжение.
Производятся и находятся в эксплуатации водородно-кислородные (водородно-воздушные) топливные элементы с полимерным электролитом, с расплавленным карбонатным электролитом и с твёрдым оксидным электролитом. В качестве эталонов напряжения используют нормальные элементы, имеющие воспроизводимое с точностью до 1·10–5 В напряжение.
Осн. сферы применения Х. и. т. – энергообеспечение портативной аппаратуры (от мобильных телефонов до игрушек), обеспечение старта двигателей внутр. сгорания, обеспечение энергией транспортных средств, сглаживание нагрузок в электросетях, обеспечение аварийного электроснабжения и т. п. Эти области применения составляют малую энергетику, в отличие от большой энергетики, связанной со стационарными электросетями.
Обзор электрохимических источников энергии для электромобилей и гибридных транспортных средств
Обзор: в этом блоге рассматриваются новые электрохимические источники энергии для приложений EV/HEV.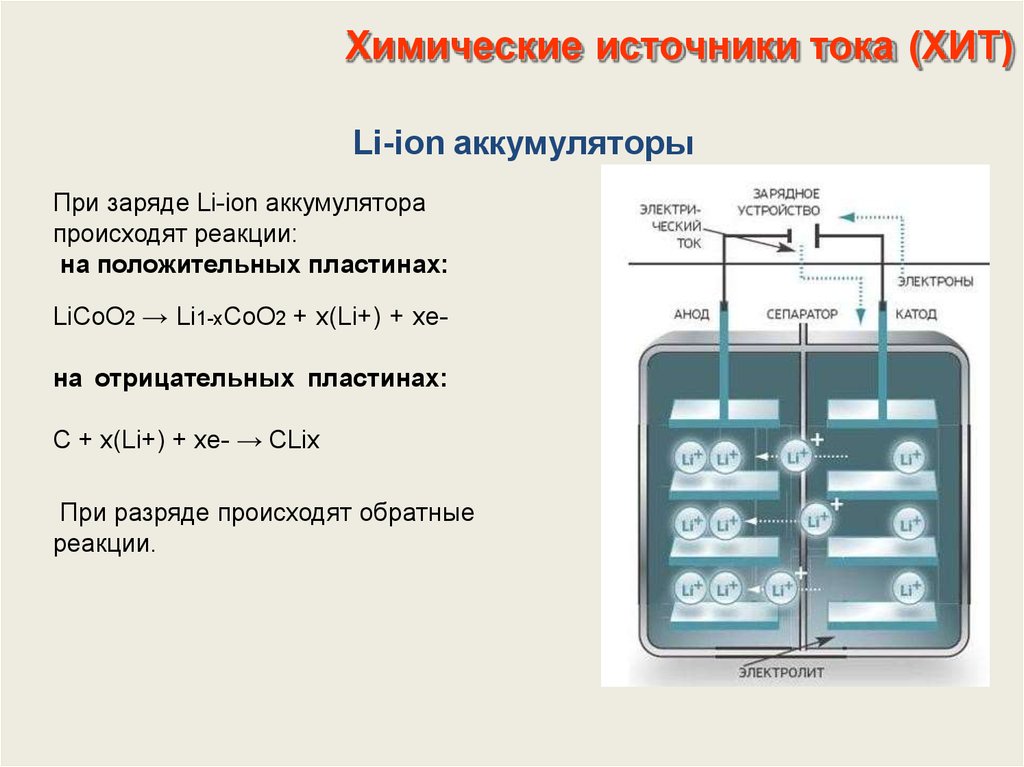 Также обсуждаются особенности, преимущества и недостатки каждого источника энергии.
Также обсуждаются особенности, преимущества и недостатки каждого источника энергии.
Значительный интерес был проявлен к электромобилям, особенно к электромобилям и гибридным электромобилям. Ожидается, что к 2040 году продажи электрических и гибридных электромобилей превысят продажи бензиновых и дизельных автомобилей. Цель этого исследования — предоставить критический обзор электрохимической энергии, разрабатываемой для использования в электромобилях и гибридных автомобилях.
Электрохимические источники энергии
Приводы электродвигателей и другие вспомогательные компоненты электромобилей/ГЭМ, такие как системы отопления, вентиляции и кондиционирования воздуха, освещения и аудио- и видеотехники, могут питаться от электрохимических источников энергии. Доступные в настоящее время электрохимические источники энергии могут давать либо высокую удельную выходную мощность, либо высокую удельную выходную мощность, но не то и другое одновременно. Батареи, топливные элементы и ультраконденсаторы — это только три из множества электрохимических источников энергии, представленных в настоящее время на рынке.
Батареи
Батарея — это устройство, которое может преобразовывать электрохимическую энергию активных материалов в электрическую энергию. Обычная батарея состоит из трех основных компонентов: положительного электрода, отрицательного электрода и электролита. Свинцово-кислотная батарея, батарея на основе никеля или батарея на основе лития являются тремя наиболее распространенными вариантами для приложений EV/HEV.
-
Свинцово-кислотные аккумуляторы
В некоторых из первых электромобилей и гибридных электромобилей использовались свинцово-кислотные аккумуляторы, и эти аккумуляторы уже давно поступили в продажу. Положительный электрод стандартной свинцово-кислотной батареи изготовлен из диоксида свинца, а отрицательный электрод — из металлического свинца. Усовершенствованные свинцово-кислотные аккумуляторы, также известные как свинцово-кислотные аккумуляторы с регулируемой стоимостью (VRLA), используют два различных типа электролита — абсорбированный электролит и гелеобразный электролит — вместо одного.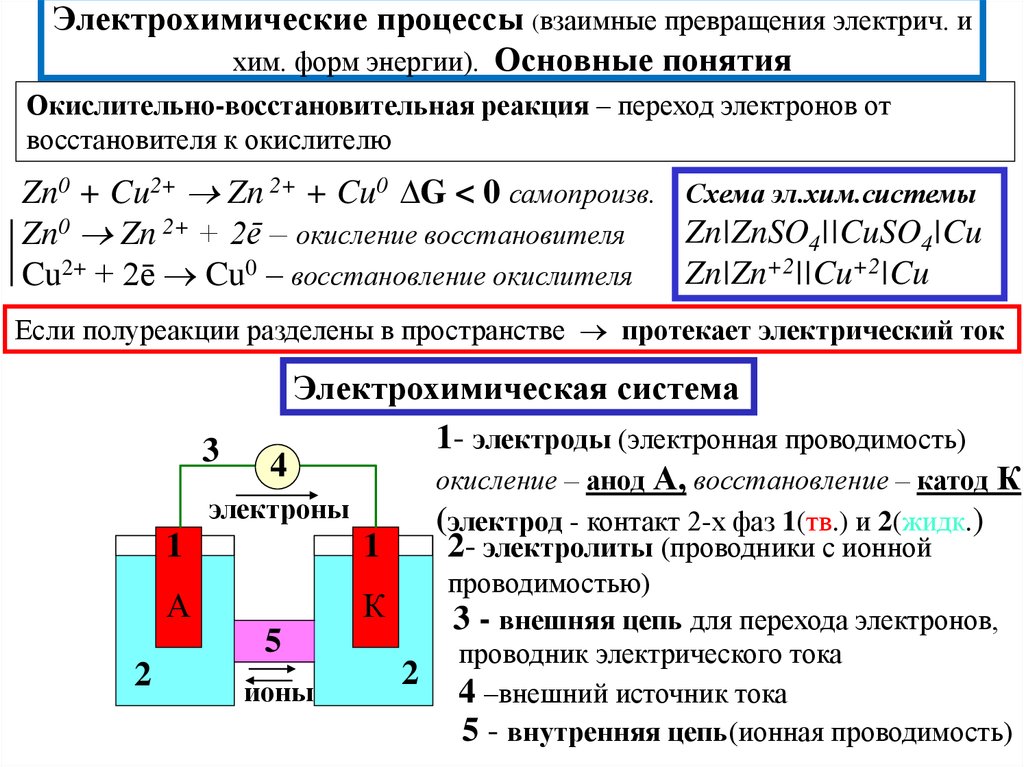 По сравнению со стандартными батареями двойная конструкция батарей VRLA значительно снижает испарение, утечку и вибрацию.
По сравнению со стандартными батареями двойная конструкция батарей VRLA значительно снижает испарение, утечку и вибрацию.
Многочисленные типы аккумуляторов на основе никеля, в том числе никель-железные (Ni-Fe), никель-кадмиевые (Ni-Cd), никель-цинковые (Ni-Zn) и никель-металлгидридные (Ni-Fe). MH) используются в различных приложениях, включая электромобили и гибридные автомобили. Батарея Ni-MH, в которой в качестве электролита используется раствор гидроксида калия, а в качестве положительного и отрицательного электродов — гидроксид никеля, является наиболее широко используемой батареей в электромобилях и гибридных автомобилях.
Проблемы с хранением, транспортировкой и использованием металлического лития являются одними из самых серьезных в отрасли. Таким образом, литий-ионная (Li-ion) батарея формируется путем замены металлического лития промежуточным материалом, который в противном случае служил бы отрицательным электродом. Положительный и отрицательный электроды типичной литий-ионной батареи состоят из интеркаляционных соединений лития.
Таблица 1. Сравнение типовых батарей. Источник: Ли и др.
Удельная энергия, удельная мощность и срок службы — три важных ключевых показателя, обычно используемых для оценки производительности батареи. Удельная энергия батареи — это ее общая потенциальная энергия, тогда как ее удельная мощность — это количество энергии, которое она фактически отдает за определенный период времени. Срок службы батареи определяется как количество раз, которое она может быть заряжена и разряжена, прежде чем проявится какой-либо заметный износ. Таблица 1 содержит сводку основных различий и сходств между распространенными типами аккумуляторов.
Топливные элементы
Топливный элемент — это тип электрохимического источника энергии, который может преобразовывать химическую энергию в электрическую.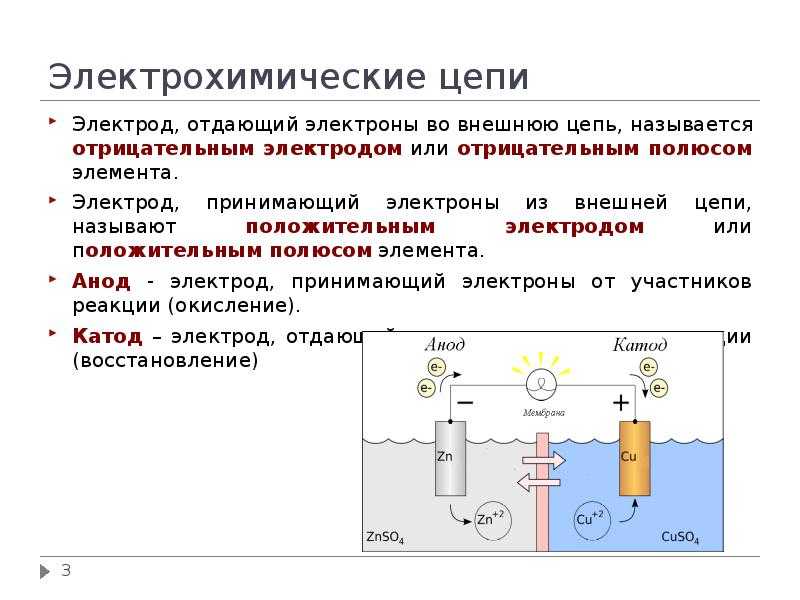 Щелочные топливные элементы (AFC), топливные элементы с фосфорной кислотой (PAFC), топливо с протонообменной мембраной (PEMFC) и топливные элементы с прямым метанолом — это четыре жизнеспособных варианта применения EV/HEV (DMFC).
Щелочные топливные элементы (AFC), топливные элементы с фосфорной кислотой (PAFC), топливо с протонообменной мембраной (PEMFC) и топливные элементы с прямым метанолом — это четыре жизнеспособных варианта применения EV/HEV (DMFC).
Используя только водород, кислород и рециркулирующий электролит, AFC были широко признаны первыми действительно жизнеспособными топливными элементами. Его превосходная эффективность, развитая технология и низкая стоимость являются неоспоримыми преимуществами. Матрица насыщается щелочным раствором, разделяющим два пористых электрода. Гидроксид калия (KOH) часто используется из-за его высокой эффективности теплопередачи в AFC. Для функционирования АФК должна иметь место окислительно-восстановительная реакция.
PAFC широко известен как первый коммерческий топливный элемент в электроэнергетике. Он использует жидкую фосфорную кислоту в качестве электролита, а уголь с платиновым покрытием является катализатором. Электроны могут перемещаться от отрицательного электрода к положительному через внешнюю цепь, в то время как положительно заряженные ионы водорода могут переходить от положительного электрода к отрицательному через кислый электролит. Поскольку PAFC должен работать в относительно более высоком диапазоне температур, в качестве электролита обычно используется фосфорная кислота. Когда PAFC вырабатывает электроэнергию, в качестве побочного продукта производится вода.
Электроны могут перемещаться от отрицательного электрода к положительному через внешнюю цепь, в то время как положительно заряженные ионы водорода могут переходить от положительного электрода к отрицательному через кислый электролит. Поскольку PAFC должен работать в относительно более высоком диапазоне температур, в качестве электролита обычно используется фосфорная кислота. Когда PAFC вырабатывает электроэнергию, в качестве побочного продукта производится вода.
Топливный элемент с протонообменной мембраной (PEMFC), также известный как топливный элемент с ионообменной мембраной или топливный элемент с твердым полимерным электролитом, использует в качестве электролита протонпроводящую мембрану. PEMFC был первым топливным элементом, использованным НАСА для космической программы Gemini в 1960-х годах, и он известен своей высокой удельной мощностью. Чтобы продлить целостность мембраны и срок службы, этот тип топливных элементов часто работает при низкой температуре, что требует использования дорогостоящего платинового металлического катализатора для химических процессов. Как и PAFC, PEMFC производит воду как побочный продукт производства электроэнергии.
Как и PAFC, PEMFC производит воду как побочный продукт производства электроэнергии.
Топливные элементы прямого действия на метаноле (DMFC) выгодны тем, что в них используется легкодоступное топливо, которое относительно легко хранить. Тем временем метанол можно косвенно преобразовать в виде комбинации газов водородного риформинга и хранить в топливном элементе (IMFC). Как и в случае с другими топливными элементами, IMFC работает наиболее эффективно при подаче водорода. Способность DMFC генерировать углекислый газ и воду зависит от его конструкции.
Таблица 2. Сравнение типовых топливных элементов. Источник: Ли и др.
Для оценки функционирования топливных элементов используются четыре основных критических показателя: обычное топливо, удельная мощность, температура и КПД. Температура — это рабочая температура, тогда как удельная мощность — это общая мощность, вырабатываемая полной ячейкой на единицу объема. В таблице 2 приведены сравнения между типичными целыми ячейками.
Ультраконденсаторы
Конденсатор представляет собой основное устройство, которое накапливает и высвобождает электроны с помощью диэлектрика между двумя металлическими электродами. Есть две основные разновидности классических конденсаторов; электростатические конденсаторы и электролитические конденсаторы. В отличие от последнего, первый не использует электролитические материалы. На данный момент ни у кого нет достаточной мощности для использования EV / HEV. Одним из обнадеживающих ответов на эту проблему является ультраконденсатор, относительно новая технология, представленная в двух основных вариантах: двухслойный конденсатор и псевдоконденсатор.
Для хранения заряда с разделенными поверхностью электрода и электролитом была разработана концепция двухслойного конденсатора. Используя последние достижения в области нанотехнологий, можно создавать высокопористые материалы для использования в качестве электродов конденсаторов. Высокая емкость двухслойного конденсатора стала возможной благодаря этому новому свойству материала.
-
Псевдоконденсатор
Для псевдоконденсатора процессы зарядки и разрядки представляют собой химические реакции, известные как процесс Фарадея, и события окисления-восстановления, происходящие на границе раздела, выделяют его. Псевдоконденсаторы, в которых используется метод Фарадея, обычно обеспечивают большую емкость и плотность энергии, чем двухслойные конденсаторы.
Рис. 1. Сравнение различных источников энергии для ЭМ/ГЭМ. Источник: Ли и др.
На рис. 1 показано сравнение аккумуляторов, топливных элементов, конденсаторов и ультраконденсаторов и бензина — четырех наиболее важных электрохимических источников энергии.
Подводя итоги по ключевым моментам:
Вот некоторые выводы из статьи:
- В настоящее время коммерчески доступны несколько различных типов электрохимических источников энергии, включая батареи, топливные элементы и ультраконденсаторы.

- В большинстве электромобилей и гибридных автомобилей используются либо свинцово-кислотные батареи, либо батареи на основе никеля, либо батареи на основе лития.
- Общепринятой практикой является оценка стоимости батареи путем измерения ее удельной энергии, удельной мощности и срока службы.
- Топливные элементы представляют собой электрохимический источник энергии, преобразующий химическую энергию в электрическую.
- Четыре возможных варианта применения EV/HEV: щелочной топливный элемент (AFC), топливный элемент на фосфорной кислоте (PAFC), топливный элемент с протонообменной мембраной (PEMFC) и топливный элемент с прямым метанолом (DMFC).
- Ультраконденсатор — это тип современного конденсатора, который может быть либо двухслойным, либо псевдоконденсатором.
- Идея двухслойного конденсатора была создана для хранения заряда с физически разделенными поверхностью электрода и электролитом.
- Псевдоконденсаторы, в которых используется метод Фарадиев, часто превосходят двухслойные конденсаторы по емкости и плотности энергии.
Эта запись в блоге является частью полной исследовательской статьи, опубликованной в IEEE Access .
«Электрохимические источники энергии: батареи, топливные элементы и суперконденсаторы»
«Электрохимические источники энергии: батареи, топливные элементы и суперконденсаторы» — technology.matthey.com«Электрохимические источники энергии: батареи, топливные элементы и суперконденсаторы»
Английский (китайский)
Архив журнала
Johnson Matthey Technol. Рев., 2015 г.,
59 , (4), 319
дои:
10.1595/205651315X689496
«Электрохимические источники энергии: батареи, топливные элементы и суперконденсаторы»
Владимир С.
 Баготский, Александр М. Скундин и Юрий М. Вольфкович (Институт физической химии и электрохимии им. А.Н. Фрумкина РАН, Россия), John Wiley & Sons Inc., Нью-Джерси, США, 2015, 372 стр. , ISBN: 978-1-118-46023-6, 66,95 фунтов стерлингов, 81,99 евро, 99,95 долларов США
Баготский, Александр М. Скундин и Юрий М. Вольфкович (Институт физической химии и электрохимии им. А.Н. Фрумкина РАН, Россия), John Wiley & Sons Inc., Нью-Джерси, США, 2015, 372 стр. , ISBN: 978-1-118-46023-6, 66,95 фунтов стерлингов, 81,99 евро, 99,95 долларов США Поделиться этой страницей:
- Твиттер
- Фейсбук
- Реддит
- Дигг
- СМЕШИВАНИЕ
«Электрохимические источники питания: аккумуляторы, топливные элементы и суперконденсаторы» представляет собой исчерпывающий учебник, описывающий материалы, области применения и перспективы вышеупомянутых устройств. Предоставленный обзор высокого уровня делает эту книгу отличным ресурсом для читателей, плохо знакомых с электрохимическими устройствами, поскольку он позволяет избежать чрезмерной детализации каждого материала, в то же время предоставляя общую перспективу и перспективы. Книга вышла под редакцией Александра Скундина и Юрия Вольфковича в честь покойного Владимира Баготского, получившего широкое признание за свою научную деятельность в области электрохимии и за свои учебники по этому предмету. Сами Скундин и Вольфкович являются главными учеными Института им. Фрумкина Российской академии наук и являются двумя ведущими экспертами в области аккумуляторов и суперконденсаторов в России с более чем 200 рецензируемыми статьями.
Книга вышла под редакцией Александра Скундина и Юрия Вольфковича в честь покойного Владимира Баготского, получившего широкое признание за свою научную деятельность в области электрохимии и за свои учебники по этому предмету. Сами Скундин и Вольфкович являются главными учеными Института им. Фрумкина Российской академии наук и являются двумя ведущими экспертами в области аккумуляторов и суперконденсаторов в России с более чем 200 рецензируемыми статьями.
Книга охватывает три основные темы: аккумуляторы, топливные элементы и суперконденсаторы, причем в каждом разделе обсуждаются основные принципы работы, материалы и перспективы технологии.
Применение электрохимических устройств
Электрохимические устройства используются в различных областях, от бытовой электроники до электромобилей, благодаря их относительно высокой эффективности и экологичности. Однако основные проблемы включают увеличение энергии, удельной мощности и эффективности этих устройств, особенно при переходе от нового материала или химии. Поэтому оценка исторических работ, общих проблем и потенциального будущего положения технологии чрезвычайно полезна.
Поэтому оценка исторических работ, общих проблем и потенциального будущего положения технологии чрезвычайно полезна.
Аккумуляторы
Первая часть книги посвящена термодинамическим аспектам электрохимических устройств с акцентом на водные окислительно-восстановительные пары, которые исторически рассматривались для применения в батареях. Рассмотрены общий принцип работы гальванических элементов, а также различные химические составы электродов, включая батареи на основе цинка, никеля и свинцово-кислотные батареи. Далее следует раздел с объяснением показателей качества, относящихся к батареям, и соображений по проектированию при переводе химии материалов в системы на уровне элементов с учетом сопутствующих сепаратора и электролита. Затем обобщаются области применения технологии, текущие ограничения и перспективы технологии.
Следующий раздел ведет к неводным системам, которые в настоящее время наиболее распространены в реальных приложениях. Здесь дается общее введение в различные типы электролитов, включая апротонные неводные растворы, расплавы солей и твердые электролиты. Затем следует обсуждение литий-ионных электродов на основе интеркаляции с их обзором, в котором делается вывод о том, что существующие материалы не смогут удовлетворить требования потребителей по плотности энергии и скорости зарядки. Поэтому они считают, что потребуется переход на альтернативные материалы, т. е. кремний, олово или алюминий, однако в этом случае срок службы становится ограничивающим фактором, а микроструктурные повреждения приводят к сокращению срока службы.
Затем следует обсуждение литий-ионных электродов на основе интеркаляции с их обзором, в котором делается вывод о том, что существующие материалы не смогут удовлетворить требования потребителей по плотности энергии и скорости зарядки. Поэтому они считают, что потребуется переход на альтернативные материалы, т. е. кремний, олово или алюминий, однако в этом случае срок службы становится ограничивающим фактором, а микроструктурные повреждения приводят к сокращению срока службы.
Их оценка грядущих аккумуляторных технологий с точки зрения повышения плотности энергии затем концентрируется на химическом анализе, основанном на конверсии, и, таким образом, на отходе от традиционных механизмов, основанных на интеркаляции. Литий-серные, литий-воздушные и натрий-ионные батареи обсуждаются с выявленными проблемами, которые снова связаны с проблемами срока службы, связанными с микроструктурными изменениями, происходящими в электродах, и гистерезисом напряжения, наблюдаемым при зарядке и разрядке, что ограничивает эффективность устройства.
В последних главах этого раздела кратко рассматриваются твердотельные батареи и батареи с расплавленными солевыми электролитами, которые исследователи исследовали, чтобы обеспечить длительный срок службы устройств, однако другие трудности, такие как проводимость электролита, в настоящее время ограничивают их широкое распространение.
Топливные элементы
Вторая часть посвящена топливным элементам, имеющим отношение как к транспортным, так и к стационарным энергетическим установкам. Опять же, это начинается с термодинамических аспектов работы устройства и основных определений компонентов и концепций, используемых в топливных элементах. В последующих разделах затем приводится более подробное объяснение различных типов: топливный элемент с протонообменной мембраной (PEMFC), топливный элемент с прямым метанолом (DMFC), топливный элемент с расплавленным карбонатом (MCFC), твердооксидный топливный элемент (SOFC) и щелочной топливный элемент ( АФК). Для PEMFC, наиболее подходящих для использования в автомобилях, дается исторический обзор, охватывающий развитие технологии, но он также затрагивает инженерные проблемы, такие как управление температурным режимом, холодный пуск и управление водой. Затем следует прогресс и сложности каждой технологии топливных элементов с кратким обзором фосфорной кислоты (PAFC), прямого углеродного топливного элемента (DCFC), бактериального топливного элемента (BFC) и проточной окислительно-восстановительной батареи (RFB). В частности, RFB привлекают большое внимание в индустрии крупномасштабных накопителей энергии из-за их потенциальной экономии средств и увеличения срока службы по сравнению с батареями с обычными обсуждаемыми полностью ванадиевыми и железо-хромовыми RFB.
Затем следует прогресс и сложности каждой технологии топливных элементов с кратким обзором фосфорной кислоты (PAFC), прямого углеродного топливного элемента (DCFC), бактериального топливного элемента (BFC) и проточной окислительно-восстановительной батареи (RFB). В частности, RFB привлекают большое внимание в индустрии крупномасштабных накопителей энергии из-за их потенциальной экономии средств и увеличения срока службы по сравнению с батареями с обычными обсуждаемыми полностью ванадиевыми и железо-хромовыми RFB.
Раздел завершается обсуждением применения топливных элементов, и кратко излагаются исторически установленные блоки топливных элементов для стационарных приборов. Только ПОМТЭ привлекла значительное внимание промышленности к использованию в автомобилестроении, и авторы предполагают, что первоначальные успехи связаны с грузовыми автомобилями. Их технологические взгляды подчеркивают их интерпретацию предстоящих вопросов, связанных с разработкой новых катализаторов для восстановления кислорода, катализаторов для полного окисления этанола и селективных катализаторов, которые не способствуют нежелательным побочным реакциям.
Суперконденсаторы
В третьем разделе основное внимание уделяется электрохимическим конденсаторам с двойным слоем или суперконденсаторам, в первую очередь рассматривая системы на основе углерода, которые имеют наибольшее промышленное значение. Здесь они представляют подробный анализ оптимизации электродов для различных видов углерода, таких как активированный уголь, карбидные производные, аэрогели, нанотрубки и графен, с различными типами электролитов с точки зрения распределения пор по размерам и влияния функциональных групп. Затем следует обсуждение ряда типов электролитов: водные, неводные и ионные жидкости.
Наблюдения показывают, что в конечном итоге дальнейшее увеличение удельной поверхности электродов за счет уменьшения размеров пор не приведет к улучшению плотности энергии суперконденсатора из-за влияния стерических эффектов. Таким образом, наблюдается повышенный интерес к материалам электродов псевдоконденсаторов, которые включают оксиды металлов, такие как оксид иридия (IV) (IrO 2 ), оксид марганца (IV) (MnO 2 ) и оксид рутения (IV) (RuO 2).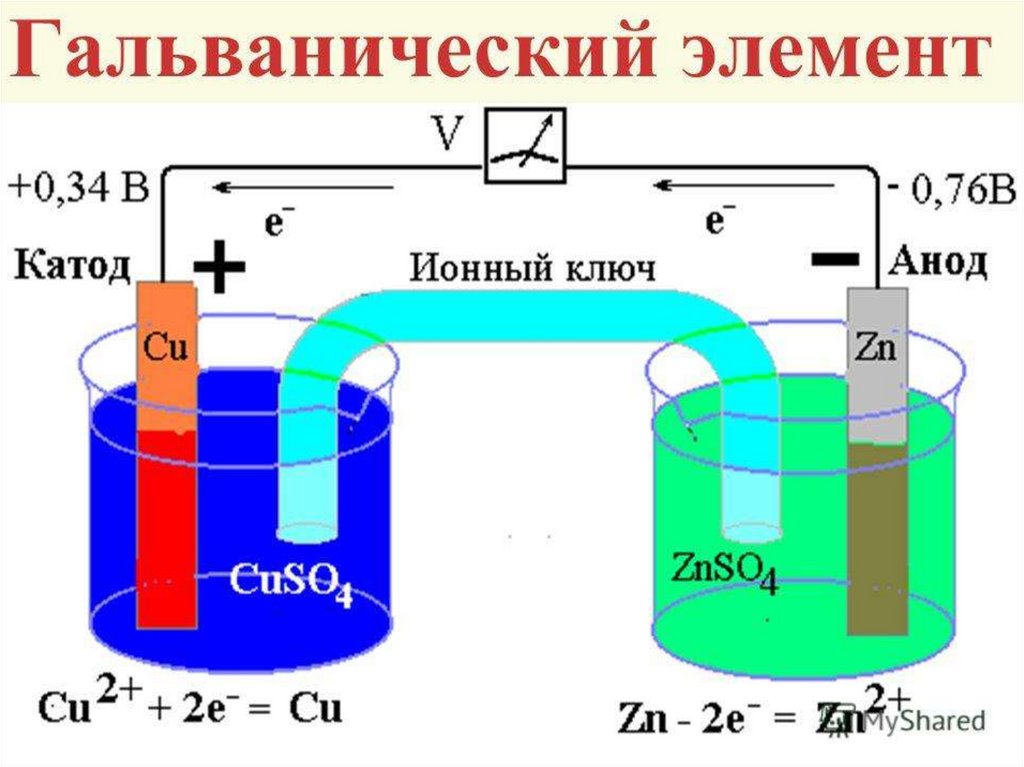 ), проводящие полимеры и мономерные окислительно-восстановительные системы. В этом тексте дается всесторонний обзор этих электродных материалов, проблем и перспектив, в отношении которых наблюдается текущая тенденция к созданию композитных электродов из оксидов металлов и проводящих полимеров для смягчения проблем с проводимостью оксидов металлов и достижения более высоких массовых нагрузок для более практичные устройства.
), проводящие полимеры и мономерные окислительно-восстановительные системы. В этом тексте дается всесторонний обзор этих электродных материалов, проблем и перспектив, в отношении которых наблюдается текущая тенденция к созданию композитных электродов из оксидов металлов и проводящих полимеров для смягчения проблем с проводимостью оксидов металлов и достижения более высоких массовых нагрузок для более практичные устройства.
Подробное обсуждение электродов суперконденсаторов на основе углерода и электродов псевдоконденсаторов затем приводит к асимметричным суперконденсаторам, которые объединяют их вместе, чтобы обеспечить более высокую плотность энергии благодаря более широкому диапазону рабочего напряжения. Размышляя обо всем этом, раздел завершается сравнением имеющихся в продаже суперконденсаторов и перспектив устройства.
Фотоэлектрохимические устройства
Заключительная глава книги посвящена электрохимическим аспектам преобразования солнечной энергии. Это дает очень краткий обзор механизмов фотоэлектрохимических устройств, таких как полупроводниковые солнечные батареи и солнечные элементы, сенсибилизированные красителем.
Это дает очень краткий обзор механизмов фотоэлектрохимических устройств, таких как полупроводниковые солнечные батареи и солнечные элементы, сенсибилизированные красителем.
Выводы
«Электрохимические источники энергии: батареи, топливные элементы и суперконденсаторы» — превосходный вводный текст по электрохимическим энергетическим устройствам, который охватывает материальные соображения, исторические разработки технологии и перспективы на будущее, охватывая фундаментальные механизмы и инженерные задачи на высоком уровне. уровневая перспектива. В частности, в разделе о суперконденсаторах гораздо более подробно рассматриваются материалы. Этот текст будет наиболее полезен для студентов, изучающих курс «Введение в электрохимию».
«Электрохимические источники энергии: батареи, топливные элементы и суперконденсаторы» ССЫЛКА http://www.wiley.com/WileyCDA/WileyTitle/productCd-1118460235,subjectCd-EG32.html преподает в Школе инженерного дизайна Дайсона при Имперском колледже Лондона, где работает над электрохимическими устройствами в различных масштабах, от новых материалов до инженерной интеграции.

